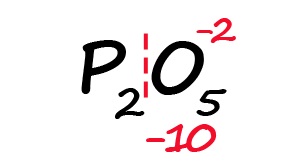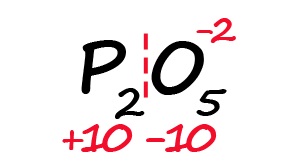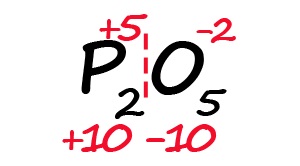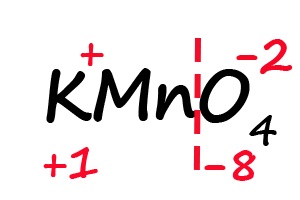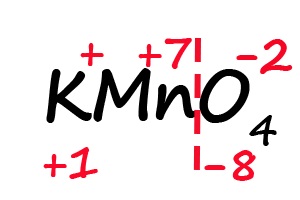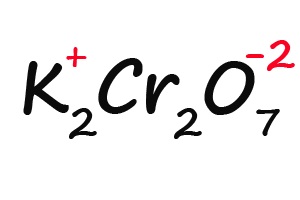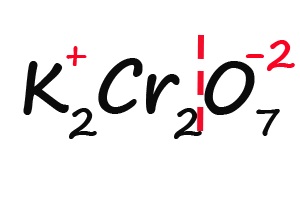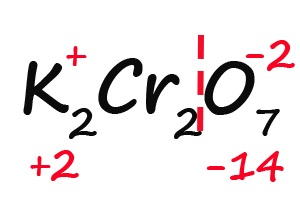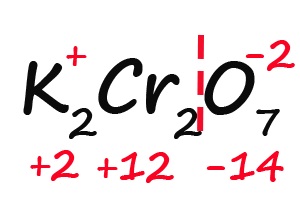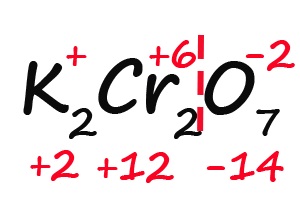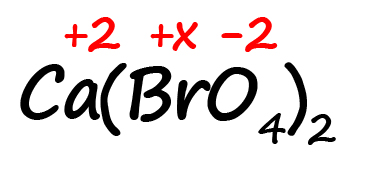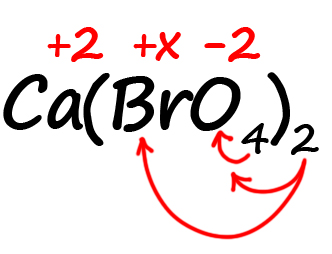Кальций в таблице менделеева занимает 20 место, в 4 периоде.
| Символ | Ca |
| Номер | 20 |
| Атомный вес | 40.0780000 |
| Латинское название | Calcium |
| Русское название | Кальций |
Как самостоятельно построить электронную конфигурацию? Ответ здесь
Электронная схема кальция
Ca: 1s2 2s2 2p6 3s2 3p6 4s2
Короткая запись:
Ca: [Ar]4s2
Одинаковую электронную конфигурацию имеют
атом кальция и
K-1, Sc+1, Ti+2, V+3, Mn+5, Fe+6
Порядок заполнения оболочек атома кальция (Ca) электронами:
1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d →
5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
На подуровне ‘s’ может находиться до 2 электронов, на ‘s’ — до 6, на
‘d’ — до 10 и на ‘f’ до 14
Кальций имеет 20 электронов,
заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
6 электронов на 2p-подуровне
2 электрона на 3s-подуровне
6 электронов на 3p-подуровне
2 электрона на 4s-подуровне
Степень окисления кальция
Атомы кальция в соединениях имеют степени окисления 2.
Степень окисления — это условный заряд атома в соединении: связь в молекуле
между атомами основана на разделении электронов, таким образом, если у атома виртуально увеличивается
заряд, то степень окисления отрицательная (электроны несут отрицательный заряд), если заряд уменьшается,
то степень окисления положительная.
Ионы кальция
Валентность Ca
Атомы кальция в соединениях проявляют валентность II.
Валентность кальция характеризует способность атома Ca к образованию хмических связей.
Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании
химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа Ca
Квантовые числа определяются последним электроном в конфигурации,
для атома Ca эти числа имеют значение N = 4, L = 0, Ml = 1, Ms = -½
Видео заполнения электронной конфигурации (gif):
Результат:
Энергия ионизации
Чем ближе электрон к центру атома — тем больше энергии необходимо, что бы его оторвать.
Энергия, затрачиваемая на отрыв электрона от атома называется энергией ионизации и обозначается Eo.
Если не указано иное, то энергия ионизации — это энергия отрыва первого электрона, также существуют энергии
ионизации для каждого последующего электрона.
Энергия ионизации Ca:
Eo = 590 кДж/моль
— Что такое ион читайте в статье.
Перейти к другим элементам таблицы менделеева
Где Ca в таблице менделеева?
Таблица Менделеева
Скачать таблицу менделеева в хорошем качестве
Как определить степень окисления
Материал по химии
Что такое степень окисления?
Степень окисления – это условная величина, отражающая количество принятых или отданных электронов при образовании заряженной частицы из электронейтрального атома при условии, что электроны переходят от одного атома к другому полностью.
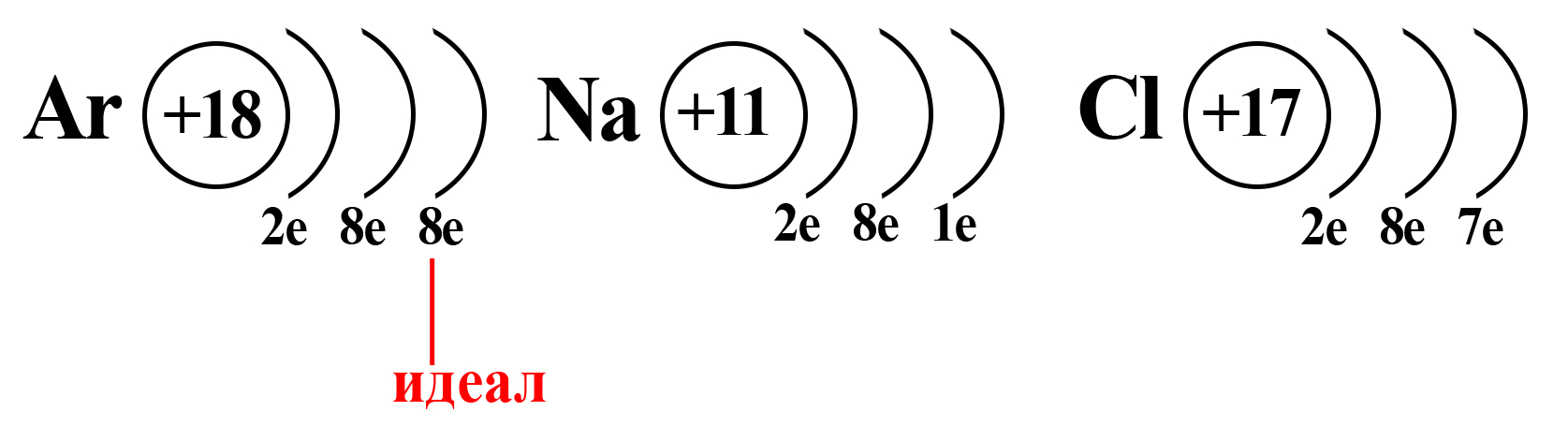
Вспомним, что идеальное количество электронов на внешнем электронном уровне атома равно восьми. Такую конфигурацию внешнего слоя имеют атомы большинства благородных газов (кроме гелия). И к такой электронной конфигурации стремятся атомы других элементов.
Как определить степень окисления
Конфигурация благородного газа
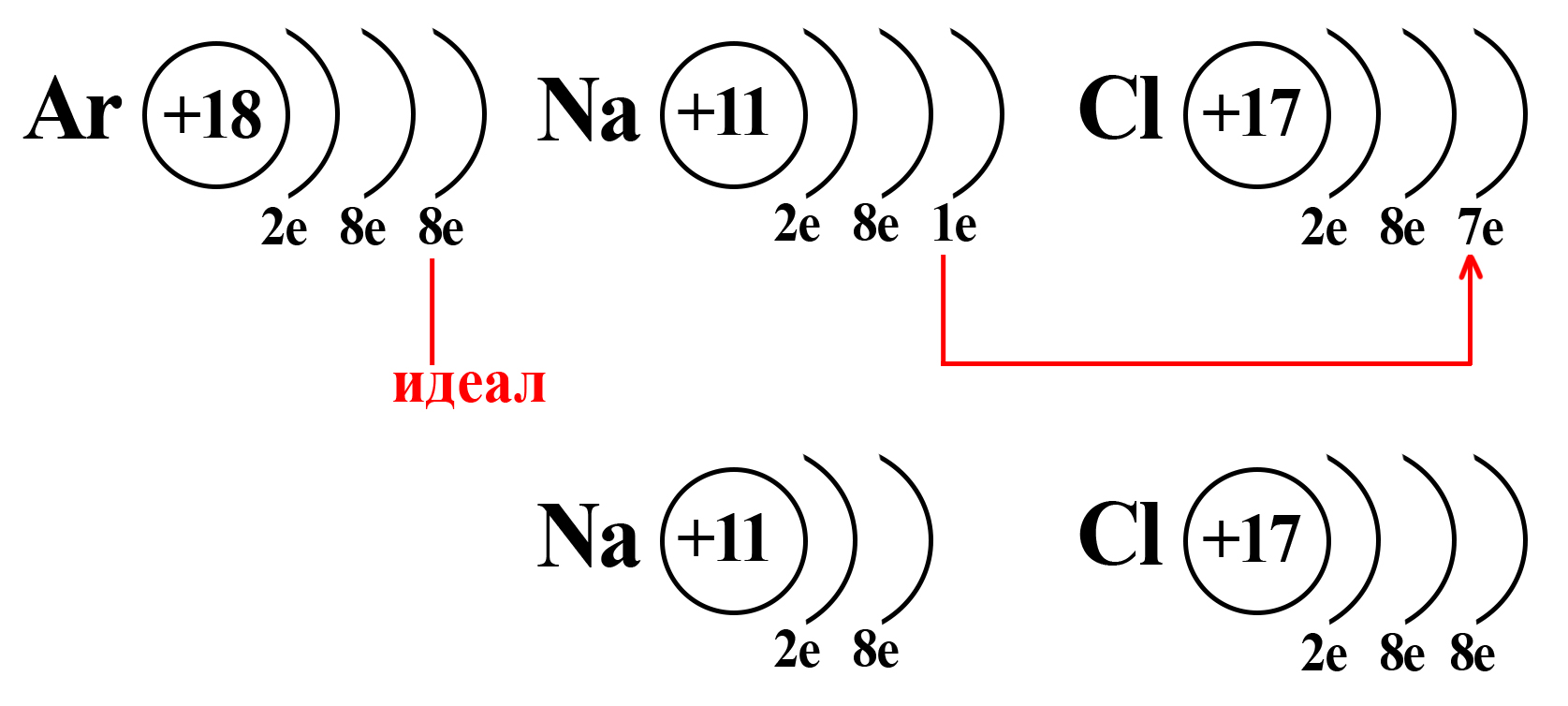
Натрий и хлор не так далеки от «идеала», как может показаться. Если атомы этих элементов столкнуться, внешний электрон натрия притянется на внешний электронный уровень хлора (из-за большей электроотрицательности хлора):
Таким образом, натрий и хлор как будто вступают в симбиоз: натрию, для приобретения «благородной» конфигурации необходимо избавиться от внешнего электрона (при потере внешнего электрона теряется и внешний уровень, а предвнешний уровень, имеющий идеальное количество электронов, становится внешним), тогда как хлору необходимо получить один электрон, чтобы завершить внешний энергетический уровень.
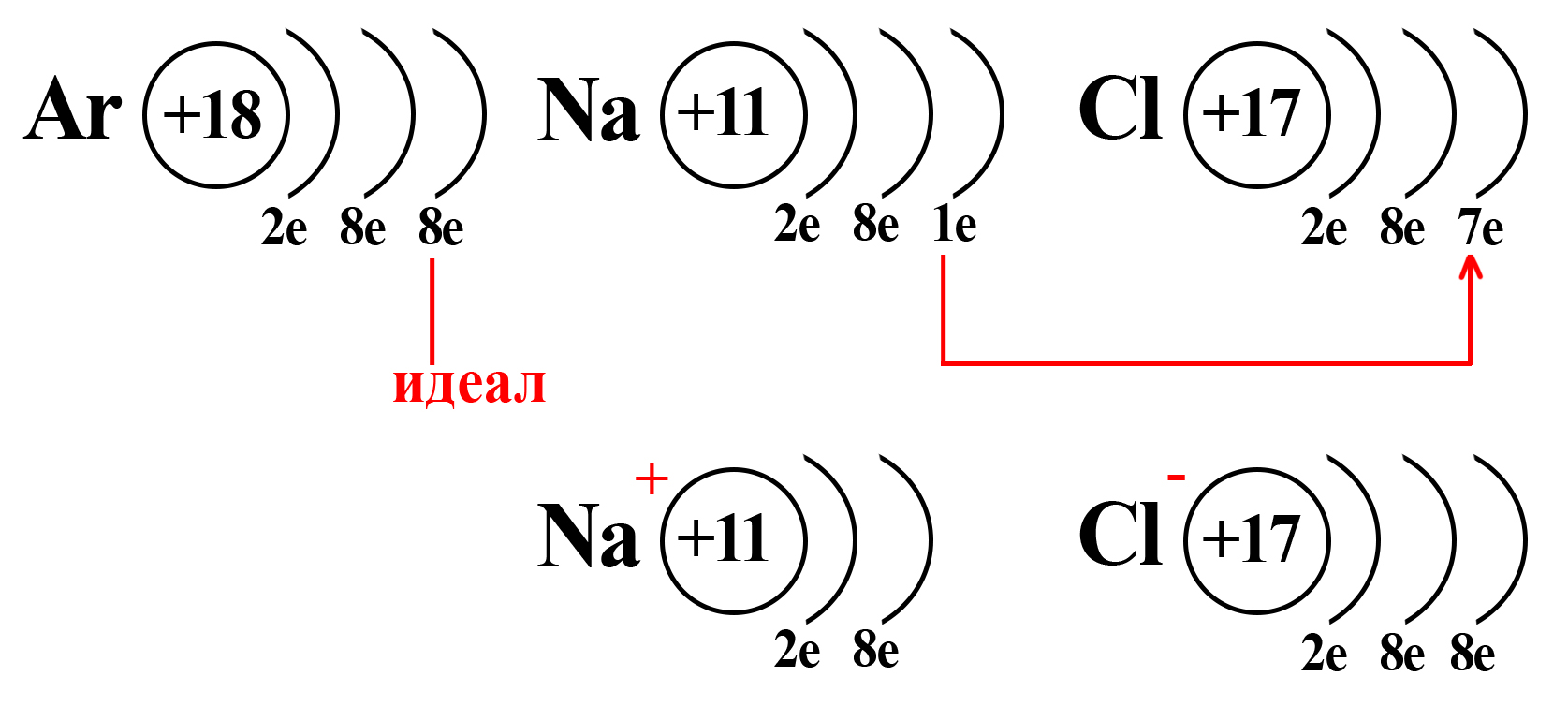
Потеряв один электрон, натрий приобретает положительный заряд, становится катионом (положительно заряженной частицей). Это объясняется тем, что ядро натрия по-прежнему имеет 11 протонов, а вот электронная оболочка, после взаимодействия с хлором, содержит 10 электронов. Таким образом, натрий будет иметь 11 положительно заряженных частиц и 10 отрицательно заряженных частиц. По простейшему уравнению: +11 – 10 = +1, становится ясно, откуда взялся положительный заряд.
Аналогичный расчет можно привести и для хлора. После взаимодействия с натрием ядро атома хлора не изменяется, оно содержит 17 положительно заряженных частиц (протонов), а оболочка – 18 отрицательно заряженных частиц (электронов). +17 – 18 = ‒1.
Полученные заряды и являются степенями окисления.
Также степень окисления можно выразить количеством электронов, которые иону нужно получить или отдать для того, чтобы стать электронейтральным атомом. Так, катион натрия, имеющий заряд «+1», должен получить 1 электрон, чтобы превратиться в атом натрия: Na+ +1ē = Na0. А анион хлора (хлорид-ион), имеющий заряд «‒1» должен отдать один электрон: Cl— -1ē = Cl0.
Для упрощения понятие «степень окисления» применяется не только для веществ с ионным строением (металл + неметалл), но и для веществ с ковалентными полярными связями. Несмотря на то, что в таком типе связи полного перехода электронов от одного атома к другому не происходит, полученные частичные заряды превращаются в целые.
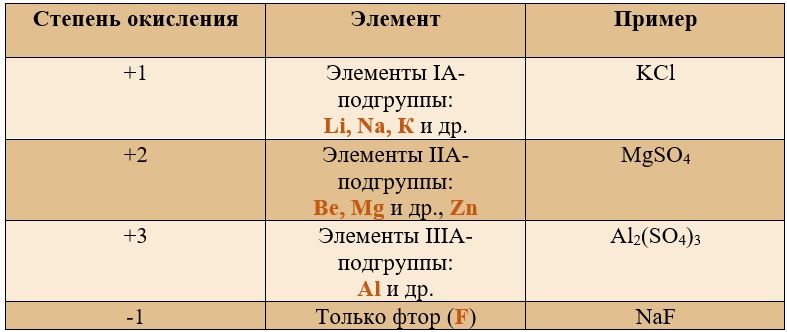
Постоянные степени окисления.
Знания этой простой, базовой темы помогут Вам решать не только тестовые задания. Одно из самых сложных заданий ЕГЭ – расстановка коэффициентов с помощью электронного баланса – не решается без знания степеней окисления.
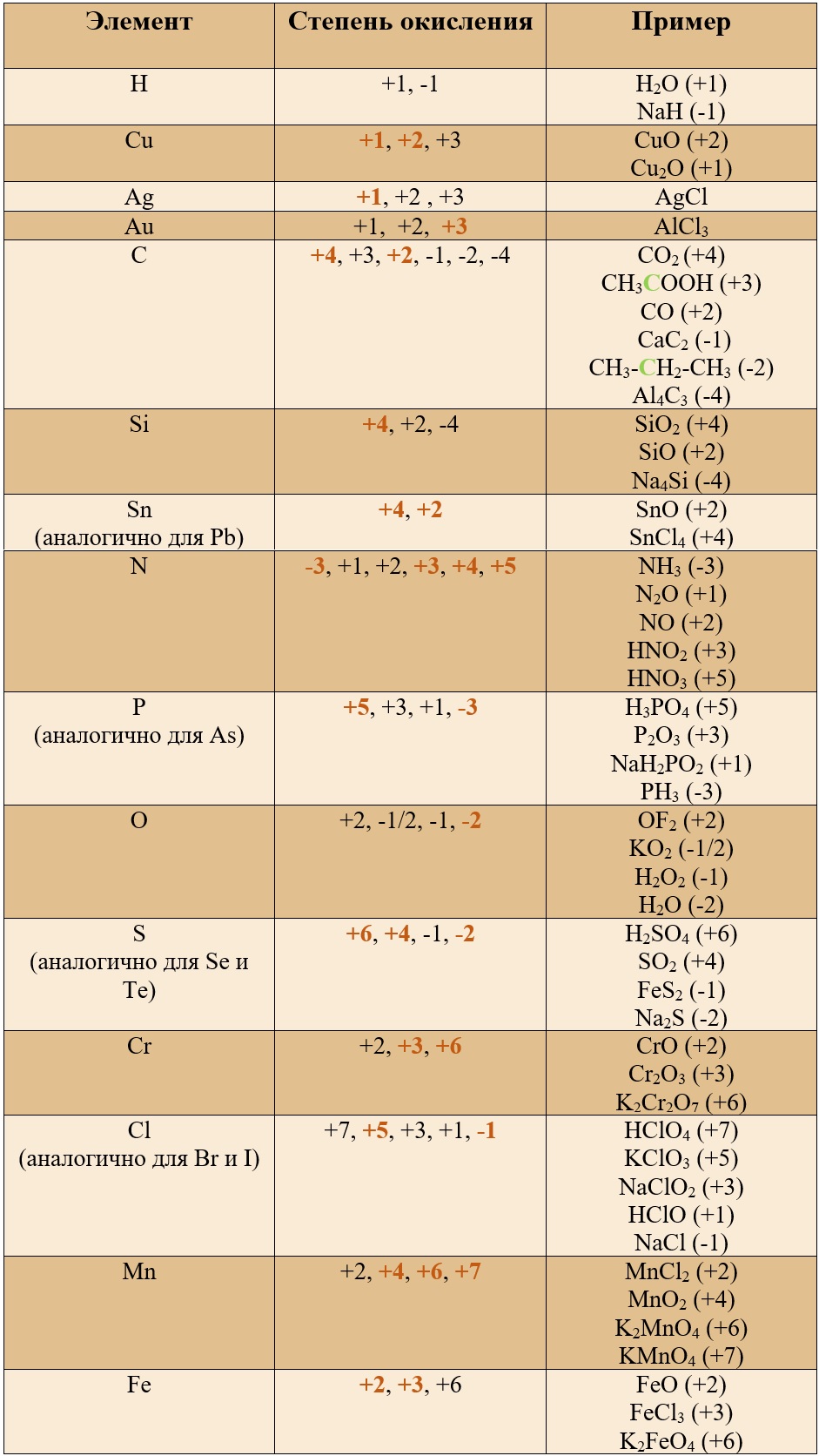
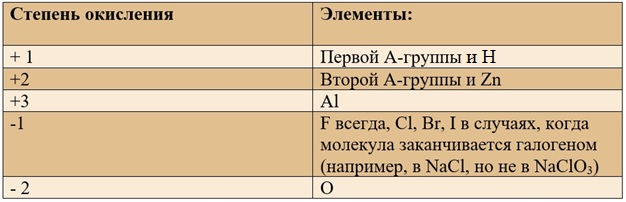
Таблица «Элементы, имеющие постоянную степень окисления»
Таблица «Наиболее популярные степени окисления у остальных элементов» (Выделены бурым)*
*В таблице указаны не все возможные степени окисления.
Таким образом, медь, серебро, золото и железо не проявляют высшей степени окисления, равной номеру группы, у остальных же элементов высшая степень окисления равна номеру группы.
Для определения степени окисления не нужно учить всю таблицу, и тем более все степени окисления. Они приведены для справки, наиболее важными являются:
Определение степеней окисления в бинарных соединениях
Для примера возьмём оксид фосфора (P2O5)
- Определим степень окисления известного элемента (в нашем случае это кислород).
- Условно разделим молекулу на две части: чаще всего первая часть молекулы положительная, а вторая – отрицательная (искл: NH3 и PH3).
- Индекс после кислорода указывает на, что в молекуле содержится пять атомов кислорода, каждый из них имеет степень окисления «-2», поэтому общее количество отрицательных зарядов будет равно «-10».
- Молекула должна быть электронейтральной, то есть количество положительных и отрицательных зарядов должны быть равными. Из этого следует, что все атомы фосфора в данной молекуле в сумме должны иметь десять положительных зарядов.
- Индекс «2» после фосфора означает, что в молекуле содержится два атома фосфора, между которыми поровну нужно разделить общий положительный заряд (+10:2=+5)
Аналогичным образом происходит определение степени окисления в более сложных веществах, для примера возьмём перманганат калия (KMnO4):
- Подпишем степени окисления для элементов, имеющих постоянные их значения:
- Разделим молекулу на положительный и отрицательный «полюс» (в соединениях, состоящих из атомов трех элементов, чаще всего первые два являются положительными, а третий — отрицательным).
- Посчитаем общее количество положительных и отрицательных зарядов с учетом индексов:
- Ответим на вопрос: какого количества плюсов не хватает, что бы положительные и отрицательные заряды имели одинаковое значение? До +8 не хватает семи положительных зарядов, откуда следует, что степень окисления марганца равна «+7».
Ну и напоследок разберем степени окисления элементов в дихромате калия (K2Cr2O7):
- Подписываем известные степени окисления:
- Делим молекулу на положительную и отрицательную части:
- Считаем общее количество «плюсов» и «минусов»:
- Подсчитываем, сколько положительных зарядов не достает для того, чтобы молекула стала электронейтральной (т. е. такой молекулой, в которой количество положительных и отрицательных зарядов было одинаковым):
- Так как молекула содержит два атома хрома, двенадцать положительных зарядов должны распределиться между ними поровну, то есть, каждый хром имеет заряд +6:
Как быть, если в формуле встретились скобки? Например, как посчитать степень окисления брома в пербромате кальция?
- Для начала определим все известные степени окисления, как делали в предыдущих примерах:
- Посчитаем сумму положительных и отрицательных зарядов. Важно учесть все индексы. Помните, что индекс. Расположенный за атомом действует только на этот атом, а индекс, расположенный за скобкой, действует на всё содержимое скобок:
Таким образом, в пербромате кальция содержится: один атом кальция, два атома брома и 8 атомов кислорода (индексы, относящиеся к одному и тому же атому перемножаются).
Следовательно, мы имеем два положительных заряда от кальция и шестнадцать отрицательных от кислорода. Так как индекс «2» за скобками действует и на бром, его заряд можно выразить как 2х.
Получаем уравнение:
2 + 2х ‒ 16 = 0
2х = 14
х = 7
Степень окисления брома в пербромате кальция равна «+7».
Степень окисления кальция.
Степень окисления кальция:
Степень окисления (окислительное число) – это вспомогательная условная величина для записи процессов окисления, восстановления и окислительно-восстановительных реакций. Она указывает на состояние окисления отдельного атома молекулы и представляет собой лишь удобный метод учёта переноса электронов. Однако она не является истинным зарядом атома в молекуле.
Степень окисления соответствует числу электронов, которое следует присоединить к положительному иону (катиону), чтобы восстановить его до нейтрального атома, или отнять от отрицательного иона (аниона), чтобы окислить его до нейтрального атома.
Степень окисления (в отличие от валентности) может иметь нулевое, отрицательное и положительное значения.
Значения степени окисления записывают арабскими цифрами сверху над символом элемента. При указании степени окисления первым ставится знак, а потом численное значение, а не наоборот.
Степень окисления (в отличие от валентности) может иметь нулевое, отрицательное и положительное значения: -5, -4, -3, -2, -1, 0, +1, +2 , +3 , +4, +5, +6 , +7.
Следует помнить, что степень окисления является сугубо условной величиной, не имеющей физического смысла, но характеризующей образование химической связи межатомного взаимодействия в молекуле.
Степень окисления в ряде случаев не совпадает с валентностью. Например, в молекуле азотной кислоты степень окисления центрального атома азота равна +5, тогда как валентность равна IV.
Степень окисления зачастую не совпадает с фактическим числом электронов, которые участвуют в образовании связей.
Степень окисления кальция равна 0, +2.
| Степень окисления кальция в соединениях | |
| 0 | Ca |
| +2 | CaCl2, CaH2, CaO, Ca(OH)2 |
Все свойства атома кальция
Источник: https://ru.wikipedia.org
Примечание: © Фото https://www.pexels.com, https://pixabay.com
Коэффициент востребованности
415
Степень окисления — это условный заряд атома химического элемента в веществе.
Правила:
1. Степень окисления элемента в простом веществе равна (0):
,
O20
,
N20
,
F20
,
Cl20
,
Fe0
,
Ca0
.
2. В сложных веществах:
- степень окисления водорода в соединениях с неметаллами равна (+1), а в соединениях с металлами — (–1):
- степень окисления кислорода равна (–2) (исключения: O+2F−12, H+12O−12):
- степень окисления фтора всегда равна (–1):
- степень окисления металла — положительная и совпадает с его валентностью. Может быть постоянной и переменной:
,
K+1
,
Ca+2
,
Mg+2
,
Al+3
;
- степень окисления неметалла может быть как положительная, так и отрицательная. Численные значения тоже совпадают с валентностью:
,
N+4
,
N+3
,
N+2
,
N+1
,
N−3
;
3. Сумма степеней окисления элементов в веществе равна (0).
Пример:
.
Составление формул по известным степеням окисления элементов
Пример:
составим формулу соединения кальция и азота. Степень окисления кальция равна (+2), а азота — (–3).
Запишем символы химических элементов рядом. Первым обычно записывают символ элемента, у которого степень окисления положительная. Укажем значения степеней окисления над символами:
Найдём для них наименьшее общее кратное и разделим на соответствующие значения степеней окисления. Получим индексы в формуле:
| Элемент | Название | Степень окисления |
|
7N |
Азот (степень окисления) |
-III, 0, +I, II, III, IV, V |
|
89Ас |
Актиний (степень окисления) |
0, + III |
|
13Al |
Алюминий (степень окисления) |
0, +III |
|
95Am |
Америций (степень окисления) |
0, + II , III, IV |
|
18Ar |
Аргон (степень окисления) |
0 |
|
85At |
Астат (степень окисления) |
-I, 0, +I, V |
|
56Ba |
Барий (степень окисления) |
0, +II |
|
4Be |
Бериллий (степень окисления) |
0,+ IV |
|
97Bk |
Берклий (степень окисления) |
0, +III, IV |
|
5B |
Бор (степень окисления) |
-III, 0, +III |
|
107Bh |
Борий (степень окисления) |
0, +VII |
|
35Br |
Бром (степень окисления) |
-I, 0, +I, V, VII |
|
23V |
Ванадий (степень окисления) |
0, + II , III, IV, V |
|
83Bi |
Висмут (степень окисления) |
0, +III, V |
|
1H |
Водород (степень окисления) |
-I, 0, +I |
|
74W |
Вольфрам (степень окисления) |
0, +IV, VI |
|
64Gd |
Гадолиний (степень окисления) |
0, +III |
| Элемент | Название | Степень окисления |
|
31Ga |
Галлий (степень окисления) |
0, +III |
|
72Hf |
Гафний (степень окисления) |
0,+IV |
|
2He |
Гелий (степень окисления) |
0 |
|
32Ge |
Германий (степень окисления) |
0, +II, IV |
|
67Ho |
Гольмий (степень окисления) |
0, + III |
|
66Dy |
Диспрозий (степень окисления) |
0, + III |
|
105Db |
Дубний (степень окисления) |
0, +V |
|
63Еu |
Европий (степень окисления) |
0, +II, III |
|
26Fe |
Железо (степень окисления) |
0, +II, III, VI |
|
79Au |
Золото (степень окисления) |
0, + I , III |
|
49In |
Индий (степень окисления) |
0 , + III |
|
77Ir |
Иридий (степень окисления) |
0, +III, IV |
|
39Y |
Иттрий (степень окисления) |
0, +III |
|
70Yb |
Иттербий (степень окисления) |
0, + II , III |
|
53I |
Йод (степень окисления) |
-I, 0, +I, V, VII |
|
48Cd |
Кадмий (степень окисления) |
0, + II |
|
19К |
Калий (степень окисления) |
0, +I |
|
98Cf |
Калифорний (степень окисления) |
0, +Ш, IV |
| Элемент | Название | Степень окисления |
|
20Ca |
Кальций (степень окисления) |
0, + II |
|
54Xe |
Ксенон (степень окисления) |
0, + II , IV, VI, VIII |
|
8O |
Кислород (степень окисления) |
-II, I, 0, +II |
|
27Co |
Кобальт (степень окисления) |
0, +II, III |
|
36Кr |
Криптон (степень окисления) |
0, + II |
|
14Si |
Кремний (степень окисления) |
-IV, 0, +11, IV |
|
96Cm |
Кюрий (степень окисления) |
0, +III, IV |
|
57La |
Лантан (степень окисления) |
0, +III |
|
3Li |
Литий (степень окисления) |
0, +I |
|
103Lr |
Лоуренсий (степень окисления) |
0, +III |
|
71Lu |
Лютеций (степень окисления) |
0, +III |
|
12Mg |
Магний (степень окисления) |
0, + II |
|
25Mn |
Марганец (степень окисления) |
0, +II, IV, VI, VIII |
|
29Cu |
Медь (степень окисления) |
0, +I, -II |
|
109Mt |
Мейтнерий (степень окисления) |
0, +IV? |
|
101Md |
Менделевий (степень окисления) |
0, +II, III |
|
42Mo |
Молибден (степень окисления) |
0 , +IV, VI |
|
33As |
Мышьяк (степень окисления) |
— III , 0 , +III, V |
|
11Na |
Натрий (степень окисления) |
0, +I |
| Элемент | Название | Степень окисления |
|
60Nd |
Неодим (степень окисления) |
0, +III |
|
10Ne |
Неон (степень окисления) |
0 |
|
93Np |
Нептуний (степень окисления) |
0, +III, IV, VI, VII |
|
28Ni |
Никель (степень окисления) |
0, +II, III |
|
41Nb |
Ниобий (степень окисления) |
0, +IV, V |
|
102No |
Нобелий (степень окисления) |
0, +II, III |
|
50Sn |
Олово (степень окисления) |
0, + II , IV |
|
76Os |
Осмий (степень окисления) |
0, +IV, VI, VIII |
|
46Pd |
Палладий (степень окисления) |
0, +II, IV |
|
91Pa. |
Протактиний (степень окисления) |
0, +IV, V |
|
61Pm |
Прометий (степень окисления) |
0, + III |
|
84Рo |
Полоний (степень окисления) |
0, +II, IV |
|
59Рг |
Празеодим (степень окисления) |
0, +III, IV |
|
78Pt |
Платина (степень окисления) |
0, +II, IV |
|
94PU |
Плутоний (степень окисления) |
0, +III, IV, V, VI |
|
88Ra |
Радий (степень окисления) |
0, + II |
|
37Rb |
Рубидий (степень окисления) |
0, +I |
|
75Re |
Рений (степень окисления) |
0, +IV, VII |
|
104Rf |
Резерфордий (степень окисления) |
0, +IV |
| Элемент | Название | Степень окисления |
|
45Rh |
Родий (степень окисления) |
0, +III, IV |
|
86Rn |
Радон (степень окисления) |
0, + II , IV, VI, VIII |
|
44Ru |
Рутений (степень окисления) |
0, +II, IV, VI, VIII |
|
80Hg |
Ртуть (степень окисления) |
0 , +I, II, IV |
|
16S |
Сера (степень окисления) |
-II, 0, +IV, VI |
|
47Ag |
Серебро (степень окисления) |
0, +I |
|
51Sb |
Сурьма (степень окисления) |
0, +III, V |
|
21Sc |
Скандий (степень окисления) |
0, +III |
|
34Se |
Селен (степень окисления) |
-II, 0,+IV, VI |
|
106Sg |
Сиборгий (степень окисления) |
0, +VI |
|
62Sm |
Самарий (степень окисления) |
0, + II , III |
|
38Sr |
Стронций (степень окисления) |
0, + II |
|
82РЬ |
Свинец (степень окисления) |
0, +II, IV |
|
81Тl |
Таллий (степень окисления) |
0, + I , II |
|
73Ta |
Тантал (степень окисления) |
0, +IV, V |
|
52Te |
Теллур (степень окисления) |
-II, 0, +IV, VI |
|
65Tb |
Тербий (степень окисления) |
0, +III, IV |
|
43Tc |
Технеций (степень окисления) |
0, +IV, VII |
|
22Ti |
Титан (степень окисления) |
0, + II , III, IV |
| Элемент | Название | Степень окисления |
|
90Th |
Торий (степень окисления) |
0, +IV |
|
69Tm |
Тулий (степень окисления) |
0 , +III |
|
6C |
Углерод (степень окисления) |
-IV, I, 0, +II, IV |
|
92U |
Уран (степень окисления) |
0, +III, IV, VI |
|
100Fm |
Фермий (степень окисления) |
0, +II, III |
|
15P |
Фосфор (степень окисления) |
-III, 0, +I, III, V |
|
87Fr |
Франций (степень окисления) |
0, +I |
|
9F |
Фтор (степень окисления) |
-I, 0 |
|
108Hs |
Хассий (степень окисления) |
0, +VIII |
|
17Cl |
Хлор (степень окисления) |
-I, 0, +I, III, IV, V, VI, VII |
|
24Cr |
Хром (степень окисления) |
0, + II , III , VI |
|
55Cs |
Цезий (степень окисления) |
0, +I |
|
58Ce |
Церий (степень окисления) |
0, + III , IV |
|
30Zn |
Цинк (степень окисления) |
0, + II |
|
40Zr |
Цирконий (степень окисления) |
0, +IV |
|
99ES |
Эйнштейний (степень окисления) |
0, +II, III |
|
68Еr |
Эрбий (степень окисления) |
0, +III |
| Элемент | Название | Степень окисления |
|
1H |
Водород (степень окисления) |
-I, 0, +I |
|
2He |
Гелий (степень окисления) |
0 |
|
3Li |
Литий (степень окисления) |
0, +I |
|
4Be |
Бериллий (степень окисления) |
0,+ IV |
|
5B |
Бор (степень окисления) |
-III, 0, +III |
|
6C |
Углерод (степень окисления) |
-IV, I, 0, +II, IV |
|
7N |
Азот (степень окисления) |
-III, 0, +I, II, III, IV, V |
|
8O |
Кислород (степень окисления) |
-II, I, 0, +II |
|
9F |
Фтор (степень окисления) |
-I, 0 |
|
10Ne |
Неон (степень окисления) |
0 |
|
11Na |
Натрий (степень окисления) |
0, +I |
|
12Mg |
Магний (степень окисления) |
0, + II |
|
13Al |
Алюминий (степень окисления) |
0, +III |
|
14Si |
Кремний (степень окисления) |
-IV, 0, +II, IV |
|
15P |
Фосфор (степень окисления) |
-III, 0, +I, III, V |
|
16S |
Сера (степень окисления) |
-II, 0, +IV, VI |
|
17Cl |
Хлор (степень окисления) |
-I, 0, +I, III, IV, V, VI, VII |
| Элемент | Название | Степень окисления |
|
18Ar |
Аргон (степень окисления) |
0 |
|
19К |
Калий (степень окисления) |
0, +I |
|
20Ca |
Кальций (степень окисления) |
0, + II |
|
21Sc |
Скандий (степень окисления) |
0, +III |
|
22Ti |
Титан (степень окисления) |
0, + II , III, IV |
|
23V |
Ванадий (степень окисления) |
0, + II , III, IV, V |
|
24Cr |
Хром (степень окисления) |
0, + II , III , VI |
|
25Mn |
Марганец (степень окисления) |
0, +II, IV, VI, VIII |
|
26Fe |
Железо (степень окисления) |
0, +II, III, VI |
|
27Co |
Кобальт (степень окисления) |
0, +II, III |
|
28Ni |
Никель (степень окисления) |
0, +II, III |
|
29Cu |
Медь (степень окисления) |
0, +I, -II |
|
30Zn |
Цинк (степень окисления) |
0, + II |
|
31Ga |
Галлий (степень окисления) |
0, +III |
|
32Ge |
Германий (степень окисления) |
0, +II, IV |
|
33As |
Мышьяк (степень окисления) |
— III , 0 , +III, V |
|
34Se |
Селен (степень окисления) |
-II, 0,+IV, VI |
|
35Br |
Бром (степень окисления) |
-I, 0, +I, V, VII |
| Элемент | Название | Степень окисления |
|
36Кr |
Криптон (степень окисления) |
0, + II |
|
37Rb |
Рубидий (степень окисления) |
0, +I |
|
38Sr |
Стронций (степень окисления) |
0, + II |
|
39Y |
Иттрий (степень окисления) |
0, +III |
|
40Zr |
Цирконий (степень окисления) |
0, +IV |
|
41Nb |
Ниобий (степень окисления) |
0, +IV, V |
|
42Mo |
Молибден (степень окисления) |
0 , +IV, VI |
|
43Tc |
Технеций (степень окисления) |
0, +IV, VII |
|
44Ru |
Рутений (степень окисления) |
0, +II, IV, VI, VIII |
|
45Rh |
Родий (степень окисления) |
0, +III, IV |
|
46Pd |
Палладий (степень окисления) |
0, +II, IV |
|
47Ag |
Серебро (степень окисления) |
0, +I |
|
48Cd |
Кадмий (степень окисления) |
0, + II |
|
49In |
Индий (степень окисления) |
0 , + III |
|
50Sn |
Олово (степень окисления) |
0, + II , IV |
|
51Sb |
Сурьма (степень окисления) |
0, +III, V |
|
52Te |
Теллур (степень окисления) |
-II, 0, +IV, VI |
|
53I |
Йод (степень окисления) |
-I, 0, +I, V, VII |
|
54Xe |
Ксенон (степень окисления) |
0, + II , IV, VI, VIII |
| Элемент | Название | Степень окисления |
|
55Cs |
Цезий (степень окисления) |
0, +I |
|
56Ba |
Барий (степень окисления) |
0, +II |
|
57La |
Лантан (степень окисления) |
0, +III |
|
58Ce |
Церий (степень окисления) |
0, + III , IV |
|
59Рг |
Празеодим (степень окисления) |
0, +III, IV |
|
60Nd |
Неодим (степень окисления) |
0, +III |
|
61Pm |
Прометий (степень окисления) |
0, + III |
|
62Sm |
Самарий (степень окисления) |
0, + II , III |
|
63Еu |
Европий (степень окисления) |
0, +II, III |
|
64Gd |
Гадолиний (степень окисления) |
0, +III |
|
65Tb |
Тербий (степень окисления) |
0, +III, IV |
|
66Dy |
Диспрозий (степень окисления) |
0, + III |
|
67Ho |
Гольмий (степень окисления) |
0, + III |
|
68Еr |
Эрбий (степень окисления) |
0, +III |
|
69Tm |
Тулий (степень окисления) |
0 , +III |
|
70Yb |
Иттербий (степень окисления) |
0, + II , III |
|
71Lu |
Лютеций (степень окисления) |
0, +III |
|
72Hf |
Гафний (степень окисления) |
0,+IV |
|
73Ta |
Тантал (степень окисления) |
0, +IV, V |
| Элемент | Название | Степень окисления |
|
74W |
Вольфрам (степень окисления) |
0, +IV, VI |
|
75Re |
Рений (степень окисления) |
0, +IV, VII |
|
76Os |
Осмий (степень окисления) |
0, +IV, VI, VIII |
|
77Ir |
Иридий (степень окисления) |
0, +III, IV |
|
78Pt |
Платина (степень окисления) |
0, +II, IV |
|
79Au |
Золото (степень окисления) |
0, + I , III |
|
80Hg |
Ртуть (степень окисления) |
0 , +I, II, IV |
|
81Тl |
Таллий (степень окисления) |
0, + I , II |
|
82РЬ |
Свинец (степень окисления) |
0, +II, IV |
|
83Bi |
Висмут (степень окисления) |
0, +III, V |
|
84Рo |
Полоний (степень окисления) |
0, +II, IV |
|
85At |
Астат (степень окисления) |
-I, 0, +I, V |
|
86Rn |
Радон (степень окисления) |
0, + II , IV, VI, VIII |
|
87Fr |
Франций (степень окисления) |
0, +I |
|
88Ra |
Радий (степень окисления) |
0, + II |
|
89Ас |
Актиний (степень окисления) |
0, + III |
|
90Th |
Торий (степень окисления) |
0, +IV |
|
91Pa. |
Протактиний (степень окисления) |
0, +IV, V |
|
92U |
Уран (степень окисления) |
0, +III, IV, VI |
| Элемент | Название | Степень окисления |
|
93Np |
Нептуний (степень окисления) |
0, +III, IV, VI, VII |
|
94PU |
Плутоний (степень окисления) |
0, +III, IV, V, VI |
|
95Am |
Америций (степень окисления) |
0, + II , III, IV |
|
96Cm |
Кюрий (степень окисления) |
0, +III, IV |
|
97Bk |
Берклий (степень окисления) |
0, +III, IV |
|
98Cf |
Калифорний (степень окисления) |
0, +Ш, IV |
|
99ES |
Эйнштейний (степень окисления) |
0, +II, III |
|
100Fm |
Фермий (степень окисления) |
0, +II, III |
|
101Md |
Менделевий (степень окисления) |
0, +II, III |
|
102No |
Нобелий (степень окисления) |
0, +II, III |
|
103Lr |
Лоуренсий (степень окисления) |
0, +III |
|
104Rf |
Резерфордий (степень окисления) |
0, +IV |
|
105Db |
Дубний (степень окисления) |
0, +V |
|
106Sg |
Сиборгий (степень окисления) |
0, +VI |
|
107Bh |
Борий (степень окисления) |
0, +VII |
|
108Hs |
Хассий (степень окисления) |
0, +VIII |
|
109Mt |
Мейтнерий (степень окисления) |
0, +IV? |