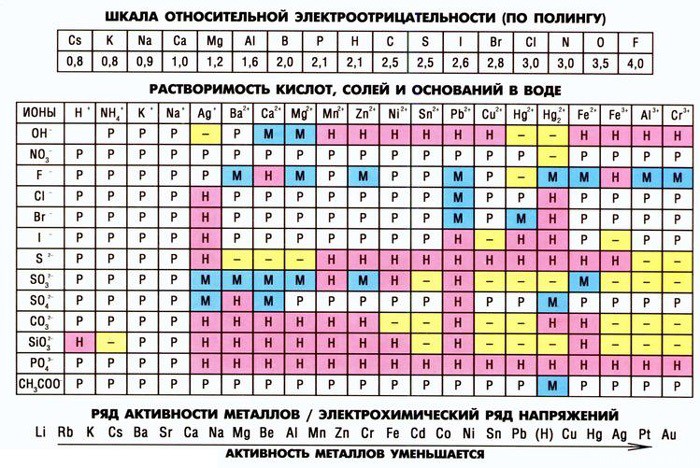
«Говорящие» кислотные остатки
24-Окт-2012 | комментария 4 | Лолита Окольнова
«Говорящие» кислотные остатки
Когда я начинаю занятия по химии и рассказываю о Периодической системе элементов, то всегда говорю, что это как ключ от всех дверей. В ней можно найти ответ на практически любой вопрос по химии.
Таблица растворимости тоже в этом плане очень информативна. Здесь можно найти не только соли и узнать растворимы они или нет. Здесь есть еще один маленький секрет, который может оказаться очень полезным…
Давайте сегодня подробно рассмотрим левый столбец — столбик Анионов, или Кислотных остатков.
Во-первых, я считаю абсолютно необходимым знать названия и заряды кислотных остатков. В принципе, их можно легко вывести, но на экзамене у вас просто не хватит на это времени. Спорить с этим бесполезно. Это факт.
Поэтому, выучиваем:
OH(-) — гидроксид;
NO3(-) — нитрат;
F(-) — фторид;
Cl(-) -хлорид;
Br(-) — бромид;
J(-) — йодид;
S(-2) — сульфид;
SO3(-2) — сульфит;
SO4(-2) — сульфат;
CO3(-2) — карбонат;
SiO3(-2) — силикат;
PO4(-3) — фосфат;
CH3COO(-) — ацетат.
Во-вторых, обратите внимание, что все названия кислотных остатков имеют различие в окончаниях: —ид, -ит и -ат.
Окончания эти говорят о многом:
- -ид (кроме -OH): фторид F(-), хлорид Cl(-), бромид Br(-), йодид J(-), cульфид (-2):
- кислотный остаток состоит из одного элемента;
- этот элемент находится в минимальной степени окисления ( = № группы-8);
Поэтому даже если какого-то кислотного остатка нет в табличке, но у него окончание -ид, мы можем легко написать его формулу.
Например, нитрид алюминия: нитрид, значит, состоит из одного элемента — N, степень окисления минимальная=-3, значит, формула будет AlN.
- —ит: cульфит SO3(-2):
- кислотный остаток состоит из элемента и кислорода;
- элемент находится в средней степени окисления (в данном примере у серы S степень окисления +4)
Например, кислотного остатка нитрита в нашей таблице нет, но окончание -ит, значит это азот и кислород NO, промежуточная степень окисления азота= +3, кислотный оксид будет N2O3, прибавим воду: N2O3 + H2O = 2HNO2, значит, кислотный остаток — NO2(-).
- -ат: сульфат SO4(-2), карбонат CO3(-2), силикат SiO3(-2), фосфат PO4(-3), ацетат CH3COO(-):
- кислотный остаток состоит из элемента и кислорода;
- этот элемент находится в максимальной степени окисления ( = № группы);
Например, кислотный остаток хлорат. Два элемента ClO. Максимальная степень окисления хлора Cl= +5. Кислотный оксид будет иметь вид Cl2O5. Кислота: Cl2O5 + H2O = 2HClO3. Кислотный остаток — ClO3(-).
Как видите, все можно вывести, но стоит ли тратить на это время? Но, бывает, что в заданиях попадаются кислотные остатки, которых нет в таблице растворимости или просто вы их не знаете. Что делать тогда? Выводить их формулу по указанной логике.
Кислотные остатки тоже оказались «говорящими»!
Обсуждение: ««Говорящие» кислотные остатки»
(Правила комментирования)
Темы кодификатора ЕГЭ: Электроотрицательность. Степень окисления и валентность химических элементов.
Когда атомы взаимодействуют и образуют химическую связь, электроны между ними в большинстве случаев распределяются неравномерно, поскольку свойства атомов различаются. Более электроотрицательный атом сильнее притягивает к себе электронную плотность. Атом, который притянул к себе электронную плотность, приобретает частичный отрицательный заряд δ—, его «партнер» — частичный положительный заряд δ+. Если разность электроотрицательностей атомов, образующих связь, не превышает 1,7, мы называем связь ковалентной полярной. Если разность электроотрицательностей, образующих химическую связь, превышает 1,7, то такую связь мы называем ионной.
Степень окисления – это вспомогательный условный заряд атома элемента в соединении, вычисленный из предположения, что все соединения состоят из ионов (все полярные связи – ионные).
Что значит «условный заряд»? Мы просто-напросто договариваемся, что немного упростим ситуацию: будем считать любые полярные связи полностью ионными, и будем считать, что электрон полностью уходит или приходит от одного атома к другому, даже если на самом деле это не так. А уходит условно электрон от менее электроотрицательного атома к более электроотрицательному.
Например, в связи H-Cl мы считаем, что водород условно «отдал» электрон, и его заряд стал +1, а хлор «принял» электрон, и его заряд стал -1. На самом деле таких полных зарядов на этих атомах нет.
Наверняка, у вас возник вопрос — зачем же придумывать то, чего нет? Это не коварный замысел химиков, все просто: такая модель очень удобна. Представления о степени окисления элементов полезны при составлении классификации химических веществ, описании их свойств, составлении формул соединений и номенклатуры. Особенно часто степени окисления используются при работе с окислительно-восстановительными реакциями.
Степени окисления бывают высшие, низшие и промежуточные.
Высшая степень окисления равна номеру группы со знаком «плюс».
Низшая определяется, как номер группы минус 8.
И промежуточная степень окисления — это почти любое целое число в интервале от низшей степени окисления до высшей.
Например, для азота характерны: высшая степень окисления +5, низшая 5 — 8 = -3, а промежуточные степени окисления от -3 до +5. Например, в гидразине N2H4 степень окисления азота промежуточная, -2.
Чаще всего степень окисления атомов в сложных веществах обозначается сначала знаком, потом цифрой, например +1, +2, -2 и т.д. Когда речь идет о заряде иона (предположим, что ион реально существует в соединении), то сначала указывают цифру, потом знак. Например: Ca2+, CO3 2-.
Для нахождения степеней окисления используют следующие правила:
- Степень окисления атомов в простых веществах равна нулю;
- В нейтральных молекулах алгебраическая сумма степеней окисления равна нулю, для ионов эта сумма равна заряду иона;
- Степень окисления щелочных металлов (элементы I группы главной подгруппы) в соединениях равна +1, степень окисления щелочноземельных металлов (элементы II группы главной подгруппы) в соединениях равна +2; степень окисления алюминия в соединениях равна +3;
- Степень окисления водорода в соединениях с металлами (солеобразные гидриды — NaH, CaH2 и др.) равна -1; в соединениях с неметаллами (летучие водородные соединения) +1;
- Степень окисления кислорода равна -2. Исключение составляют пероксиды – соединения, содержащие группу –О-О-, где степень окисления кислорода равна -1, и некоторые другие соединения (супероксиды, озониды, фториды кислорода OF2 и др.);
- Степень окисления фтора во всех сложных веществах равна -1.
Выше перечислены ситуации, когда степень окисления мы считаем постоянной. У всех остальных химических элементов степень окисления — переменная, и зависит от порядка и типа атомов в соединении.
Примеры:
Задание: определите степени окисления элементов в молекуле дихромата калия: K2Cr2O7.
Решение: степень окисления калия равна +1, степень окисления хрома обозначим, как х, степень окисления кислорода -2. Сумма всех степеней окисления всех атомов в молекуле равна 0. Получаем уравнение: +1*2+2*х-2*7=0. Решаем его, получаем степень окисления хрома +6.
В бинарных соединениях более электроотрицательный элемент характеризуется отрицательной степенью окисления, менее электроотрицательный – положительной.
Обратите внимание, что понятие степени окисления – очень условно! Степень окисления не показывает реальный заряд атома и не имеет реального физического смысла. Это упрощенная модель, которая эффективно работает, когда нам необходимо, например, уравнять коэффициенты в уравнении химической реакции, или для алгоритмизации классификации веществ.
Степень окисления – это не валентность! Степень окисления и валентность во многих случаях не совпадают. Например, валентность водорода в простом веществе Н2 равна I, а степень окисления, согласно правилу 1, равна 0.
Это базовые правила, которые помогут Вам определить степень окисления атомов в соединениях в большинстве случаев.
В некоторых ситуациях вы можете столкнуться с трудностями при определении степени окисления атома. Рассмотрим некоторые из этих ситуаций, и разберем способы их разрешения:
- В двойных (солеобразных) оксидах степень у атома, как правило, две степени окисления. Например, в железной окалине Fe3O4 у железа две степени окисления: +2 и +3. Какую из них указывать? Обе. Для упрощения можно представить это соединение, как соль: Fe(FeO2)2. При этом кислотный остаток образует атом со степенью окисления +3. Либо двойной оксид можно представить так: FeO*Fe2O3.
- В пероксосоединениях степень окисления атомов кислорода, соединенных ковалентными неполярными связями, как правило, изменяется. Например, в пероксиде водорода Н2О2, и пероксидах щелочных металлов степень окисления кислорода -1, т.к. одна из связей – ковалентная неполярная (Н-О-О-Н). Другой пример – пероксомоносерная кислота (кислота Каро) H2SO5 (см. рис.) содержит в составе два атома кислорода со степенью окисления -1, остальные атомы со степенью окисления -2, поэтому более понятной будет такая запись: H2SO3(O2). Известны также пероксосоединения хрома – например, пероксид хрома (VI) CrO(O2)2 или CrO5, и многие другие.
- Еще один пример соединений с неоднозначной степенью окисления – супероксиды (NaO2) и солеобразные озониды KO3. В этом случае уместнее говорить о молекулярном ионе O2 с зарядом -1 и и O3 с зарядом -1. Строение таких частиц описывается некоторыми моделями, которые в российской учебной программе проходят на первых курсах химических ВУЗов: МО ЛКАО, метод наложения валентных схем и др.
- В органических соединениях понятие степени окисления не очень удобно использовать, т.к. между атомами углерода существует большое число ковалентных неполярных связей. Тем не менее, если нарисовать структурную формулу молекулы, то степень окисления каждого атома также можно определить по типу и количеству атомов, с которыми данный атом непосредственно связан. Например, у первичных атомов углерода в углеводородах степень окисления равна -3, у вторичных -2, у третичных атомов -1, у четвертичных — 0.
Потренируемся определять степень окисления атомов в органических соединениях. Для этого необходимо нарисовать полную структурную формулу атома, и выделить атом углерода с его ближайшим окружением — атомами, с которыми он непосредственно соединен.
Полезные советы:
- Для упрощения расчетов можно использовать таблицу растворимости – там указаны заряды наиболее распространенных ионов. На большинстве российских экзаменов по химии (ЕГЭ, ГИА, ДВИ) использование таблицы растворимости разрешено. Это готовая шпаргалка, которая во многих случаях позволяет значительно сэкономить время.
- При расчете степени окисления элементов в сложных веществах сначала указываем степени окисления элементов, которые мы точно знаем (элементы с постоянной степенью окисления), а степень окисления элементов с переменной степенью окисления обозначаем, как х. Сумма всех зарядов всех частиц равна нулю в молекуле или равна заряду иона в ионе. Из этих данных легко составить и решить уравнение.
Тренировочный тест по теме «Степени окисления и валентность» 10 вопросов, при каждом прохождении новые.
244
Создан на
07 января, 2022 От Admin
Тренировочный тест «Степени окисления»
1 / 10
1) Al 2) S 3) Ca 4) N 5) Na
Из указанных в ряду химических элементов выберите два элемента, которые в составе образованных ими оксидов с общей формулой ЭО2 могут иметь одинаковую степень окисления.
Запишите в поле ответа номера выбранных элементов.
2 / 10
1) Al 2) S 3) Cr 4) P 5) Si
Из числа указанных в ряду элементов выберите два элемента, степень окисления которых в высших оксидах равна +6.
3 / 10
1) S 2) Na 3) Al 4) Si 5) Mg
Из числа указанных в ряду элементов выберите два элемента, которые в соединении с кислородом проявляют степень окисления +4.
4 / 10
1) Cr 2) P 3) Na 4) Si 5) N
Из указанных в ряду элементов выберите два элемента, которые не проявляют отрицательной степени окисления.
5 / 10
1) Fe 2) Mg 3) S 4) P 5) Cu
Из указанных в ряду элементов выберите два элемента, которые в соединениях проявляют степень окисления +6.
6 / 10
1) Fe 2) Mg 3) S 4) P 5) Cu
Из указанных в ряду элементов выберите два элемента, степень окисления которых в соединениях может принимать отрицательное значение.
7 / 10
1) Mn 2) B 3) F 4) Cl 5) N
Из указанных в ряду элементов выберите два элемента, которые в соединениях могут проявляют степень окисления +7.
8 / 10
1) Mn 2) B 3) F 4) Cl 5) N
Из указанных в ряду элементов выберите два элемента, которые не проявляют валентности, равной номеру группы.
9 / 10
1) Zn 2) Si 3) Cu 4) S 5) P
Из числа указанных в ряду элементов выберите два элемента, степень окисления которых в оксидах может принимать значение +4.
10 / 10
1) Ti 2) P 3) N 4) Al 5) O
Из указанных в ряду элементов выберите два элемента, валентность которых в молекулах летучих водородных соединений равна III.
Ваша оценка
The average score is 54%
| 01 |
Основания и кислоты — это две противоположности в химии. Как черное и белое, положительное и отрицательное, теплое и холодное, правое и левое. Именно поэтому они отлично взаимодействуют друг с другом: из двух крайностей образуется нечто нейтральное, а именно соли. Но пока мы рассмотрим, что же представляют собой эти два класса, и как им следует давать названия. |
Основания |
|
| 02 | Это достаточно немногочисленный класс неорганических соединений:
основаниями, или гидроксидами, называются вещества, состоящие из атома металла и одной или нескольких групп «OH» Группа «OH» известна также под названием гидрокси́л, от латинского произношения элементов: гидроген (водород) и оксиген (кислород). |
| 03 |
Название основания, данное по систематической номенклатуре, состоит из слова гидроксид, названия металла и его валентности, если она не постоянна: |
| 04 | Гидроксил имеет постоянную степень окисления –1:
Поэтому атом металла будет иметь положительную степень окисления, равную количеству гидроксилов в молекуле основания, а значит, и такую же валентность. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 05 | Вывести формулу основания по его названию тоже не представляет сложности. Для этого необходимо записать символ металла, затем формулу гидроксила, и, если валентность металла больше единицы, взять гидроксил в скобки и присвоить им индекс, равный валентности металла. Например:
гидроксид железа (II) — Fe(OH)2 гидроксид калия — KOH |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 06 |
Как правило, при н. у. основания являются кристаллическими веществами. Те из них, которые хорошо растворяются в воде, называются щелоча́ми, а металлы, их образующие — щелочными и щёлочно-земельными. Самая распространенная щёлочь — гидроксид натрия NaOH, — используется в целлюлозно-бумажной промышленности, при производстве мыла, в нефтепереработке и даже в качестве пищевой добавки. При этом, как и другие щёлочи, она является очень едким веществом, поэтому должна маркироваться специальным знаком (рис. 1). Раньше, до введения систематической номенклатуры, гидроксид натрия назывался едким натром. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 07 |
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Кислоты |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 08 | Перед нами следующий, также немногочисленный класс неорганических веществ:
кислоты — это соединения, состоящие из атомов водорода и кислотных остатков Как это ни забавно звучит, но кислотным остатком принято считать то, что остается от кислоты, если убрать все атомы водорода. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 09 |
Валентность кислотного остатка всегда совпадает с количеством атомов водорода в молекуле кислоты:
Очевидно, степень окисления кислотного остатка будет равна его валетности, взятой со знаком «минус», поскольку водород имеет постоянную степень окисления +1:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 10 |
В отличие от остальных классов неорганических соединений, для которых IUPAC сформулировал вполне определенные правила систематической номенклатуры, названия важнейших кислот и их кислотных остатков необходимо выучить. Все они приведены в таблице. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 11 |
Таблица. Важнейшие кислоты и кислотные остатки
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 12 |
Самые внимательные наверняка заметили, что у кислотных остатков, не содержащих атомов кислорода, названия оканчиваются буквой «д», в то время как у остальных — буквой «т». |
| 13 | А теперь — вы  |
||||||||||||
1. Назовите по систематической номенклатуре следующие основания:
2. Напишите формулы следующих оснований:
3. В 195,2 г гидроксида щелочно-земельного металла содержится столько же молекул, сколько в 100,8 г азотной кислоты. Что это за металл? 4. Среди перечисленных в таблице кислот есть несколько, которые при н. у. являются газообразными веществами. Относительная плотность одной из них по озону составляет 0,71. О какой кислоте идет речь? |
|||||||||||||
| *** |
План урока:
Валентность
Причины постоянной и переменной валентности
Правила определения степени окисления
Валентность
Представьте на минуточку, что атомы не могли бы соединяться между собой, какой вид имела бы планета, а вопрос: «Существовала ли вообще Солнечная система?» Именно благодаря тому, что атомы соединяются между собой, существуют вещества, а также и мы.
Вернёмся к деталям, мы их будем сравнивать с атомами, а их внешний вид, с количеством связей, которые они могут образовать.
Представим, что в нашем распоряжении есть вот такие детали.
Валентность элементов обусловлена количеством неспаренных электронов на внешнем уровне.
Рассмотрим металлы, расположенные в I группе. Их объединили в одно семейство щелочных металлов, поскольку реагируя с водою, они все образуют щёлочи, состава МеОН. Формула внешнего уровня имеет вид ns1. Если провести параллель с элементами конструктора, то они будут выглядеть следующим образом.
Они могут отличаться цветом, формой, однако их объединяет количество связей, которые они способны образовать. Иначе говоря, что щелочные металлы одновалентны.
Это правило срабатывает и для элементов II группы, только они будут иметь вид двойных деталей.
Вспоминаем, что элементы этой группы имеют формулу ns2, приходим к тому, что валентность атомов численно равна II.
Как возможно Вы заметили, или вспомнили с темы строение атома, что высшая валентность определяется номером группы, но не всегда ей равна. Исключением с данного правила являются атомы элементов таких как азот, фтор и кислород.
Почему фтор, находясь в VII группе, имеет валентность постоянную равную единице. В то время, для других его родственников, она будет равнять I, III, V или даже VII.
Источник
Поиграем с Вами в старую добрую игру «Найди … отличий». Несмотря на то, что они находятся в одной группе, имеют общую формулу внешнего слоя ns2np5, валентность их будет отличаться. Атомы хлора выигрывают за счёт свободного 3d уровня, на который при определённых условиях могут мигрировать электроны с наружного слоя, образуя при этом 3 возбуждённых состояния. Атом фтора в этом плане бедный, в распоряжении его электронов нет d-орбитали, его электронам некуда мигрировать.Поэтому имея только 1 неспаренный электрон, может образовать только единственную связь.
Причины постоянной и переменной валентности
Для большинства элементов характерно иметь переменную валентность. Но для некоторых она будет постоянной. Некоторые элементы Вам уже известны, пополнит этот список кислород и цинк, которые всегда двухвалентны, алюминий имеет число связей III.
Расположение элементов в периодической таблице подсказывает, о количестве связей, которые могут они образовать.
Источник
Определение валентности элементов по формулам
На рисунке изображены молекулы известных Вам веществ: это аммиак NH3, запах этого газа очень резкий и его трудно забыть, если хоть раз ощущали запах нашатырного спирта, с помощью его приводят людей в чувство после обморока.
Источник
С молекулой метана СН4 Вы встречаетесь на кухне, когда открываете газовый кран, чтобы приготовить пищу. На самом деле, метан не имеет запаха, но поскольку он относится к взрывоопасным веществам, то к нему прибавляют специальные соединения, имеющие запах, чтобы в случае утечки, его можно было обнаружить.
Молекула Н2О окружает нас повсюду. Во всех этих соединениях имеются атомы водорода, только в разных количествах. Давайте попробуем определить валентность по формуле вещества. Вспомним, что водород одновалентен. Если в аммиаке водорода насчитываем 3 атома, значит азот, условно, можем изобразить в виде такой детали.
Как видно с рисунка, он имеет валентность III. Поэтому принципу определим валентность углерода, приходим к выводу, что он четырёхвалентен.
Но не всегда мы видим структурные формулы, которые отображают связи между атомами, и не всегда имеем дело с одновалентными элементами. Возьмём, к примеру, вещество состава Р2О5. На два атома фосфора приходится 5 атомов кислорода. Постоянную валентность имеет кислород, которая равняется II. Чтобы определить, какую валентность будет иметь фосфор, необходимо выполнить следующие математические действия.
Встречаются такие соединения, где необходимо определить валентность остатков, входящих в состав кислот. Например, вещество состава Mg3(PO4)2.
Выполним согласно алгоритму. Магний всегда двухвалентен.
Искомая валентность кислотного остатка равна III. Следует заметить, что в веществе всегда находиться элемент, который проявляет постоянную валентность.
При написании уравнений реакций возникает необходимость составления формул веществ. Рассмотрим реакцию обмена между оксидом алюминия и соляной кислотой.
В результате обмена образуется два вещества состава AlCl и НО. Чтобы определить количественный состав в веществах, воспользуемся следующим алгоритмом.
Составление химических формул по валентности
Уравнение приобретает вид
Обратите внимание, что количество атомов отличается в реагентах и продуктах, его необходимо уравнять.
Составим формулы веществ по валентности элементов.
Немаловажную роль наравне с валентностью играет такое понятие как степень окисления (СО).
Термин валентность применим для соединений, имеющих молекулярное строение. Но, как известно, ещё существуют вещества ионного строения, которые образуются за счёт электростатического притяжения между разноимёнными зарядами. Каким образом они образуются? Чтобы ответить на данный вопрос, вспомним об электроотрицательности.
При образовании вещества, одни атомы будут отдавать свои электроны, другие – принимать. Рассмотрим на примере соединений молекулярного строения Cl2, HCl и ионного NaCl.
Обратите внимание, что вещества молекулярного строения, имеют структурную формулу, соединение атомов между собой показывается в виде черты – между ними. Для веществ имеющих строение, отличающее от молекулярного, более применимо понятие степени окисления, которое имеет универсальное применение для всех типов веществ.
Каким образом получается молекула вещества HCl? У водорода имеется один-единственный электрон, который располагается на 1s уровне, у хлора целых 7, занимающих уровни 3s2 и 3р5. Как Вы считаете, какой атом будет отдавать, а какой принимать электроны? При всём своём желании, атом водорода никак не сможет принять электроны хлора, ему просто некуда. Как он сможет расположить в своей 1s ячейке целых 7 электронов хлора. Логично предположить, что принимать будет хлор. Ему как раз не хватает одного электрона, чтобы завершить свой уровень. Поэтому водород будет иметь заряд +, а хлор -. Степень окисления указывается в правом верхнем углу элемента, арабскими цифрами, знак + или – ставим перед цифрой H+Cl−.
А вот какую степень окисления имеет простое вещество. Атомы равноценные партнёры, поэтому она будет нулевая.
При образовании ионного соединения NaCl натрий, как элемент имеющий малое число электронов на внешнем слое, а именно 1, подобно водороду, отдаёт его хлору, образуя при этом катион Na+, хлор при этом становится отрицательным анионом Cl−.
Правила определения степени окисления
Подобно валентности, для определённых элементов свойственна постоянная степень окисления. Это металлы, которые отличаются малым количеством электронов внешнего слоя. Отличительной характеристикой их будет невозможность иметь отрицательный заряд, поскольку они ВСЕГДА отдают электроны.
В противовес металлам существует один-единственный элемент, который абсолютно ни с кем не хочет делиться своими электронами.Ни при каких условиях он не отдаст их, это фтор, который всегда отрицателен F−.
Такой элемент, как кислород, обычно имеет отрицательный заряд, это -2. И только с фтором, он будет положительным +2.
Аналогичная ситуация с водородом, характерная СО (степень окисления) +1, однако исключения составляют соединения с металлами, где его степень окисления будет отрицательная и равняется -1.
Все эти значения вытекают с периодической системы, которая помогает определить степени окисления элементов.
Источник
С таблицы видно, что для большинства элементов эта величина не постоянная.
Чтобы вычислить степень окисления элементов в соединениях, будем руководствоваться следующими правилами.
Как бы то ни было, природа не ограничивается бинарными соединениями. Существует множество веществ состоящих из 2 и более элемента. Впрочем вычисление совсем не отличается, первоначально определяем элементы, имеющие постоянную степень окисления, а дальше проделав нехитрые математические действия находим СО для остальных. Главное правило, чтобы вещество было нейтральным, количество плюсов должно равняться количеству минусов.
К примеру, в веществе H2SO3 самым электроотрицательным является кислород, он заберёт электроны как в водороде, так и в серы, вследствие этого имеет отрицательную СО, а Hи Sстанут положительными. В этом соединение имеются 2 элемента, имеющих известную СО – это Н и О.
Обратите внимание, на нахождение СО в кислотном остатке. В данном случае, мы приравниваем не к 0, а к заряду аниона.
Здесь у серы х внизу
Как правило, валентность и степень окисления совпадают по абсолютной величине. Но исключения составляют простые вещества, например, в простом веществе азот, формула которого N2, степень окисления равняется 0, в тоже время, валентность атомов азота равна III. N0 ≡ N0.
Либо в катионе аммония NH4+. Азот имеет СО -3, а валентность IV.