Задание 1
- Описать все превращения по диаграмме(название диаграммы, описание всех
точек, линий, фаз и структур). - Определить с помощью правила отрезков:
a. структуру сплава с 20%В при Т= 400°C
b. химический состав сплава по структуре Qβ= 33%, Qα= 67% при Т= 200°C
Определить химический состав найденных (задание а) и заданных (заданиеb) фаз. - Начертить кривую охлаждения для сплава содержащего15%В.
- Определить число степеней свободы для сплава с 30%В при Т= 300°C
Решение
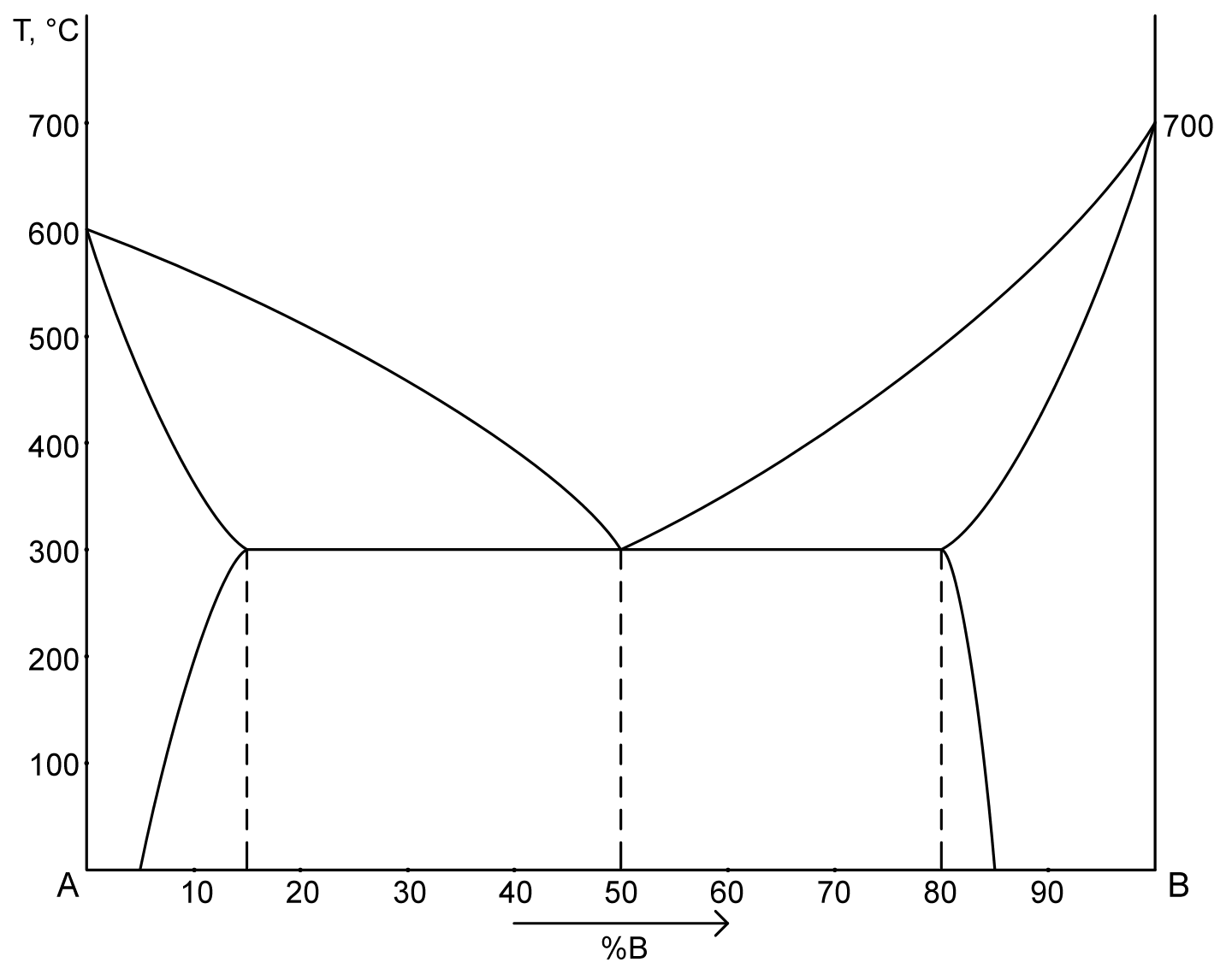
1. Диаграмма состояния сплавов, испытывающих фазовые превращения в твердом состоянии.
2 компонента:
- A – температура плавления компонента A
- B – температура плавления компонента B
3 фазы:
- L – жидкость
- α – кристаллы твердого раствора A
- β – кристаллы твердого раствора B
ACB – ликвидус
ADCEB – солидус
DF – линия предельной растворимоси компонента B в A
EG – линия предельной растворимоси компонента A в B
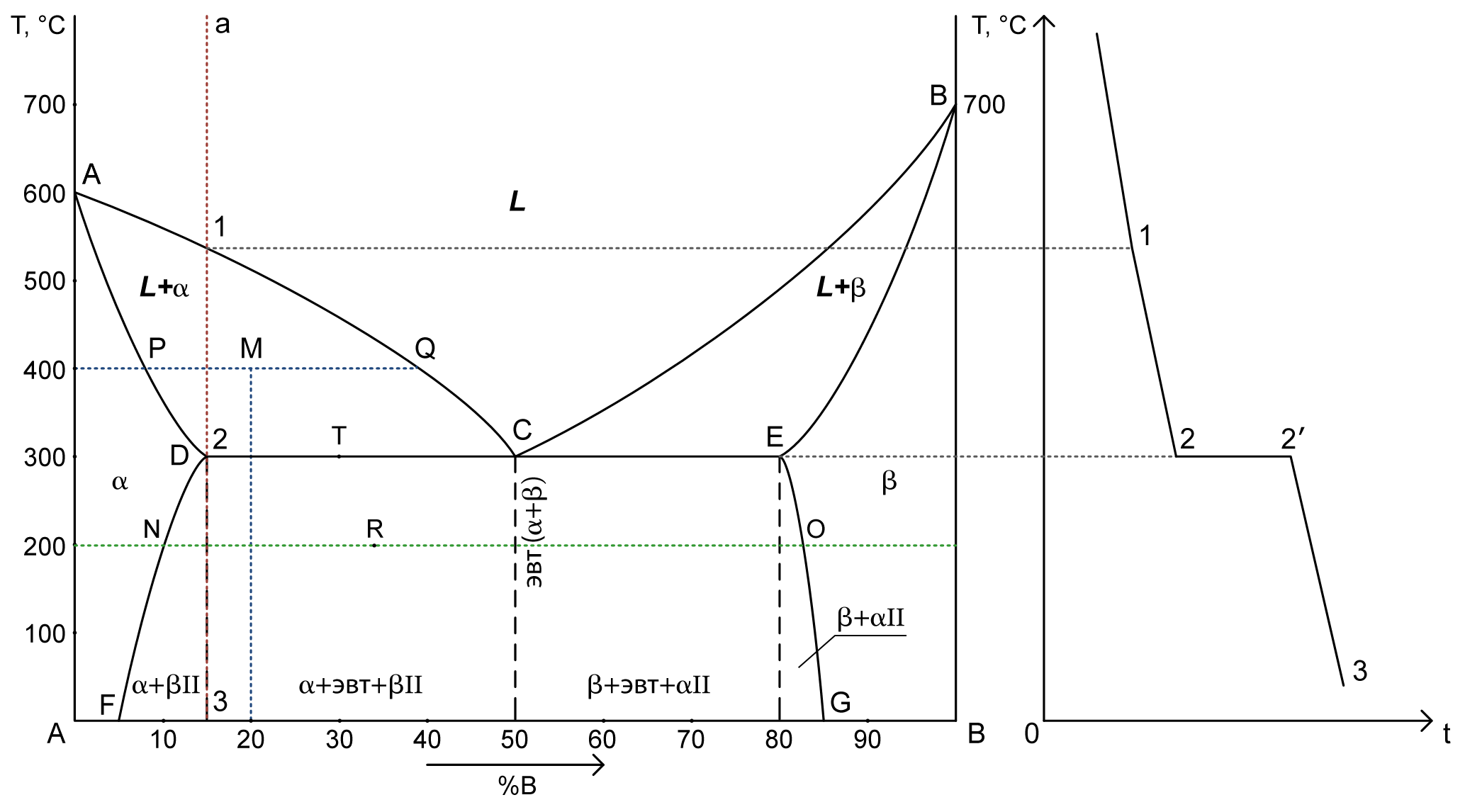
2. a) Структура сплава 20%В при Т= 400°C – точка M.
PM – твердый раствор α: 7% B => 93% A. Cα= 7% B+ 93% A
MQ – жидкость: 40% B => 60% A. Cж= 40% B+ 60% A
Qα= (MQ/PQ)·100% = (40-20)/(40-7)·100% = 60,6%
Qж= 100%-60,6% = 39,4% (Или: (PM/PQ)·100% = (20-7)/(40-7)·100% = 39,4%)
b) химический состав сплава по структуре Qβ= 33%, Qα= 67% при Т= 200°C – точка R.
Qβ/Qобщ= RN/NO = 33%/100%
RN/(83-10) = 33/100
RN ≈ 24
B = 10+24=34% => A = 66%
Cсплава= 34%B + 66%A
Cα= 10%B + 90%A
Cβ= 83%B + 17%A
3. Кривая охаждения для сплава 15%В – a
4. Число степеней свободы для сплава с 30%В при Т= 300°C – точка T.
C = 2-3+1 = 0 (компоненты (A, B) – фазы (α, β, эвтектика) + 1)
Задание 2
- Описать все превращения по диаграмме(название диаграммы, описание всех
точек, линий, фаз и структур). - Определить с помощью правила отрезков:
a. структуру сплава с 30%В при Т= 200°C
b. химический состав сплава по структуре Qβ= 40%, Qж= 60% при Т= 300°C
Определить химический состав найденных (задание а) и заданных (заданиеb) фаз. - Начертить кривую охлаждения для сплава содержащего 90%В.
- Определить число степеней свободы для сплава с 10%В при Т= 300°C
Решение
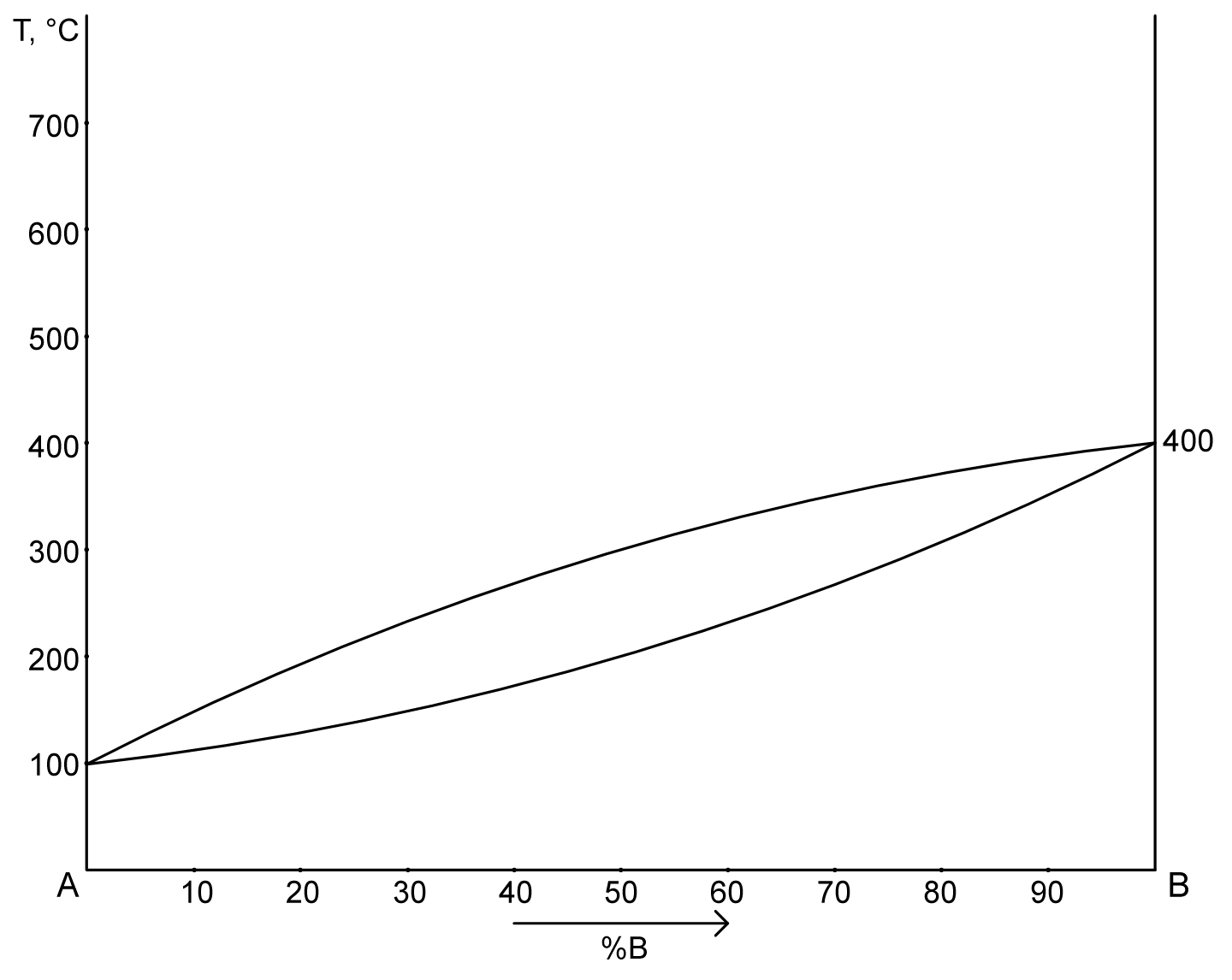
1. Диаграмма состояния сплавов с неограниченной растворимостью в твердом состоянии.
2 компонента:
- A – температура плавления компонента A
- B – температура плавления компонента B
2 фазы:
- L – жидкость
- β – кристаллы твердого раствора
ACB – ликвидус
ADB – солидус
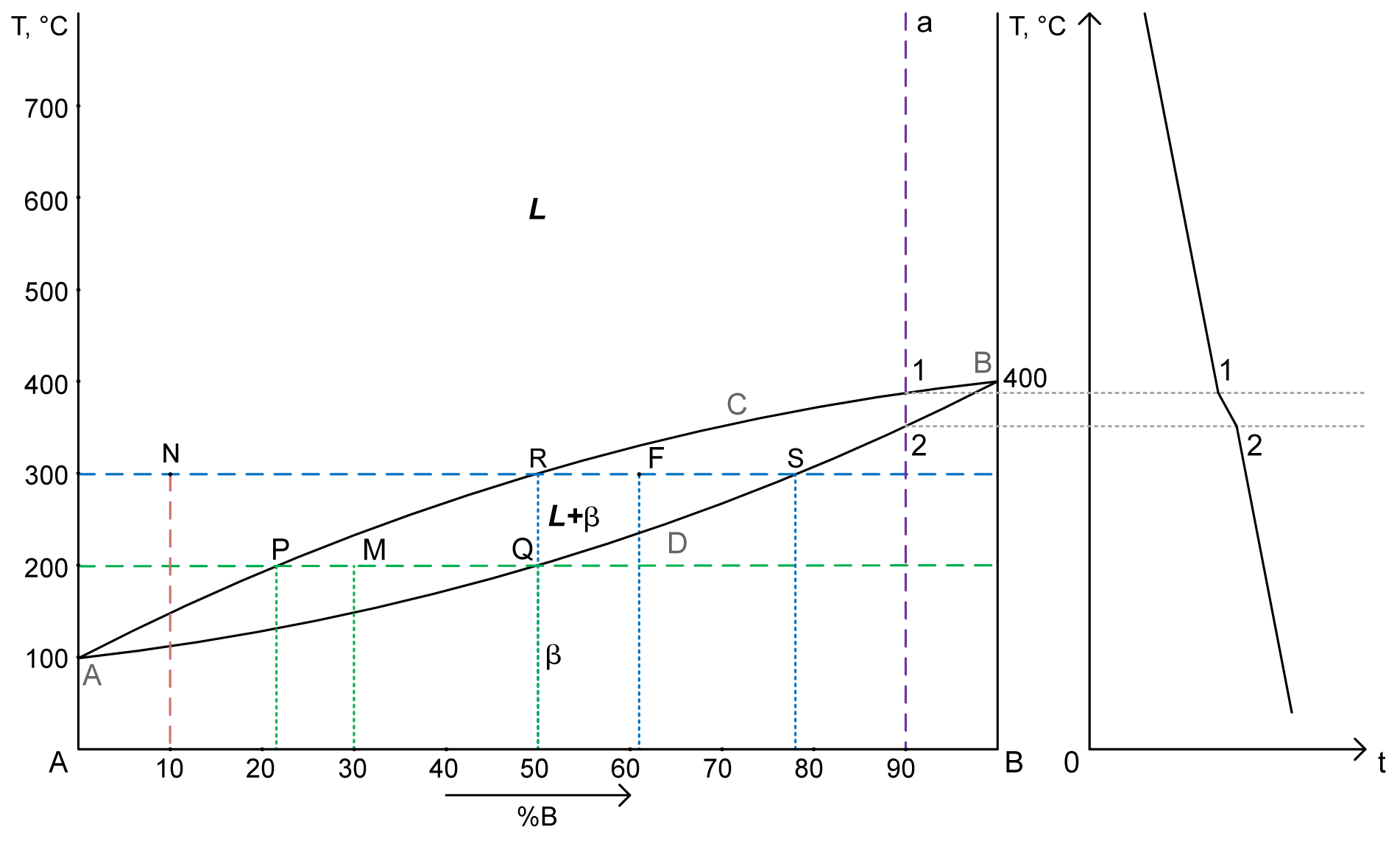
2. a) Структура сплава 30%В при Т= 200°C – точка M.
PM – жидкость: 21% B => 79% A. Cж= 21% B+ 79% A
MQ – кристаллы твердого раствора: 50% B => 50% A. Cтв= 50% B+ 50% A
Qж= (MQ/PQ)·100% = (50-30)/(50-21)·100% = 69%
Qтв= 100%-69% = 31% (Или: (PM/PQ)·100% = (30-21)/(50-21)·100% = 31%)
b) химический состав сплава по структуре Qβ= 40%, Qж= 60% при Т= 300°C – точка F.
Qβ/Qобщ= RF/RS = 40%/100%
RF/(78-50) = 40/100
RF ≈11
B = 50+11=61% => A = 39%
Cсплава= 61%B + 39%A
Cβ= 78%B + 22%A
Cж= 50%B + 50%A
3. Кривая охаждения для сплава 90%В – a
4. Число степеней свободы для сплава с 10%В при Т= 300°C – точка N.
C = 2-1+1 = 2 (компоненты (A, B) – фазы (жидкость) + 1)
По Лукашова Т.В. Варианты заданий и пример решения по двухкомпонентным диаграммам состояния [Текст]: Методическое указание / Т.В.Лукашова, М.М.Сычев, С.И. Гринева. – СПб.: СПбГТИ(ТУ), 2008. – 41 с.
Структурные составляющие сплавов
Чистые
металлы – однофазны, поскольку состоят
только из кристаллов чистого металла.
Сплавы могут быть и однофазными и
многофазными. Однофазные сплавы всегда
состоят из кристаллов твердого раствора
одного вида (состава).
В
многофазных сплавах может одновременно
присутствовать несколько структурных
составляющих: 1) кристаллы твердого
раствора (одного или нескольких составов),
2) кристаллы химических соединений, 3)
кристаллы компонент сплава, 4) эвтектики
и 5) эвтектоиды.
Первые
три структурных составляющих представляют
собой кристаллы рассмотренных выше
фаз. Аэвтектики и эвтектоиды – это
однородныекомпозиции
из кристаллов разных фаз.
Важно, что кристаллы в них сильно
измельчены
по сравнению с кристаллами твердого
раствора или первичными кристаллами.
При рассмотрении в микроскоп они выглядят
одинаковыми участками, имеют особые
свойства и поэтому являются самостоятельными
структурными составляющими.
Эвтектика
— это композиция из кристаллов, которые
образуются при распаде жидкого раствора
(при первичной кристаллизации). В
зависимости от состава они обозначаются
следующим образом:
Эвт
(А+В)
– первичные кристаллы чистыхметалловА
и В.
Эвт
(?+В)
– зерна твердого раствора?и
кристаллы компоненты В.
Эвт
(АmBn+?)
– кристаллы химического соединения
АmBn
и твердого раствора?и
т.д.
Эвтектики
имеют важную особенность. Они плавятся
при температуре, которая меньше
температуры плавления составляющих её
фаз.
Другой
тип структурной составляющей, внешне
похожий на эвтектику – эвтектоид.
Он образуется из твердой фазы (при
вторичной кристаллизации), поэтому при
нагреве эвтектоид не плавится. Пример
обозначения: Эвт-д
(?
+ ?)
—эвтектоидная
смесь состоит из кристаллов твердых
растворов ?
и ?.
Самый известный пример эвтектоида —
перлит
в углеродистых сталях.
Особой
структурной составляющей является
мартенсит
(чаще всего образуется в сталях).
Большинство
сплавов при изменении температуры
изменяют свой фазовый состав и,
следовательно, микроструктуру. Фотографии
микроструктур различных сплавов с
описанием их структурных составляющих
можно посмотреть на сайте
microstructure.ru.Подробно
в учебнике.
Диаграммы состояния
Описание
любых сплавов всегда начинается с
рассмотрения их диаграмм состояний.
Поэтому имеет смысл разобраться, что
на них изображено и зачем они нужны.
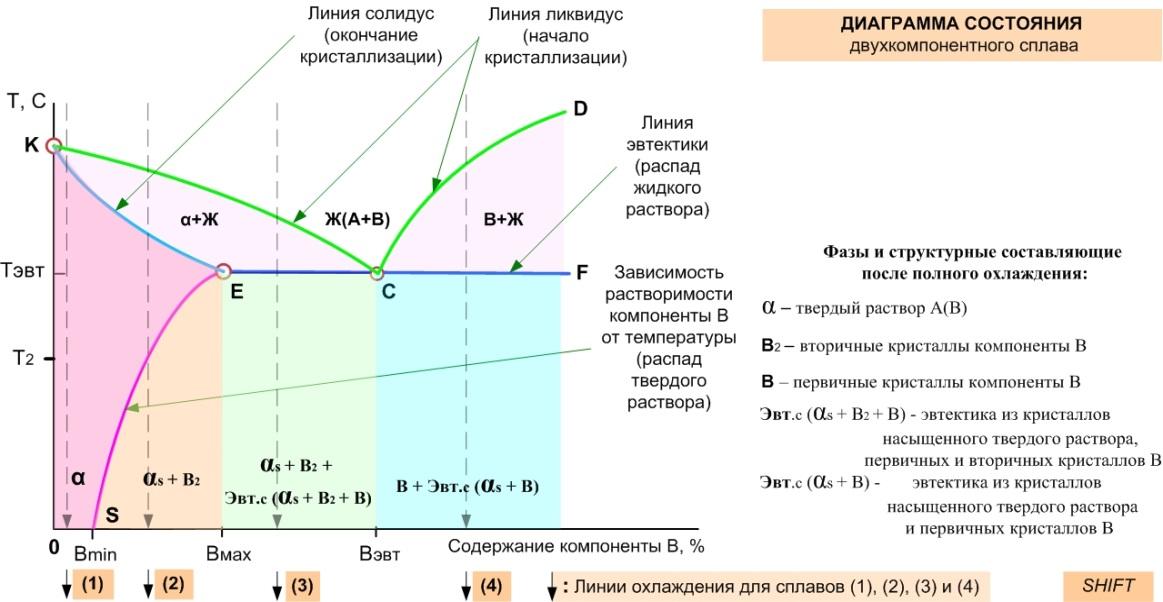
Существует с десяток видов диаграмм.
Одна
из них показана на рисунке и описывает
систему, две компоненты которой (А
и В)
неограниченно растворимы в жидком
состоянии, но ограниченно растворимы
в твердом состоянии. По вертикальной
оси отложена температура, погоризонтальной
– концентрация компоненты В.
Такая диаграмма позволяет рассматривать
свойства целого семейства сплавов.
Линии
KCD
и KEпоказывают
как зависят от концентрацииВ
температуры начала
(ликвидус TL)
и окончания
кристаллизации
(солидусTS).
Величина интервала кристаллизации, (TL
– TS),
в котором растут кристаллы твердого
раствораА
иВ,
зависит от состава сплава.
Линия
SE
(линия сольвус) характеризует растворимость
компонентыВот
температуры (в данном случае она
уменьшается при охлаждении). Линии
солидус и сольвуспересекаются в точке
Е.
Ей соответствует температура Тэвт,
при которой кристаллы твердого раствора,
растущие из расплава, становятся
насыщенными и поэтому не могут расти
дальше.
Поскольку
«нормальная» кристаллизация не
завершается, отвердение жидкой фазы
должно закончиться иначе: при температуре
ТЭВТ
из оставшейся части жидкого раствора
образуется эвтектика. Соответствующая
температура называется эвтектической,
а линия EF
– линией эвтектики.
Пересечение
линии солидус с линией эвтектики
определяет точкуС
(точка эвтектики). Ей соответствует
состав сплава, называемый эвтектическим.
Видно, что эвтектический состав имеет
температуру (а не интервал!) плавления
ТЭВТ,
которая
ниже температуры плавления компонент,
составляющих сплав. Этот факт объясняет
происхождение термина: на древнегреческом
«эвтектика» означает «легкоплавкая».
Диаграмма
состояния позволяет определить:
1.
области существования сплавов с
однотипной микроструктурой (на рисунке
выделены цветом)
2.
превращения, которые могут происходить
при изменении температуры
3.возможные
фазы и структурные составляющие, которые
и определяют свойства сплавов.
4.
интервалы кристаллизации и температуры
проведения различных видов термообработки.
Кристаллизация
сплавов.
Кристаллизация
сплавов подчиняется тем же закономерностям,
что и кристаллизация чистых металлов.
Необходимым условием является стремление
системы в состояние с минимумом свободной
энергии.
Основным
отличием является большая роль
диффузионных процессов, между жидкостью
и кристаллизующейся фазой. Эти процессы
необходимы для перераспределения
разнородных атомов, равномерно
распределенных в жидкой фазе.
В
сплавах в твердых состояниях, имеют
место процессы перекристаллизации,
обусловленные аллотропическими
превращениями компонентов сплава,
распадом твердых растворов, выделением
из твердых растворов вторичных фаз,
когда растворимость компонентов в
твердом состоянии меняется с изменением
температуры.
Эти
превращения называют фазовыми
превращениями в твердом состоянии.
При
перекристаллизации в твердом состоянии
образуются центры кристаллизации и
происходит их рост.
Обычно
центры кристаллизации возникают по
границам зерен старой фазы, где решетка
имеет наиболее дефектное строение, и
где имеются примеси, которые могут стать
центрами новых кристаллов. У старой и
новой фазы, в течение некоторого времени,
имеются общие плоскости. Такая связь
решеток называется когерентной связью.
В случае различия строения старой и
новой фаз превращение протекает с
образованием промежуточных фаз.
Нарушение
когерентности и обособления кристаллов
наступает, когда они приобретут
определенные размеры.
Процессы
кристаллизации сплавов изучаются по
диаграммам состояния.
Диаграмма
состояния.
Диаграмма
состояния представляет
собой графическое изображение состояния
любого сплава изучаемой системы в
зависимости от концентрации и температуры
(рис. 4.5)
.
Рис.
4.5. Диаграмма состояния
Диаграммы
состояния показывают устойчивые
состояния, т.е. состояния, которые при
данных условиях обладают минимумом
свободной энергии, и поэтому ее также
называют диаграммой равновесия, так
как она показывает, какие при данных
условиях существуют равновесные фазы.
Построение
диаграмм состояния наиболее часто
осуществляется при помощи термического
анализа.
В
результате получают серию кривых
охлаждения, на которых при температурах
фазовых превращений наблюдаются точки
перегиба и температурные остановки.
Температуры,
соответствующие фазовым превращениям,
называют критическими точками. Некоторые
критические точки имеют названия,
например, точки отвечающие началу
кристаллизации называют точками
ликвидус,
а концу кристаллизации – точками
солидус.
По
кривым охлаждения строят диаграмму
состава в координатах: по оси абсцисс
–концентрация компонентов, по оси
ординат – температура.
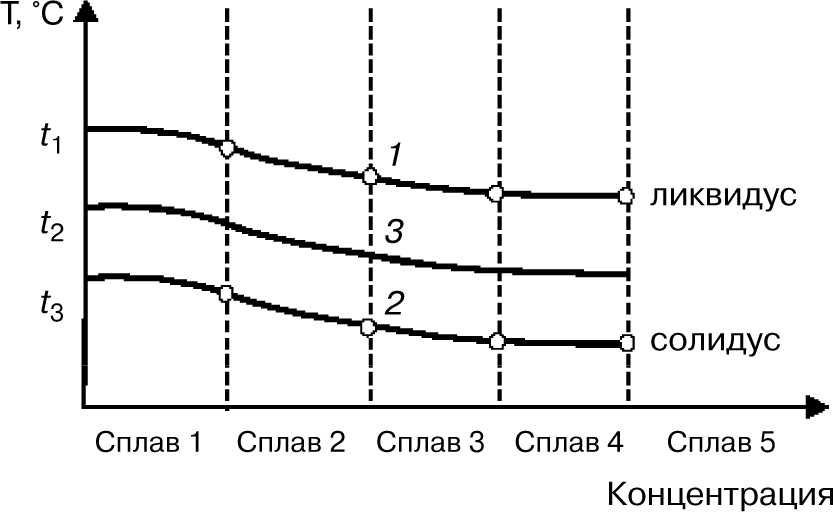
Шкала
концентраций показывает содержание
компонента В. Основными
линиями являются линии ликвидус (1) и
солидус (2), а также линии соответствующие
фазовым превращениям в твердом состоянии
(3, 4).
По
диаграмме состояния можно определить
температуры фазовых превращений,
изменение фазового состава, приблизительно,
свойства сплава, виды обработки, которые
можно применять для сплава.
-
Диаграмма
состояния сплавов с отсутствием
растворимости в твердом состоянии (I
типа)
Диаграмма
состояния сплавов, образующих механические
смеси из чистых компонентов (I рода)
Исходные
данные: оба компонента неограниченно
растворимы в жидком состоянии, а в
твердом состоянии нерастворимы и не
образуют химических соединений.
Компоненты:
химические элементы А, В (К = 2).
Фазы:
жидкость Ж, кристаллы А, В (Ф = 3).
Примером
диаграмм этого типа является диаграмма
состояния сплавов системы Pb-Sb. Диаграмма
Pb-Sb строится на основе использования
кривых охлаждения, полученных методом
термического анализа (рис. 1).
Система
сплавов Pb-Sb включает в себя составы со
100 % РЬ и 0 %
Sb, т. е. чистый свинец, и со 100 % Sb и 0 % РЬ,
т. е. чистую сурьму. Кривые охлаждения
для этих чистых металлов имеют по одному
горизонтальному участку, характеризующему
температуру кристаллизации: соответственно
для свинца 327 °С и для сурьмы 631 °С. На
диаграмме состояния эти температуры
находятся на осях ординат, где содержатся
соответственно чистый свинец и чистая
сурьма. Структура чистых металлов
представляет собой однородные зерна.
Рис.
1. Диаграмма состояния, кривые охлаждения
и схемы структур сплавов системы Pb—Sb
при полном охлаждении до комнатной
температуры
Сплав,
содержащий 13 % Sb и 87 % РЬ, также имеет один
горизонтальный участок, т. е. одну
критическую точку (245 °С) -температуру
затвердевания этого сплава. Этот сплав
характеризуется тем, что в нем происходит
одновременнаякристаллизация из
жидкой фазы кристаллов РЬ и Sb (в общем
случае компонентов А и В) с образованием
механической смеси. Такая механическая
смесь двух (или более) видов кристаллов,
одновременно кристаллизующихся из
жидкости, называется эвтектикой. Сам
сплав с 13 % Sb и 87 % РЬ является эвтектическим,
а его микроструктура представляет собой
попеременно чередующиеся выделения
сурьмы в свинцовой основе (рис. 1). Принято
эвтектическую реакцию записывать так:
Ж —> Pb + Sb, или в общем виде Ж —> А + В.
Кристаллизация
любого сплава, имеющего 0 % < Sb < 13 %,
начинается с выделения кристаллов РЬ.
Эти сплавы затвердевают в интервале
температур, и на кривых охлаждения
имеются две критические точки,
соответствующие началу и концу
затвердевания (например, сплав с 5 % Sb,
рис. 1). Все они называются до эвтектическими
сплавами, претерпевают эвтектическое
превращение при охлаждении ниже
температуры 245 °С и имеют после
окончательного охлаждения структуру
РЬ + Э(РЬ + Sb), рис. 1. В этой структуре
имеется две структурные составляющие:
кристаллы РЬ и эвтектика Э(РЬ + Sb), которые
получаются на базе двух фаз: кристаллов
РЬ и кристаллов Sb.
Кристаллизация
любого сплава с концентрацией 100 % > Sb
>> 13 % начинается с выделения кристаллов
Sb. Эти сплавы также
затвердевают
в интервале температур — начала и конца
затвердевания (например, сплав с 40 % Sb,
рис. 5.1). При охлаждении ниже температуры
245 °С в них протекает эвтектическое
превращение. Эти сплавы называются
заэвтектическими и имеют после охлаждения
окончательную структуру Sb + Э(РЬ + Sb),
рис. 1. Структура заэвтектических сплавов
также является двухфазной (кристаллы
Sb и РЬ) и состоит из двух структурных
составляющих: кристаллов Sb и эвтектики
Э (Pb + Sb).
На
диаграмме можно выделить три характерные
зоны: область, где существует только
жидкая фаза, — выше системы линий,
ограниченной точками: температура 327
°С — эвтектическая точка 245 °С — температура
631 °С; область, где существует только
твердая фаза (кристаллы РЬ и Sb), — ниже
эвтектической линии (вся горизонтальная
линия на уровне температуры 245 °С с
концами в месте ее пересечений с
ординатами со 100 % РЬ и 100 % Sb); область,
где одновременно сосуществует жидкая
и твердая фаза (область с жидко-твердой
фазой) — между линиями, ограничивающими
соответственно жидкое и твердое состояние
сплавов.
Линия,
ограничивающая на диаграмме область
жидкой фазы сплавов, называется линией
ликвидус. Линия, ограничивающая область
полностью затвердевшего сплава от
остальной области на диаграмме состояний,
называется линией солидус.
-
Диаграммасостояния
сплавов с неограниченной растворимостью
компонентов в твердом состоянии(II
типа)
Диаграмма
состояния сплавов с неограниченной
растворимостью компонентов в твердом
состоянии (II рода)
Исходные
данные: оба компонента неограниченно
растворимы в твердом и жидком состоянии
и не образуют химических соединений.
Компоненты:
химические элементы А, В (К = 2).
Фазы:
жидкость Ж, кристаллы твердого раствора
а (Ф = 2).
Примером
сплавов с такими диаграммами состояния
являются сплавы системы Cu-Ni.
Если
два компонента (А и В) неограниченно
растворяются в жидком и твердом состоянии,
то они не могут при затвердевании
образовывать собственных кристаллов
во всех сплавах на базе этих компонентов.
Соответственно при кристаллизации в
этих сплавах будут выделяться кристаллы
а-твердого раствора, а следовательно,
максимальное число фаз в этих сплавах
равняется двум (жидкость и a-твердый
раствор). В этом случае в соответствии
с правилом фаз кристаллизация всех
сплавов будет протекать только в
интервале температур (кристаллизация
при постоянной температуре у сплавов
возможна только при наличии трех фаз)
и, соответственно, на диаграмме состояния
отсутствует горизонтальная линия, а
присутствуют только наклонные кривые
(рис. 2).
тНа
диаграмме (рис. 5.2) присутствуют три
области: область выше линии Аа’В —
жидкость; область между линиями Аа’В и
АЬ’В — жидкость и твердый раствор. Ниже
линии АЬ’В — область твердого раствора.
Линия Аа’В является линией ликвидус, а
линия АЬ ‘В — линией солидус.
Кристаллизация
любого сплава начинается выпадением
из жидкого расплава отдельных кристаллов
твердого раствора а (например, в точке
а’, рис. 2) и заканчивается полным
затвердеванием твердого раствора
(например, в точке Ъ’, рис 5.2). Но так как
в интервале кристаллизации (например,
между точками а’ и Ъ’, рис. 2) сплавы
находятся в двухфазном состоянии (Ж +
а), то при понижении температуры должно
изменяться соотношение количества
жидкой и твердой фазы в двухфазной
области — количество жидкости уменьшается,
а количество a-твердого раствора растет.
Кроме того, при понижении температуры
будут меняться также составы жидкой и
твердой фаз. Для определения относительного
количества каждой фазы и состава фаз
на диаграммах состояния любого типа,
пользуются правилом отрезков (правилом
рычага), основные положения которого
формулируются следующим образом. Чтобы
определить концентрации компонентов
в двухфазной области, через интересующую
нас точку, характеризующую состояние
сплава (состав сплава и его температуру),
проводится горизонтальная линия до
пересечения с линиями, ограничивающими
двухфазную область. Проекции точек
пересечения на ось концентраций покажут
состав жидкой и твердой фаз.
Рис.
2. Диаграмма состояния, кривые охлаждения
и схемы типовых структур сплавов с
неограниченной растворимостью в твердом
состоянии
Чтобы
определить количественное соотношение
жидкой и твердой фаз, необходимо составить
обратно пропорциональную зависимость
между их количеством и отрезками
горизонтальной линии, образованными
между точкой, характеризующей состояние
сплава, и точками, определяющими состав
жидкой и твердой фаз.
Рассмотрим
на примере двух типов диаграмм (рис. 3),
как с помощью правила отрезков можно
определить количество и состав фаз,
например, для состояния, соответствующего
точке k.
Для
определения соотношения фаз и их состава
через точку k проводим горизонтальную
линию до пересечения с линиями,
ограничивающими двухфазную область на
диаграмме (точки las, рис. 3, а, б). Проекции
точек пересечения на ось концентраций
показывают состав жидкой фазы (точка V
— проекция точки I, лежащей на линии
ликвидус) и твердой фазы (точка s’ —
проекция точки s, соответствующей на
рис. 3, а концентрации 100 % Sb и лежащей на
линии солидус на рис. 3, б). В соответствии
с правилом рычага отрезки горизонтальной
линии между точкой k и точками, определяющими
составы фаз, обратно пропорциональны
количествам этих фаз, т. е. можно записать:
—
где Q„ Q, — количество твердой и жидкой
фаз соответственно.
Для
определения отношения какой-либо фазы
(твердой или жидкой) ко всему количеству
сплава Qs +, используются выражения:
где
si — вся длина горизонтальной линии.
Правило
отрезков может использоваться не только
для изучения процесса кристаллизации
сплавов, но и для рассмотрения процессов,
происходящих в твердом состоянии. Оно
применимо ко всем двухфазным сплавам
независимо от их агрегатного состояния.
Рис.
3. Применение правила отрезков для
сплавов, образующих механические смеси
(а) и твердые растворы (б)
Если
вернуться к рассмотрению диаграммы
состояния с неограниченной растворимостью
компонентов в твердом состоянии (рис.
2), то следует обратить внимание на то,
что во всем интервале кристаллизации
(например, от точки а’ до Ь’) из жидкого
сплава с концентрацией компонентов,
отвечающей точке k (45 % Си + 55 % Ni) (рис. 3),
происходит постоянное выделение новых
кристаллов. Причем состав первых
кристаллов определяется проекцией
точки s, лежащей на линии солидус.
Заканчивается выделение новых кристаллов
сплава k в точке Ь’, когда затвердевает
последняя капля жидкости, имеющая
состав, определяемый проекцией точки
I, лежащей на линии ликвидус.
Отсюда
следует, что при охлаждении сплава в
интервале кристаллизации состав жидкой
фазы в соответствии с правилом отрезков
меняется по линии ликвидус, а твердой
фазы — по линии солидус.
-
Диаграмма
состояния сплавов(III типа) с односторонней
ограниченной растворимостью одного
компонента в твердом состоянии.
-
Диаграмма
состояния сплавов(III
типа)с ограниченной растворимостью
обоих компонентов в твердом состоянии.
Диаграмма
состояния сплавов с ограниченной
растворимостью компонентов в твердом
состоянии (III рода)
Диаграмма
с эвтектическим превращением
Исходные
данные: оба компонента неограниченно
растворимы в жидком состоянии, ограниченно
растворимы в твердом состоянии и не
образуют химических соединений.
Компоненты:
химические элементы А, В (К = 2).
Фазы:
жидкость Ж, твердые растворы а (раствор
компонента А в В) и Р (раствор компонента
В в А) (Ф = 3).
Этот
тип диаграмм очень важен в практическом
отношении, так как часто представлен в
составе сложных диаграмм широко
распространенных промышленных сплавов,
например сплавов систем Fe-C, Al-Cu и др.
В
рассматриваемой системе ограниченная
растворимость компонентов в твердом
состоянии может не меняться с изменением
температуры, а может и меняться. Оба
рассматриваемых случая представлены
на рис. 4 (соответственно линии EN и DF). В
итоге имеем диаграмму состояния с
двусторонней ограниченной растворимостью
компонентов в твердом состоянии.
На
этой диаграмме линия GCH — линия ликвидус,
выше которой все сплавы имеют однородный
жидкий раствор. Линия GEDH -линия солидус,
ниже которой в сплавах отсутствует
жидкая фаза.
В
рассматриваемой системе компоненты А
и В не могут при затвердевании образовывать
собственных кристаллов, так как они
между собой образуют твердые растворы
а и Р в тех областях диаграммы, которые
расположены соответственно слева от
вертикалит
Рис.
4. Диаграмма состояния, кривые охлаждения
и схемы образования структур сплавов
с ограниченной растворимостью в твердом
состоянии и с эвтектическим превращением
EN
и справа от линии DF. В этих областях все
сплавы кристаллизуются в интервале
между ликвидусом и солидусом, так же,
как этот процесс проходит в любом сплаве
на диаграммах состояния II рода (см. разд.
5.2). Соответственно в области, лежащей
слева от линии EN при кристаллизации из
жидкости начинают выделяться кристаллы
твердого раствора а (например, для сплава
I в точке 1). В интервале кристаллизации
сплавы имеют двухфазную структуру Ж +
а. После завершения кристаллизации и
вплоть до окончательного охлаждения
все эти сплавы имеют структуру однородного
твердого раствора а. Аналогичная ситуация
имеет место у всех сплавов, расположенных
правее точки F, с той лишь разницей, что
вместо a-твердого раствора у них выделяются
кристаллы (3-твердого раствора.
У
сплавов, расположенных в интервале
между точкой F и проекцией точки D,
первичная кристаллизация в интервале
междуликвидусом и солидусом протекает
аналогично ранее описанной. При этом
эти сплавы после завершения кристаллизации
вплоть до пересечения с линией DF имеют
однородную структуру Р-твердого раствора
(например, сплав IV в интервале между
точками 2 и 3). При дальнейшем же охлаждении
этих сплавов (например, сплаваIV ниже
точки 3) вплоть до полного охлаждения в
структуре этих сплавов происходят
изменения, связанные с выделением из
Р-твердого раствора второй фазы ап
(например, у сплава IV), причиной появления
которой является уменьшение предела
растворимости P-твердого раствора при
снижении температуры сплава. На это
указывает наклонный характер кривой
DF. При понижении температуры твердый
раствор Р становится пересыщенным
компонентом А, и для приведения системы
в равновесие из этого твердого раствора
Р выделяется избыток растворенного
компонента А. Но так как в рассматриваемой
системе чистые компоненты не могут
существовать как самостоятельные фазы
(они должны образовывать твердые
растворы), то на базе избыточных кристаллов
компонента А образуется сразу же
a-твердый раствор, кристаллы которого
и выделяются из P-твердого раствора и
располагаются в виде мелкодисперсных
включений внутри зерен основной фазы
(см. рис. 4). Такие избыточные кристаллы,
выделяющиеся не из жидкости, а из твердой
фазы, обозначаются ап (вторичные а
кристаллы), а сам процесс выделения
новой фазы в твердом состоянии называется
вторичной кристаллизацией.
Точки
Е и N характеризуют предельную растворимость
компонента В в компоненте А, т. е.
предельную растворимость а-твер-дого
раствора при эвтектической и комнатной
температурах, а точки D и F — предельную
растворимость компонента А в компоненте
В, т. е. предельную растворимость
P-твердого раствора также при эвтектической
и комнатной температурах.
Как
видно, предельная растворимость
a-твердого раствора не изменяется с
понижением температуры (линия EN —
вертикальная), а предельная растворимость
p-твердого раствора с понижением
температуры уменьшается (линия DF —
наклонная).
Точки
Е и D являются границами линии ED, в
пределах которой протекает эвтектическое
превращение, а точка С — эвтектической
точкой. Следовательно, во всех сплавах,
расположенных в пределах границ
эвтектической линии, будет проходить
эвтектическое превращение, аналогичное
тому, которое имеет место на диаграммах
состояния I рода (см. разд. 5.2) с той лишь
разницей, что в данном случае эвтектика
состоит не из механической смеси
компонентов А и В, а из механической
смеси их твердых растворов а и р. В данном
случае эти твердые растворы как бы
являются компонентами сплавов для той
части диаграммы, которая ограничена
длиной эвтектической линии. Соответственно,
эвтектика в этом случае будет иметь
вид: Э(а + (3), а эвтектическая реакция
может быть записана так: Ж —> а? + рв.
Сплав с концентрацией компонентов А и
В, соответствующей проекции точки С, т.
е. сплав состава точки С, называется
эвтектическим.
Все
сплавы, расположенные между точками С
и Е, называются до эвтектическими. Их
кристаллизация будет начинаться с
выделения кристаллов a-твердого раствора
(например, сплава II в точке 1). В интервале
кристаллизации (например, между точками
1 и
2) у этих сплавов будет двухфазная
структура Ж + а. На линии ЕС (например, в
точке 2) в доэвтектических сплавах будет
проходить эвтектическая реакция у той
части жидкости Ж, которая еще осталась
в сплаве на этот момент (ее количество
можно определить по правилу отрезков).
Поэтому для доэвтектических сплавов
правомерно будет записать эвтектическую
реакцию в следующем виде: а + Ж —» а + Э(а
+ (3). Они после окончательного охлаждения
будут иметь структуру а + Э (а + Р).
Все
сплавы, расположенные между точками С
и D, называются заэвтектическими. Их
кристаллизация будет начинаться с
выделения кристаллов (3-твердого раствора
(например, у сплава III в точке Г). В
интервале кристаллизации (например, у
сплава III между точками 1 и 2) эти сплавы
имеют двухфазную структуру Ж + (3. На
линии CD у заэвтектических сплавов будет
проходить эвтектическая реакция,
подобная реакция доэвтектических
сплавов, т. е. Р + Ж —> (3 + Э(а + (3). Но при
дальнейшем охлаждении заэвтектических
сплавов в их структуре будут проходить
последующие превращения, которых не
было в доэвтектических сплавах. Причиной
этих превращений является наклонный
характер линии DF. Как уже было показано
ранее, при наклонном характере кривой
растворимости компонента А в компоненте
В (линия DF) с понижением температуры
предельная растворимость А в В становится
меньше того количества А, которое в
данный момент присутствует в сплаве.
Поэтому из твердого раствора Р будет
выделяться ап. Следовательно, все
заэвтектические сплавы ниже температуры
эвтектического превращения (например,
сплав III ниже точки 2) будут иметь следующую
структуру: р + Э (а + Р) + ап Эта структура
содержит три структурных составляющих:
р, Э(а + Р) и а„, но при этом структура
является двухфазной: a-фаза и Р-фаза.
-
Диаграмма
состояния сплавов образованием
химических соединений(IV
типа)
Диаграмма
состояния сплавов, образующих химические
соединения (IV рода)
Исходные
данные: оба компонента неограниченно
растворимы в жидком состоянии, нерастворимы
в твердом состоянии, но образуют
химические соединения.
Компоненты:
химические элементы А и В (К = 2).
Фазы:
жидкость Ж, кристаллы компонентов А, В
или химического соединения А„ВШ (Ф =
3).
Химическое
соединение может быть устойчивым, т. е.
до расплавления сплава не разлагаться
при нагреве. Соответственно неустойчивое
химическое соединение при нагреве
разлагается.рис. 6. Диаграмма состояния
с устойчивым химическим соединением
Рис.
6. Диаграмма состояния с устойчивым
химическим соединением
Рассмотрим
диаграмму состояния с устойчивым
химическим соединением. Такая диаграмма
изображена на рис. 6.
Примером
диаграмм этого типа является диаграмма
состояния сплавов системы Mg—Са.
Химическое
соединение (например,
А„Вт)
характеризуется определенным соотношением
компонентов (например, п % компонента А
и т % компонента В). На оси концентрации
компонентов (ось абсцисс) химическое
соединение обозначает точку, из которой
выходит вертикальная линия, фактически
разбивающая диаграмму на две простые
диаграммы, в которых химическое соединение
выступает уже в качестве самостоятельного
компонента и, соответственно, образует
эвтектики с компонентом А по реакции Ж
—» А + А„Вт (7 простая диаграмма) и с
компонентом В по реакции Ж —» В + А,Д,„
(II простая диаграмма).
Кристаллизация
сплавов в пределах I и II простых диаграмм
проходит аналогично кристаллизации
сплавов, образующих эвтектику из чистых
компонентов (диаграмма I рода). Поэтому
после окончательного остывания у
эвтектического сплава на I простой
диаграмме структура будет состоять
только из эвтектики Э(А + А(1В„,), у
эвтектического сплава на II простой
диаграмме -из эвтектики Э(В + А„Вт); у
доэвтектических сплавов соответственно
на I простой диаграмме и на II простой
диаграмме структура будет иметь вид: А
+ Э(А + А„Вт) и А„В,„ + Э(В + А„Вт); у
заэв-тектических сплавов на I простой
диаграмме — А„ВШ + Э (А + А„Вт) и у
заэвтектических сплавов на II простой
диаграмме — В + Э (В + + АяВт).
Диаграмма
состояния сплавов, испытывающих
полиморфные превращения
Исходные
данные: оба компонента неограниченно
растворимы в жидком состоянии, в твердом
состоянии могут образовывать механические
смеси, в результате эвтектического или
пе-ритектического превращения, а также
могут образовывать непрерывные твердые
растворы, и, кроме всего перечисленного,
хотя бы один из компонентов обладает
полиморфизмом.
Компоненты:
химические элементы: А, В (К — 2).
Фазы:
жидкость Ж, твердые растворы а, (З (Ф =
3).
8,%— N B,°/o —
Рис.
7. Диаграммы состояний с полиморфными
превращениями
При
полиморфных превращениях в сплавах
происходит перекристаллизация
существующих твердых фаз, которая
подчиняется тем же закономерностям,
что определяют процесс кристаллизации
из жидкого состояния.
Если
в сплавах один или оба компонента
обладают полиморфизмом, то и сами сплавы
из этих компонентов претерпевают
полиморфные превращения в твердом
состоянии. В этом случае диаграммы
состояния становятся «многоярусными»,
причем верхний ярус диаграммы характеризует
первичную кристаллизацию из жидкого
состояния, а нижняя часть диаграммы —
вторичную (перекристаллизацию), т. е.
выделение кристаллов новой твердой
фазы из твердой первичной фазы, например
кристаллов a-твердого раствора из
первичного (3-твердого раствора с другой
кристаллической решеткой (рис. 7, а).
В
общем случае вид диаграммы рассматриваемого
случая зависит от того, какие фазы
образуются в сплавах в процессе
полиморфных превращений. Всевозможных
вариантов может быть много. Но мы
рассмотрим два наиболее характерных
случая (рис. 7, а, б).
В
первом случае (рис. 7, а) компонент А имеет
аллотропические модификации Аа и Ар,
которые образуют с компонентом В два
твердых раствора а и р.
Кристаллизация
сплавов в интервале кристаллизации с
учетом перитектического превращения
уже была ранее описана. В результате
сплавы до температуры, соответствующей
точке С (температуры полиморфного
превращения), имеют либо однофазную
структуру Р-твердого раствора, либо
двухфазную структуру а + Р-твердого
раствора. В этих сплавах при охлаждении
ниже температуры полиморфного превращения
проходит полиморфное превращение Р —»
а с изменением кристаллической решетки.
Во
втором случае (рис. 7, б) оба компонента
испытывают полиморфные превращения,
при этом низкотемпературные модификации
их ограниченно растворимы друг в друге,
а высокотемпературные модификации —
неограниченно.
Не
останавливаясь на деталях процесса
кристаллизации сплавов из жидкого
состояния (см. разд. 5.2), отметим, что в
нижнем ярусе диаграммы фактически
представлена диаграмма III рода, т. е.
диаграмма с образованием ограниченных
твердых растворов и протеканием
эвтектического превращения. Однако
отличительная черта данного эвтектического
превращения состоит в том, что исходной
фазой распада является не жидкость Ж,
а твердый раствор у, который при переходе
через линию KCN распадается на два новых
раствора а и (3 по реакции у —> а + р.
Такое
превращение, по сути аналогичное
эвтектическому, но происходящее в
твердом состоянии, называется эвтектоидным,
а полученная механическая смесь —
эвтектоидом. Сплав состава точки С
называется эвтектоидным. Соответственно,
сплавы, расположенные слева от точки С
(сплав эвтектоидного состава) называются
доэвтектоидными, а справа от нее —
заэвтектоидными.
-
Стали
обыкновенного качества, качественные,
высококачественные, марки и применение.
|
Стали Углеродистые Стали Углеродистые Стали Углеродистые Стали Легированные |
Углеродистые
стали
Углеродистая
сталь обыкновенного качества выпускается
виде заготовок с установок непрерывной
разливки труб, штамповок, ленты, проволоки
следующих марок: СтО, Ст1кп, Ст1пс, Ст2кп
и т.д.
Буквы
Ст обозначают сталь, цифры – условный
номер марки и не указывают массовое
содержание углерода. Индексы означают: кп –
кипящая, пс –
полуспокойная, сп –
спокойная сталь.
Углеродистая
качественная сталь выпускается
марок 05кп, 08кп, 08пс, 08, 10кп, 10пс, 10, 11кп,
15пс и т.д. Цифры в марке означают среднее
массовое содержание углерода в сотых
долях процента. Из этой стали делают
ответственные детали машин и механизмов,
штамповки, калиброванные прутки,
серебрянку – светлые, круглые прутки
точных размеров со специальной отделкой
поверхности.
Углеродистая
инструментальная сталь выпускается
следующих марок:
качественная –
У7, У8, У9 и т.д. до У13
высококачественная –
У7А, У8А, У8ГА, У9А, У10А, У11А, У12А и У13А.
Цифры
стоящие после буквы У (углеродистая
инструментальная), указывают содержание
углерода в десятых долях процента
(например, в стали У7 содержится 0,7% С);
буква Г – повышенное содержание марганца;
буква А указывает, что сталь
высококачественная. Инструментальную
сталь используют для изготовления
режущих, измерительных и других
инструментов (зубил, молотков, отверток,
ножей, ножниц, сверл, хирургических
инструментов и др.). В
высококачественной стали содержится
меньше серы, фосфора и других вредных
примесей. Она лучше сопротивляется
действию ударных нагрузок, имеет большую
прочность.
Автоматная
сталь (
с повышенным содержанием серы и фосфора) –
углеродистая сталь специального
назначения – маркируют буквой А, после
которой следует цифра, показывающая
среднее содержание углерода в сотых
долях процента; буква Г – повышенное
содержание марганца, Например, А12, А20,
А30, А35, А40Г. Так как сера и фосфор придают
стали хрупкость, поэтому она идет на
изготовление малоответственных деталей,
главным образом крепежных (втулки, болты
и др.)
Легированные
стали
Для
обозначения легирующих элементов
приняты следующие буквы: Х – хром, Н –
никель, Г – марганец, С – кремний, В –
вольфрам, М – молибден, Ф – ванадий, К
– кобальт, Т – титан, Ю – алюминий, Д –
медь, П –фосфор, Р – бор, А – азот, Е –
селен, Ц – цирконий, Б – ниобий. Сталь
может содержать один или несколько
легирующих элементов, которые придают
им специальные свойства.
Для
легированной конструкционной стали
принята маркировка, по которой первые
две цифры указывают среднее массовое
содержание углерода в сотых долях
процента. Если содержание углерода
меньше 0,1%, то первая цифра ноль, например
06, 08. Цифры, следующие за буквами
(указывающими легирующее элементы) –
процентное массовое содержание этих
элементов в стали. Если за буквой
отсутствует цифра, то это значит, что
сталь содержит данный элемент в количестве
до 1,5%, кроме элементов, присутствующих
в малых количествах (для комплексно-легированных
сталей). Например, марка 35Х обозначает
хромовую сталь, в которой около 0,35% С и
до 1,5% Cr; 45Г2 – марганцевую сталь с
содержанием около 0,45% С и 2% Mn
К
конструкционным легированным
сталям относятся цементируемые
легированные стали(низкоуглеродистые
и среднелегированные) получают, насыщая
поверхность стали углеродом и подвергая
ее термической обработке. Этим
обеспечивается высокая поверхностная
твердость и сохраняется прочность
сердцевины металла. Марки: 15Х, 18ХГ, 25 ХГМ
и др. Эти стали предназначены для деталей,
работающих в условиях трения, при высоких
давлениях и ударных нагрузках (деталей
автотракторной, автомобильной
промышленности и др.).
Улучшаемые
легированные стали (среднеуглеродистые
и низколигированные)
термически улучшают, подвергая закалке
и высокому отпуску (500-600 0С) для обеспечения
необходимых свойств (прочности,
пластичности, вязкости). Марки: 40ХС,
40ХФА, 50ХГ. Эти стали применяют для
деталей, работающих с переменными и
ударными нагрузками (валы, шатуны,
зубчатые колеса и т.д.)
Высокопрочные
легированные стали –
это стали, имеющие предел прочности
180–200 кг/мм2. В
качестве высокопрочных широкое применение
получили стали с 0,45-0,50% С, дополнительно
легированные Cr, Mo, W и V. После закалки и
низкотемпературного отпуска предел
прочности этих сталей достигает 200-220
кг/мм2 при сравнительно удовлетворительной
пластичности и вязкости. Такие стали
находят применение в машино-, ракето- и
самолетостроении.
Инструментальная
легированная сталь входит
в группу среднелегированных сталей.
Введение хрома, вольфрама, ванадия,
молибдена, марганца, кремния, никеля
придает инструментальным сталям высокую
твердость, износоустойчивость, способность
выдерживать высокие температуры, не
теряя твердость, и другие ценные
свойства.По сравнению с ними углеродистые
стали хрупки (особенно после закалки),
поэтому, изготовленные из них режущие
инструменты при нагреве ~ до 2000С теряют
свою твердость.
Инструментальная
легированная сталь делится на две группы
Стали
для режущего и измерительного инструмента
марок 7XФ, 8ХФ, 11Х, 13Х, ХВ5, В1, 9ХС, ХВГ, 9ХВГ,
ХВГС, 9Х5Ф, 9Х5ВФ,8Х4ВФ1; из них изготавливаю
пилы, резцы, фрезы, метчики, развертки,
сверла, клейма и др.
Стали
для штампованного инструмента марок
9Х, Х6ВФ, Х12, 5ХНМ, 5ХГМ, 6ХВТ и ряд других;
применяют для изготовления горячих и
холодных штампов, молотовых штампов,
пресс-форм и т.д.
К
инструментальным легированным сталям
относится также быстрорежущая сталь,
отличающаяся высокой твердостью и
теплостойкостью. Они входят в группу
высоколегированных сталей. Установлены
следующие марки быстрорежущей стали:
Р18, Р12, Р9, Р6М3, Р9Ф5, Р9К10, Р18Ф2 и др. Эти
стали применяют при обработке широкого
круга конструкционных материалов, для
резьбонарезных инструментов, работающих
с ударными нагрузками, для отделки
материалов с абразивными свойствами
(пластмасс, эбонита) и т.д.
Легированные
стали специального назначения делятся
на две группы
Стали
с особыми физическими свойствами
Стали
с обычными химическими свойствами
Стали
с особыми физическими свойствами
применяют для изготовления деталей
машин и механизмов, обладающих этими
свойствами. Так, в электротехнике для
изготовления постоянных магнитов,
электромагнитов, трансформаторов
применяют сплавы, имеющие большую
магнитную проницаемость. Для элементов
электронагревательных устройств,
реостатов нужны сплавы с высоким
омическим сопротивлением. В приборах,
где ферромагнитные материалы могут
повлиять на точность показаний,
применяются немагнитные сплавы. Все
эти свойства стали приобретают за счет
введения легирующих примесей. Они
являются высоколегированными. Стали и
сплавы с высоким омическим сопротивлением
состоят из хрома и никеля. Их марки
Х15Н60, Х20Н80 и др.
Магнитотвердые
сплавы идут
на изготовление постоянных магнитов.
Их марки 52КФ11, 52 Кф13 (первая цифра –
содержание кобальта, цифра после буквы
Ф – содержание ванадия в %).
Магнитомягкие
сплавы марок
50 Н (50% Ni), З4НКМ, 38НС и др. используют для
изготовления сердечников, трансформаторов,
электромагнитов.
Немагнитные
стали являются
заменителями цветных металлов в
электромашиностроении. Применяются
стали марок Н25, 55Н9Г9.
Износоустойчивые
стали используются
для изготовления рабочих элементов
землеройных машин, шаровых мельниц и
других сильно изнашивающихся деталей.
К ним относятся высокмарганцовистые
стали марки Г13.
Существуют
и другие сплавы с особыми физическими
свойствами.
К
группе сплавов с особыми химическими
свойствами относятся высоколегированные
коррозионностойкие, жаростойкие и
жаропрочные стали.
Коррозионостойкие
(нержавеющие) стали –
это высокохромистые стали марок 1Х13,
2Х13, 3Х13 и др. (первая цифра указывает на
содержание углерода в десятых долях %,
остальные – содержание хрома в %). Кроме
хрома, в состав сталей вводятся никель,
титан, ванадий (марки 1Х13Н3, 1 Х17Н2 и др.)
Жаростойкие
(окалиностойкие) стали не
окисляются при действии высоких
температур и небольших нагрузок.
Стойкость против окисления в этих
сплавах создается за счет введения
хрома, алюминия, кремния. Марки: Х28, Х5,
1Х12 СЮ и др. Из них изготавливаются камеры
сгорания, чехлы к термопарам, муфели.
Жаропрочные
стали сохраняют
прочность при высоких температурах и
могут работать в этих условиях под
действием больших нагрузок (детали
реактивных двигателей, лопасти паровых
и газовых турбин). Жаропрочные стали
являются одновременно и жаростойкими.
Марки жаропрочных сталей: ХН70ВМТЮ,
ХН75МБТЮ и др.
-
Чугуны.
Белый чугун. Процессы графитизации в
чугунах.
Сплавы
железа
с углеродом, в которых содержание
углерода более 1,7% называются
чугунами.
Чугуны различаются по
структуре, способам изготовления,
химическому составу и назначению.
По
структуре чугуны бывают серые, белые и
ковкие. По способам изготовления—обыкновенные
и модифицированные.
По химическому
составу чугуны различают не легированные
и легированные, т. е. такие, в составе
которых имеются специальные примеси.
Углерод
в чугуне может находиться в связанном
состоянии – в виде карбида железа
(цементита) и в свободном – в виде
графитовых включений различной формы,
или одновременно в виде карбида и
графита. В зависимости от этого различают
чугуны.
1.
Белый, в нем весь
углерод находится в связанном состоянии
в виде карбидов, излом чугуна имеет
характерный блестящий белый цвет;
2.
Серый, большая часть
углерода в нем находится в свободном
состоянии в виде графита, имеющего
пластинчатую форму;
3.
Ковкий, большая часть
углерода в этом чугуне находится в
свободном состоянии в виде графита,
имеющего хлопьевидную форму (углерод
отжига);
4.
Высокопрочный, в нем
большая часть углерода находится в
свободном состоянии в виде графита,
имеющего шаровидную форму.
Белый
чугун
Белый
чугун применяется в машиностроении в
значительна меньших количествах, чем
серый. Он представляет собой сплав
железа с углеродом, в котором углерод
находится в виде химического соединения
с железом. Белый чугун очень хрупкий и
твёрдый. Он не поддаётся механической
обработке режущими инструментами и
применяется для отливки деталей, не
требующих обработки, или подвергается
шлифованию абразивными кругами. В
машиностроении применяется белый чугун
как обыкновенный, так и легированный.
Сварка
белого чугуна весьма затруднительна в
связи с образованием трещин при нагреве
и охлаждении, а также из-за неоднородности
структуры, образующейся в месте сварки.
Белый
и отбеленный чугун – применение
Описанный
выше состав белого чугуна определяет
его высокую твердость, сочетающуюся с
хрупкостью, затрудняющими в целом
обработку заготовок механическими
способами (резание, фрезерование и т.д.)
и требующими применения специальных
приемов такой обработки (инструменты
из марок быстрорежущих сталей). В чистом
виде применение белых чугунов
довольно ограничено.
Промышленностью
выпускается специальный, называемый
передельным, белый чугун, применение
которого специализировано для переплавки
в различные стали. Нормирование ГОСТами
определяет пониженность содержания в
его составе кремниевых добавок и более
высокую концентрацию марганцев. Такие
заготовки получают литьевыми способами.
В
зависимости от степени графитизации
при выплавке могут получаться половинчатые,
переходные стадии чугунов, эти сплавы
принято называть отбеленный чугун.
Такой сплав содержит наряду с карбидами
железа (химически связанный углерод –
Fe3C)
графитовый углерод (свободный углерод
– C).
И
этот чугун используется в качестве
фрикционных деталей механизмов сухого
трения, таких как всем известные тормозные
колодки. Наряду с тем, таким сплавам
также свойственна высокая износоустойчивость,
поэтому из них выполняют валы и валки
на прокатном оборудовании широкого
назначения.
Структура
белого чугуна – в чем принципиальное
отличие?
Растворимость
цементитов (Fe3C,
где содержание С около 6,5%) в аустенитах
(не химическое соединение железа и
углерода, а раствор включения, где
свободный углерод внедрен в кристаллическую
решетку железа) на классической диаграмме
состояния железоцементитных сплавов
(по таким диаграммам вычисляют состав
фазы сплава в тот или иной температурный
момент) составляет чуть более двух
процентов.
В
чугунах углероды могут присутствовать
как цементит и графит. Формы зерен
графитов и соотношение их количества
с цементитами (также количеством и
формой) определяют виды чугунов.
По
составу они могут иметь добавки кремния,
фосфора, серы, марганца. Кроме того, в
виду хрупкости, иногда применяется
легирование алюминием, никелем, хромом
или ванадием. Очевидно, что с изменением
характеристик и составов, в спектре
сплавов чугунов, углероды могут
содержаться в большем количестве, как
пластинчатые графиты. И цвет изломов
будет серым. Поэтому принято называть
такие разновидности серыми.
В
таких сплавах железа, углеродов и
кремния, присутствуют также сера,
марганец и фосфор. В отличие от белого
сплава, в сером углерод содержится в
свободном виде. В то время как структура
белого чугуна содержит углероды в виде
карбидов железа.
Как
уже говорилось, белым называется чугун,
в котором преобладающими связанными
углеродными структурами являются
ледебуриты (как род состояния цементитов
точки плавления), перлиты и собственно
цементиты. Такое сочетание придает
материалу высокую твердость и хрупкость,
что затрудняет прямое его применение.
Из такого применения можно назвать его
использование для изготовления
великолепных шаров и цильпебсов
(цилиндров) для измельчения рудных
материалов, пород, шлаков, клинкеров,
других материалов.
Процесс
образования графита в чугуне называется
графитизацией. Основными
факторами, влияющими на процесс
графитизации, являются скорость
охлаждения и химический состав чугуна.
Скорость
охлаждения.
Образование графита из жидкости или
аустенита при охлаждении происходит в
узком интервале температур, следовательно,
для того, чтобы как можно дольше жидкость
и аустенит находились в этих интервалах
температур, скорость охлаждения должна
быть мала. В производственных условиях
скорость охлаждения удобно характеризовать
по толщине стенки отливки. Чем тоньше
отливка, тем быстрее охлаждение и в
меньшей степени протекает графитизация.
Химический
состав.
Углерод
и кремний
способствует графитизации чугуна,
поэтому с увеличением их содержания в
чугуне графитизация будет протекать
полнее. Содержание кремния в чугуне
составляет 1,2-3,5%.
Марганец
препятствует графитизации, т.е. затрудняет
выделение графита и способствует
образованию карбидов и таким образом
способствует получению белого чугуна.
Сера
способствует
отбеливанию чугуна. Ее отбеливающее
влияние в 5 раз больше, чем для марганца.
Фосфор
на процесс графитизации заметного
влияния не оказывает.
Образование
графита может происходить не только
при кристаллизации из жидкости или
аустенита. Возможен и другой способ его
образования – в результате распада
предварительно образовавшегося
цементита, в процессе длительного
нагрева его при высоких температурах.
При температуре выше PSK цементит
распадается на аустенит и графит, а ниже
PSK цементит распадается на феррит и
графит.
-
Серый
чугун, микроструктура, марки, применение.
Серый
чугун
Такое
название чугун получил по виду излома,
который имеет серый цвет. В структуре
серого чугуна имеется графит. Поскольку
структура чугуна состоит из металлической
основы и графита в большинстве случаев
(в форме пластин), то и свойства его будут
зависеть от этих двух составляющих.
Таким образом, большая часть углерода
в сером чугуне находится в виде чешуек
графита, чем частично разобщает
металлическую сплошность сплава и
вызывает хрупкость. Содержание углерода
в сером чугуне не должно превышать 4%.
Наиболее прочные чугуны содержат 2,8—3%
углерода. Процесс выделения графита
сопровождается увеличением его объема,
что понижает общую усадку чугуна до 1%.
Кроме того, при увеличении содержания
углерода чугун становится более
жидкотекучим. Вследствие этого углерод
повышает литейные свойства и позволяет
получать качественное тонкостенное
литье. Кроме этих составляющих в составе
чугуна имеются кремний, марганец, сера,
фосфор и в меньшем количестве другие
элементы.
Кремнийявляется
элементом, который способствует получению
серого чугуна. Он образует с железом
химические соединения (FeSi и Fe3Si2)и
способствует выделению графита. Таким
образом, увеличение количества кремния
в чугуне приводит к уменьшению в нем
карбидов железа и, следовательно, к
улучшению обрабатываемости его режущими
инструментами. Кроме того, кремний
увеличивает жидкотекучесть, понижает
температуру плавления и способствует
замедлению охлаждения чугуна. Количество
кремния в сером чугуне колеблется в
пределах от 0,75 до 3,75%.
Марганецувеличивает
устойчивость карбидов железа (Fe3C)
при затвердевании и охлаждении чугуна,
что способствует получению белого
чугуна.Присутствие марганца в сером
чугуне также допускается в количестве
до 1,3%, так как марганец повышает прочность
чугуна, парализует вредное влияние
серы, а также улучшает жидкотекучесть
чугуна.
Серапонижаетжидкотекучесть
чугуна, делая его густым, плохо заполняющим
форму,противодействует выделению
графита и придает чугуну хрупкость.
Поэтому она является вредной примесью.
Предельно допустимое содержание серы
в чугуне0,07%.
Фосфор
создает в чугуне твердую и хрупкую
фосфидную эвтектику, поэтому в отливках
деталей машин, подверженных ударным
нагрузкам, его содержание не должно
превышать 0,3%. В отливках, работающих на
истирание, твердые участки фосфидной
эвтектики повышают их износоустойчивость;
в таких отливках допускается содержание
фосфора до 0,7—0,8%. Фосфор, кроме того,
понижает температуру плавления чугуна,
сильно увеличивает его жидкотекучесть
и уменьшает усадку. Это позволяет
получать из фосфористого чугуна тонкие
отливки с чисто гладкой поверхностью.
Поэтому чугун, содержащий до 1,2% фосфора,
применяется для художественного литья
труб и т. д.
Микроструктура
чугуна состоит из металлической основы
(матрицы) и графитных включений. Свойства
чугуна
определяются свойствами металлической
основы и характера включений графита.
Чугуны
содержат следующие структурные
составляющие графит (Г); перлит (П); феррит
(Ф); ледебурит (Л); фосфидную эвтектику.
По
микроструктуре различают: белый чугун
I (Ц+Г); серый перлитный чугун II (П+Г); серый
ферритный чугун III (Ф+Г); половинчатый
чугун II а (П+Ц+Г); высокопрочный чугун IV
(П+шаровидный графит).Формирование
микроструктуры чугуна зависит от его
химического состава и скорости охлаждения
(толщины) отливки. Структура металлической
основы определяет твердость чугуна.
Углерод
в составе чугуна может присутствовать
в виде химического соединения — цементит
Fe3C, графита или их смеси. По сравнению
с металлической основой графит имеет
низкую прочность. Места его залегания
можно считать нарушениями сплошности
металла. Чугун как бы пронизан включениями
графита, ослабляющими его металлическую
основу. По мере округления графитных
включений (за счет модифицирования
чугуна присадками SiCa, FeSi, Al, Mg) их
отрицательная роль как надрезов
металлической основы снижается и
механические свойства чугуна
растут.Например, серый чугун (пластинчатая
форма графита) имеет низкие характеристики
механических свойств, так как пластинки
включений графита играют роль концентратов
напряжений в отливке. Однако серый чугун
имеет ряд преимуществ: обладает высокой
жидкотекучестью и малой литейной
усадкой; включения графита делают
стружку ломкой, позволяя легко обрабатывать
чугун резанием; благодаря смазывающему
действию графита чугун обладает хорошими
антифрикционными свойствами; хорошо
гасит вибрации и резонансные колебания.
Из высокопрочных чугунов (шаровидная
форма графита) изготавливают ответственные
детали: зубчатые колеса, коленчатые
валы.
Маркировка
серого чугуна
Отливками
из серого чугуна называются литые
изделия,получаемые путем переплавки в
вагранках или иных плавильных агрегатах
доменных чушковых чугунов, чугунного
и стального лома с последующей заливкой
полученного жидкого металла в литейные
формы. Таким образом, чугун в отливках
есть чугун вторичной плавки.
Марка
серого чугуна состоит из букв Сч (серый
чугун) и цифры,показывающей значение
временного сопротивления при растяжении
(кгс/мм2).Показателями
механических свойств серых чугунов в
соответствии с ГОСТ 1412-79 является
прочность при статическом растяжении
(табл. 1).
Таблица
1 – Механические свойства серых чугунов
|
чугун |
σв, |
НВ |
|
Сч15 |
150 |
163-229 |
|
Сч25 |
250 |
180-250 |
|
Сч40 |
400 |
207-285 |
|
Сч45 |
450 |
229-289 |
|
Сч00 |
Испытание |
Механические
свойства чугуна обусловливаются
строением его металлической основы, а
также количеством, формой и характером
расположения включений графита.
Лучшими
механическими свойствами обладает
перлитный чугун, содержащий графит в
виде мелких равномерно рассеянных
чешуек; особенно повышенные свойства
получаются при округлых (глобулярных)
включениях графита.
Для
повышения прочности чугунов производится
их легирование (никелем,хромом, молибденом,
медью и др.), а также модифицирование и
термическая обработка (отжиг, закалка
и отпуск).
Серый
чугун наиболее широко применяется в
машиностроении для отливок из него
различных деталей машин. Он характеризуется
тем, что углерод в нём находится в
свободном состоянии в виде графита.
Поэтому серый чугун хорошо обрабатывается
режущими инструментами. В изломе он
имеет серый и темно-серый цвет. Получается
серый чугун путём медленного охлаждения
после плавления или нагревания. Получению
серого чугуна также способствует
увеличение в его составе содержания
углерода и кремния.
Механические
качества серого чугуна зависят от его
структуры.
По структуре серый чугун
бывает:
-
феррито-графнтовый,
-
феррито-дерлито-графитовый
и -
перлито-графитовый.
Если
серый чугун быстро охлаждать после
плавления, то он отбеливается, т. е.
становится очень хрупким и твердым.
Серый чугун в несколько раз лучше
работает на сжатие чем на растяжение.
Серый
чугун достаточно хорошо сваривается с
применением предварительного подогрева
и в качестве присадочного мате риала
специальных чугунных стержней с
повышенным содержанием углерода и
кремния. Сварка без предварительного
подогрев затруднена вследствие
отбеливания чугуна в зонах шва.
-
Высокопрочный
чугун, получение, марки, применение.
Чугун
с повышенными показателями прочности.
Получают высокопрочный чугун главным
образом модифицированием. В качестве
модификатора используют магний (Mg),
кальций (Ca),
церий (Ce)
и другие элементы. Микроструктура
высокопрочного чугуна характеризуется
наличием графита шаровидной формы, что
и обеспечивает повышение прочности.
Наибольший эффект повышения прочности
достигается в толстостенных отливках.
Пример маркировки: ВЧ 40-10, где первая
цифра показывает предел прочности при
растяжении в кгс/мм2,
а вторая — относительное удлинение в %.
Известно, что на сферических поверхностях
внутренние напряжения не концентрируются.
Именно это и положено в основу производства
высокопрочных чугунов, у которых графит
приобретает шаровидную форму. Структура
металлической основы у таких чугунов
феррито-перлитная с большим или меньшим
количеством перлита.
Получают
высокопрочные чугуны путем введения в
ковш с жидким чугунов специальных
присадок, получивших название
модификаторов. Модификаторы играют
роль искусственных центров кристаллизации
и, равномерно распределяясь по объему
жидкого металла, приводят к началу
кристаллизации не только от стенок
литейной формы, но и внутри самого объема
этой формы. Поскольку искусственный
зародыш в момент кристаллизации чугуна
со всех сторон окружен жидким металлом,
это создает условия для формирования
кристаллов сферической формы.
В
качестве модификаторов обычно используется
магний, но т.к. введение металлического
магния сопровождается сильным
пироэффектом, то чистый магний заменяют
его лигатурами (например,
сплавом магния и никеля).
Неплохие результаты дает модифицирование
чугуна церием или силикокальцием.
+ — Таблица
механических свойств некоторых марок
высокопрочных чугунов
чтобы свернуть
В
таблице 1 приведены механические свойства
некоторых марок высокопрочных чугунов.
Таблица
1 — Механические свойства высокопрочных
чугунов
|
Марка |
σв, |
δ, |
Твердость |
Структура |
|
ВЧ |
38 |
17 |
140-170 |
Феррит |
|
ВЧ |
42 |
12 |
140-200 |
То |
|
ВЧ |
50 |
7 |
171-241 |
То |
|
ВЧ |
60 |
2 |
200-280 |
Перлит |
|
ВЧ |
80 |
2 |
250-330 |
То |
|
ВЧ |
120 |
2 |
302-380 |
То |
Высокопрочные
чугуны успешно можно использовать в
самых разнообразных отраслях техники,
как заменители сталей. При этом следует
иметь в виду, что наибольший эффект от
модифицирования достигается в
толстостенных отливках. Высокопрочный
чугун после изотермической закалки с
выдержкой в бейнитной области
Умеренно
легированный чугун с шаровидным графитом,
который подвергнут изотермической
закалке на бейнит для получения высокой
прочности при достаточной пластичности.
-
Ковкий
чугун, получение, марки, применение.
Ковкий
чугун
Ковкий
чугун обычно получают из отливок белого
чугуна путем длительного томления их
в печах при температуре 800—950°С, Существуют
два способа получения ковкого чугуна:
американский и европейский.
При
американском способе томление производится
в песке при температуре 800—850°С. При
этом углерод из химически связанного
состояния переходит в свободное состояние
в виде графита, располагаясь между
зёрнами чистого железа. Чугун приобретает
вязкость, почему и называется ковким.
При
европейском способе томление отливок
производится в железной руде при
температуре 850—950°. При этом углерод из
химически связанного состояния с
поверхности отливок переходит в железную
руду и таким путём поверхность отливок
обезуглероживается и становится мягкой,
почему и чугун называется ковким, хотя
сердцевина остается хрупкой.
В
обозначениях марок ковкого чугуна после
букв пишется число, показывающее среднюю
величину предела прочности при разрыве
в кг/мм2, а затем число, показывающее
удлинение в %.
Например КЧ37—12
обозначает ковкий чугун, с пределом
прочности, равным 37 кг/мм2, и удлинением
12%.
Сварка
ковкого чугуна сопряжена с затруднениями
в связи с отбеливанием чугуна в зоне
шва.
Содержание страницы
- 1. Основные сведения о сплавах
- 2. Диаграмма состояний для случая неограниченной растворимости компонентов в твердом состоянии
- 3. Диаграмма состояний сплавов, образующих механические смеси из чистых компонентов
- 4. Диаграмма состояния сплавов для случая ограниченной растворимости компонентов в твердом состоянии
- 5. Диаграмма состояния сплавов, образующих химические соединения
- 6. Структурные составляющие железоуглеродистых сплавов
- 7. Диаграмма состояния «железо — цементит»
- 8. Диаграмма состояния «железо — графит»
1. Основные сведения о сплавах
Чистые металлы характеризуются низким пределом прочности, поэтому в машиностроении применяют главным образом их сплавы. Металлическим сплавом называют сложное вещество, полученное сплавлением (или спеканием) нескольких металлов или металлов с неметаллами. При этом улучшаются эксплуатационные и технологические свойства металлического материала.
Компонентами называют вещества, образующие систему. Чистый металл представляет собой однокомпонентную систему, сплав двух металлов — двухкомпонентную систему и т.д. Фазой называют однородную часть системы, имеющую одинаковый состав, одно и то же агрегатное состояние и отделенную от остальных частей системы поверхность раздела, при переходе через которую химический состав или структура вещества изменяются скачкообразно. Совокупность фаз, находящихся в равновесии при определенных внешних условиях (давлении, температуре), называют системой.
Сплав называют однородным (гомогенным), если его структура однофазна, и разнородным (гетерогенным), если его структура состоит из нескольких фаз.
Под структурой сплава понимают видимое в микроскоп взаимное расположение фаз, их форму и размеры. Твердые растворы образуются в результате перехода в твердое состояние однородных жидких растворов. Твердые растворы бывают следующих типов: твердые растворы замещения и твердые растворы внедрения. Независимо от типа твердые растворы однофазны.
Химические соединения образуются при сплавлении различных металлов или металла с неметаллом. Химическое соединение — однородное кристаллическое тело, имеющее кристаллическую решетку с упорядоченным расположением атомов, которая отлична от решеток элементов, образующих это соединение.
Механическая смесь двух компонентов А и В образуется тогда, когда при кристаллизации компоненты сплава неспособны к взаимному растворению в твердом состоянии и не вступают в химическую реакцию с образованием соединения. Рентгенограмма сплава отчетливо показывает наличие двух решеток компонентов А и В.
Температуры, при которых изменяется строение металлов и сплавов, называют критическими точками. При плавлении и затвердевании чистые металлы имеют одну критическую точку, а сплавы — две. В интервале между этими двумя точками в сплавах существуют две фазы — жидкий сплав и кристаллы.
2. Диаграмма состояний для случая неограниченной растворимости компонентов в твердом состоянии
Диаграмма состояния — графическое изображение фазового состояния сплавов в зависимости от температуры и концентрации компонентов. Рассмотрим диаграмму состояния сплавов системы «медь — никель», которая является диаграммой для случая неограниченной растворимости компонентов в твердом состоянии (рис. 3).
Температура плавления меди 1083°С, никеля — 1445°С. Чистые металлы имеют одну критическую точку — температуру затвердевания (кристаллизации), а сплавы — две, т.е. сплавы, в отличие от чистых металлов, кристаллизуются в интервале температур. Например, кристаллизация сплава начинается при температуре t1, при этой температуре из жидкого сплава начинают выпадать первые кристаллы твердого раствора, а заканчивается кристаллизация при температуре t3. При этой температуре затвердевает последняя капля жидкого сплава. Разная температура конца кристаллизации сплавов свидетельствует о том, что состав твердой фазы непрерывно изменяется.
Для построения диаграммы состояния рассматриваемой системы на оси абсцисс сетки в координатах температура — концентрация откладывают составы пяти сплавов и восстанавливают из каждой точки вертикальные линии. После этого переносят на эти вертикальные линии с кривых охлаждения сплавов критические точки, а на левой и правой ординатах температур отмечают температуры кристаллизации чистых металлов — меди (100%) и никеля (100%). Соединив плавными кривыми температуры начала и конца кристаллизации всех сплавов, получают диаграмму состояния сплавов системы «медь — никель» с неограниченной растворимостью компонентов в твердом состоянии.
Верхняя линия на диаграмме обозначает начало затвердевания при охлаждении или конец расплавления при нагреве, нижняя — соответственно конец затвердевания или начало плавления. Эта диаграмма состояния сплава меди и никеля имеет три области. Область существования жидкого расплава
(1) лежит выше верхней линии, соединяющей точки плавления меди и никеля, а область существования кристаллических твердых растворов (2) — ниже нижней линии. Между этими линиями находится двухфазная область (3), в которой одновременно существуют расплав и кристаллы твердого раствора. Верхнюю границу этой области называют линией ликвидус, а нижнюю — линией солидус («ликвидус» в переводе с латинского означает жидкий, «солидус» — твердый). По диаграмме состояния можно определить концентрации твердой и жидкой фаз в сплаве при его кристаллизации.
3. Диаграмма состояний сплавов, образующих механические смеси из чистых компонентов
Диаграммы состояния — показатели фазового состояния сплавов в зависимости от температуры и концентрации компонентов. Диаграммы состояния строят для условий равновесия, т.е. такого состояния сплава, которое достигается при очень малых скоростях охлаждения или длительном нагреве. Диаграммы состояния сплавов в равновесном состоянии являются теоретическими диаграммами, так как истинное равновесие в практических условиях достигается редко.
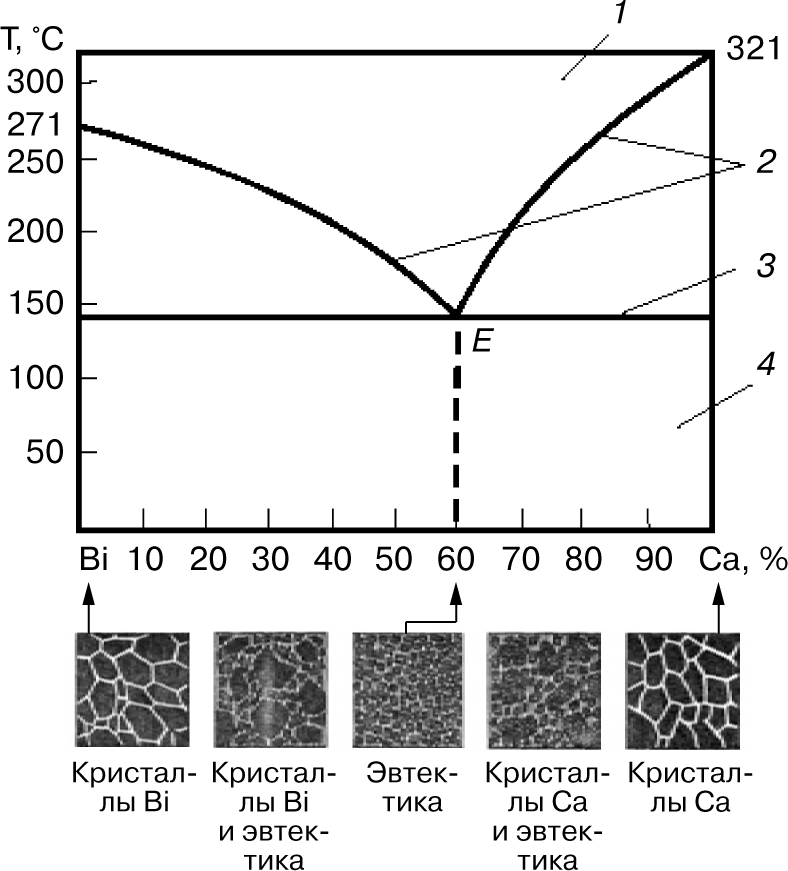
Рассмотрим диаграмму состояний одного из сплавов, образующих механические смеси из чистых компонентов, системы «висмут — кадмий» (рис. 4).
Область существования жидкого расплава ограничена сверху ломаной линией, соединяющей точки плавления висмута и кадмия через точку Е. В точке Е сплав (40% висмута и 60% кадмия) имеет одинаковые температуры ликвидуса и солидуса. Все остальные сплавы системы затвердевают и плавятся в пределах температурного интервала, который снизу ограничен горизонтальной линией солидуса. Сплав в точке Е имеет очень мелкие кристаллы висмута и кадмия, находящиеся в определенном взаимном расположении. Этот сплав называется эвтектикой, что в переводе с греческого означает легко плавящийся. Эвтектика — это механическая смесь двух (или более) видов кристаллов, одновременно кристаллизующихся из жидкого сплава. Твердые сплавы, лежащие левее эвтектической точки Е, и сплавы, содержащие до 40% висмута, называют доэвтектическими, а лежащие правее точки Е и содержащие более 40% висмута — заэвтектическими. Доэвтектические сплавы состоят из смеси кристаллов висмута и эвтектики (кристаллы висмута + кристаллы кадмия), а заэвтектические — из смеси кристаллов кадмия с эвтектикой.
По этому типу диаграммы состояния кристаллизуются также сплавы систем Zn—Sn, Pb—Ag, Ni—Cr, Cr—Mn, Cu—Bi, Al—Si.
4. Диаграмма состояния сплавов для случая ограниченной растворимости компонентов в твердом состоянии
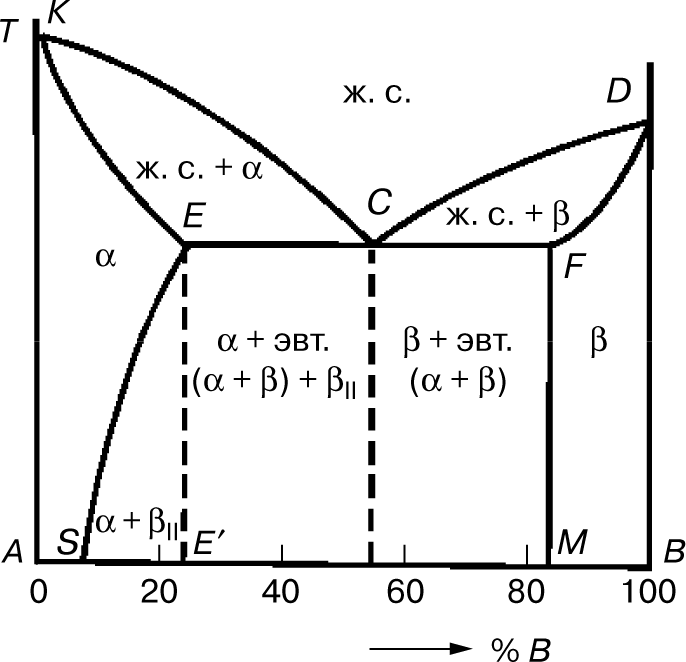
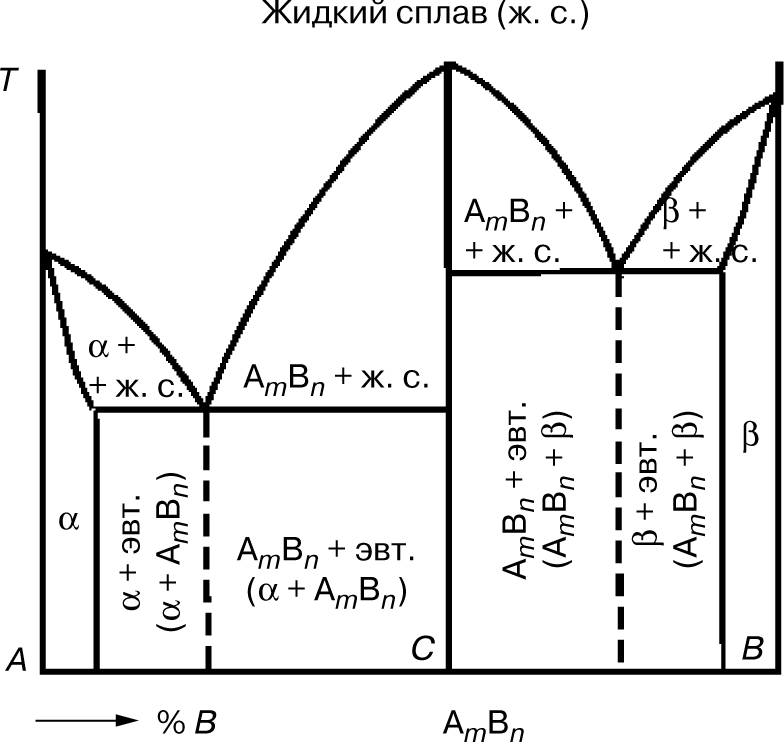
Эта диаграмма состояний содержит три фазы — жидкий раствор, твердый раствор компонента В в компоненте А () и твердый раствор компонента А в компоненте В (α). Линия диаграммы KCD — линия ликвидуса, линия KECFD — линия солидуса (рис. 5). Кристаллы α выделяются из жидкого сплава (ж. с.) по линии ликвидуса КС, а кристаллы β — по линии CD. Затвердевание сплавов происходит по линии солидуса КЕ с образованием кристаллов α и по линии DF — с образованием кристаллов β. Одновременная кристаллизация α- и β-фаз с образованием механической смеси кристаллов этих фаз происходит на линии солидуса ECF.
Сплав состава точки С после затвердевания называется эвтектическим, поскольку он состоит только из одной эвтектики α + β. Составы сплавов, лежащих левее эвтектической точки С на линии ЕС после затвердевания, называются доэвтектическими сплавами и имеют структуру α + эвтектика (α + β). Составы сплавов, лежащих правее точки С на линии CF после затвердевания, называются заэвтектическими сплавами и имеют структуру β + эвтектика (α + β).
Предельная растворимость компонента В в А характеризуется точкой Е, а А в В — точкой F. При кристаллизации сплавов, состав которых находится левее точки S (или правее точки М), при любой температуре в твердом состоянии все количество компонента В (или А) находится в твердом растворе, и структура таких сплавов состоит из зерен α (или β).
В сплавах, состав которых находится между точками S и Е′, образовавшихся при затвердевании, кристаллы α при понижении температуры ниже линии ES пересыщены компонентом В, и поэтому из них происходит выделение избыточных кристаллов. Это кристаллы β концентрации точки М, называемые вторичными (βII). Такие сплавы после полного охлаждения имеют структуру, состоящую из кристаллов α состава точки S и кристаллов βII, т.е. α + βII.
В сплавах состава линии ЕС, имеющих после затвердевания структуру α + эвтектика (α + β), из кристаллов α выделяются кристаллы β, и после полного охлаждения структура будет α + эвтектика (α + β) + βII.
5. Диаграмма состояния сплавов, образующих химические соединения
Сплавы, представляющие собой химическое соединение компонентов А и В, имеют сложную диаграмму состояния. Химическое соединение обозначают АmВn, т.е. в соединении на m атомов компонента А приходится n атомов компонента В. Химические соединения представляют собой сложное соединение с одной точкой плавления, в отличие от сплавов, у которых таких точек две.
В данной системе различают три фазы:
- жидкий раствор;
- твердый раствор компонента В в компоненте А (фаза α) (рис. 6);
- твердый раствор компонента А в компоненте В (фаза β).
Эта диаграмма как бы составлена из диаграмм для двух систем:
- компонент А — химическое соединение АmВn;
- компонент В — химическое соединение АmВn.
В сплавах левее точки С компонента А больше, чем входит
в химическое соединение АmВn. В этих сплавах левее точки промежуточного состояния образуется эвтектика α + АmВn. В сплавах правее точки С компонента В больше, чем может
входить в химическое соединение АmВn. В этих сплавах образуется эвтектика АmВn+ β.
Между составом и структурой сплава, определяемой типом, диаграммой состояния и свойствами сплава, существует определенная зависимость (правило Н.С. Курнакова). В механических смесях свойства (твердость Н, электропроводность Е, вязкость, хрупкость и др.) изменяются линейно. В твердых растворах свойства изменяются по криволинейной зависимости. В химических соединениях свойства выражаются ломаными линиями.
При концентрации, соответствующей химическому соединению, отмечается характерный перелом на кривой свойств, так как химические соединения обладают индивидуальными свойствами, отличающимися от свойств компонентов. По диаграммам можно определять и технологические свойства сплавов, что облегчает выбор материала для изготовления изделий.
6. Структурные составляющие железоуглеродистых сплавов
Основными компонентами, от которых зависят структура и свойства железоуглеродистых сплавов, являются железо и углерод. Чистое железо — металл серебристо-белого цвета; температура плавления 1539°С. Железо имеет две полиморфные модификации: α и γ. Модификация α существует при температурах ниже 91°С и выше 1392°С; γ-железо — при температуре 911…1392°С. В зависимости от температуры и концентрации углерода железоуглеродистые сплавы имеют следующие структурные составляющие:
- Феррит (Ф) — твердый раствор внедрения углерода в α-железе. Растворимость углерода в α-железе при комнатной температуре до 0,005%; наибольшая растворимость — 0,02% при 727°С. Феррит имеет незначительную твердость (НВ = 80…100) и прочность (σв = 250 МПа), но высокую пластичность (δ = 50%; Ψ = 80%), где σв — предел прочности; δ — относительное удлинение; Ψ — относительное сужение.
- Аустенит (А) — твердый раствор внедрения углерода в γ-железе. В железоуглеродистых сплавах он может существовать только при высоких температурах. Предельная растворимость углерода в γ-железе — 2,14% при температуре 1147°С и 0,8% — при 727°С. Аустенит имеет твердость НВ = 160…200 и весьма пластичен (δ = 40…50%).
- Цементит (Ц) — химическое соединение железа с углеродом (карбид железа Fe3C). В цементите содержится 6,67% углерода. Температура плавления цементита около 1600°С. Он очень тверд (НВ » 800), хрупок и практически не обладает пластичностью.
- Графит — это свободный углерод, мягкий (НВ = 3) и обладает низкой прочностью. В чугунах и графитизированной стали содержится в виде включений различных форм (пластинчатой, шаровидной и др.). С изменением формы графитовых включений меняются механические и технологические свойства сплава.
- Перлит (П) — механическая смесь феррита и цементита, содержащая 0,8% углерода. Перлит может быть пластинчатым и зернистым (глобулярным), что зависит от формы цементита и определяет механические свойства перлита. При комнатной температуре зернистый перлит имеет предел прочности σв ≈ 800 МПа; относительное удлинение δ =15%; твердость НВ = 160.
- Ледебурит (Л) — механическая смесь аустенита и цементита, содержащая 4,3% углерода. Ледебурит образуется при затвердевании жидкого расплава при 1147°С. Ледебурит имеет твердость НВ = 600…700 и большую хрупкость.
Помимо перечисленных структурных составляющих, в железоуглеродистых сплавах могут быть нежелательные неметаллические включения: окислы, нитриды, сульфиды, фосфиды — соединения с кислородом, азотом, серой и фосфором.
7. Диаграмма состояния «железо — цементит»
Диаграмма (рис. 7) показывает фазовый состав и структуру сплавов с концентрацией от чистого железа до цементита (6,67%). Сплавы с содержанием углерода 2,14% называют сталью, а от 2,14 до 6,67% — чугуном.
Первичная кристаллизация, т.е. затвердевание жидкого сплава, начинается при температурах, соответствующих линии ликвидуса. Точка А на этой диаграмме соответствует температуре плавления 1539°С (затвердевания) железа, точка D — температура плавления (затвердения) ~ 1600°С цементита.
Линия солидуса AEСF соответствует температурам конца затвердевания. При температурах, соответствующих линии АС, из жидкого сплава кристаллизуется аустенит, а линии CD — цементит, называемый первичным цементитом.
В точке С при 1147°С и содержании углерода 4,3% из жидкого сплава одновременно кристаллизуются аустенит (А) и цементит (Ц) (первичный), образуя эвтектику — ледебурит (Л).
При температурах, соответствующих линии солидуса АЕ, сплавы с содержанием углерода до 2,14% окончательно затвердевают с образованием аустенита. На линии солидуса ECF сплавы с содержанием углерода от 2,14 до 6,67% окончательно затвердевают с образованием эвтектики (ледебурита) и структур, образовавшихся ранее из жидкого сплава, а именно: в интервале 2,14…4,3%, С — аустенита, а в интервале 4,3…6,67% С — цементита первичного.
В результате первичной кристаллизации во всех сплавах с содержанием углерода до 2,14% (т.е. в сталях) образуется однофазная структура — аустенит. В сплавах с содержанием углерода более 2,14% (т.е. в чугунах) при первичной кристаллизации образуется эвтектика ледебурита.
Вторичная кристаллизация (превращение в твердом состоянии) происходит при температурах, соответствующих линиям GSE, PSK и GPQ. Превращения в твердом состоянии происходят вследствие перехода железа из одной аллотропической модификации в другую ( в ) и в связи с изменением растворимости углерода в аустените и феррите. С понижением температуры растворимость уменьшается. Избыток углерода выделяется из твердых растворов в виде цементита. В области диаграммы AGSE находится аустенит.
8. Диаграмма состояния «железо — графит»
Систему «железо — цементит» называют метастабильной, т.е. неустойчивой, так как при определенных условиях цементит распадается на аустенит и свободный углерод в виде графита. При очень медленном охлаждении из расплава в процессе кристаллизации углерод выделяется в виде графита. Систему «железо — графит» называют стабильной.
Процесс кристаллизации графита в сплавах железа с углеродом называют графитизацией. Она может происходить и в твердом состоянии, поскольку цементит при высоких температурах неустойчив. В этом случае графитизация происходит в несколько накладывающихся стадий:
- распад цементита и растворение атомов углерода в аустените;
- образование центров графитизации в аустените;
- диффузия атомов углерода в аустените к центрам графитизации;
- рост выделений графита.
На рис. 8 показана совмещенная диаграмма: сплошными линиями изображена метастабильная диаграмма «железо — цементит», штриховыми линиями — стабильная диаграмма. По диаграмме «железо — цементит» в области чугунов получают белые чугуны, а по диаграмме «железо — графит» — серые чугуны.
На диаграмме «железо — графит» горизонтальные линии E′C′F ′ и P ′S′K′ лежат несколько выше, а наклонные линии C′D′ и E′S′ — несколько левее соответствующих линий диаграммы «железо — цементит». На диаграмме «железо — графит» линия AC′D′ — линия ликвидуса. При охлаждении расплава по ветви АС выделяется аустенит, а по ветви C′D′ — графит (первичный).
На линии солидуса E′C′F′ при температуре 1153°С образуется эвтектика, состоящая из графита и аустенита. Ее называют графитной эвтектикой. При понижении температуры в системе «железо — графит» из аустенита будет выделяться графит, который называют вторичным. На линии P′S′K′ при температуре 738°С аустенит, содержащий 0,7% углерода (точка S′), распадается, образуя эвтектоид, состоящий из феррита и графита. Этот эвтектоид называют графитным. После полного охлаждения структура состоит из феррита и графита (эвтектического, вторичного и эвтектоидного).
Структура металлов и сплавов
1. Развитие металлографии
Металлография, или металловедение,— наука, занимающаяся изучением свойств, состава и структуры металлов и их сплавов. Металловедение кзк наука создана русскими учеными-металлур-гами. Выдающийся русский ученый-металлург Павел Петрович Аносов первый заложил основы металловедения. Работая на Златоустовском оружейном заводе на Урале, он впервые в мире в 1831 г. применил микроскоп для исследования строения стали на полированных травленых шлифах. П. П. Аносов положил начало современному процессу производства стали, называемому мартеновским; он осуществил метод передела чугуна в сталь (в 1873 г.) без добавки железа, опередив этим более чем на 30 лет братьев Мартен.
П. П. Аносов проделал большую научную работу по изучению влияния углерода на свойства стали. Его научные работы оказали большое влияние на развитие производства качественных сталей и на улучшение методов их термической обработки. Дальнейшую работу по изучению свойств металлов и металлических сплавов в зависимости от изменения их состава и строения продолжал гениальный русский ученый Дмитрий Константинович Чернов. Работая инженером на Обуховском сталелитейном заводе в Петербурге, он сделал открытие, которое имело исключительно важное значение для дальнейшего развития металловедения. Д. К. Чернов в результате многочисленных наблюдений над поведением стальных поковок в процессе тепловой обработки установил, что при определенных температурах в стали, находящейся в твердом состоянии, происходит перестройка ее частиц, благодаря чему изменяется структура стали и ее свойства.
Открытия, сделанные Д. К. Черновым, были опубликованы в 1868 г., в связи с чем он получил всемирную известность и заслуженно считается основоположником металлографии. Благодаря его открытиям стала возможной правильная, научно обоснованная термическая обработка металлов и металлических сплавов.
Последователи и ученики Д. К. Чернова — Н. С. Курнаков, А. А. Байков и др.— в дальнейшем способствовали своими научными работами и исследованиями еще большему развитию отечественного металловедения.
2. Кристаллическая структура металлов
Существуют тела аморфные и кристаллические. Структура аморфных тел состоит из хаотически расположенных атомов. К таким телам относятся, например, стекло, янтарь, смолы и т. п. Кристаллические тела отличаются от аморфных тем, что атомы в них располагаются в геометрически правильном порядке. Металлы и металлические сплавы относятся к типичным кристаллическим телам. Атомы, располагаясь в металлах в строго определенном геометрическом порядке, образуют кристаллическую решетку (рис. 11). В зависимости от расположения атомов образуются различные виды кристаллических решеток.
В металлах чаще всего встречаются кристаллические решетки в виде центрированного куба, гранецентрированного куба и гексагональной призмы.
Такие, например, металлы как хром, ванадий, вольфрам, молибден и ряд других, имеют кристаллическую решетку в виде центрированного куоа (рис. 12, а), в которой восемь атомов располагаются в углах куба и один — в центре куба.
Алюминий, медь, свинец, никель, серебро и др. имеют кристаллическую решетку — гранецентрированную, т. е. в виде куба с центрированными гранями (рис. 12,6). В такой решетке в каждом углу куба находится по одному атому и по одному атому в центре каждой грани. Всего, следовательно, 14 атомов.
Кристаллическую решетку в зиде гексагональной призмы (рис. 12, е) имеют такие металлы, как, например, цинк, титан, марганец. Расположение атомов в кристаллической решетке типа гексагональной призмы следующее: в каждом углу призмы находится по одному атому, в центре верхнего основания один атом, в центре нижнего основания один атом и три атома в среднем сечении.
Рис. 11. Кристаллическая решетка
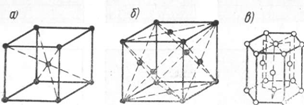
Рис. 12. Виды кристаллических решеток:
а — куб центрированный; б — куб гранецентрированный; в — гексагональная призма
Расстояния между атомами в кристаллической решетке чрезвычайно малы и измеряются специальной единицей длины, которая носит название ангстрема (по имени ученого). Один ангстрем равен одной стомиллионной Юле сантиметра.
В расплавленном жидком металле атомы находятся в движении.‘Движение их носит хаотический характер, но по мере того, как температура металла понижается и приближается к критической, т. е. к температуре затвердевания, в нем образуются так называемые центры кристаллизации, или зародыши кристаллизации. Центры кристаллизации представляют собой чрезвычайно мелкие группы атомов, которые группируются в геометрически правильном порядке.
Образующиеся зародыши кристаллизации очень неустойчивы, и многие из них снова растворяются. Практическими наблюдениями установлено, что зародыши кристаллизации приобретают устойчивость и начинают расти тогда, когда жидкий металл переохладится до некоторой температуры. Кривая охлаждения чистого металла дает наглядное представление о том, как протекает процесс кристаллизации.
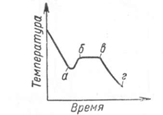
Рис. 13. Кривая охлаждения чистого металла
В переохлажденном металле (рис. 13, а) процесс кристаллизации начинает протекать быстрее. После начала интенсивной кристаллизации температура переохлажденного металла поднимается до температуры его затвердевания (б) за счет выделения скрытой теплоты кристаллизации.
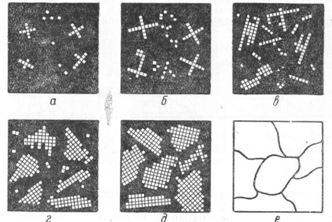
Рис. 14. Схема образования зерен
В течение всего процесса кристаллизации температура металла остается постоянной (б, в). После того как металл перейдет из жидкого состояния в твердое, начинается понижение его температуры до температуры окружающей среды (г). В процессе кристаллизации происходит рост зародышей за счет атомов из окружающей их жидкости, которые располагаются в кристаллической решетке в строго определенном порядке (рис. 14, а, б). Вначале рост зародышей кристаллизации протекает свободно, и они имеют правильную внешнюю геометрическую форму. Но так как одновременно образуется много зародышей, то наступает такой момент, когда они начинают встречаться друг с другом (рис. 14, в, г, д). После такого столкновения рост их становится возможным только в тех направлениях, где нет помех. Это приводит к тому, что внешняя геометрическая форма кристаллов металла становится неправильной, вследствие чего они обычно называются зернами металла (рис. 14, е).
3. Изменение структуры в твердых металлах (явление аллотропии)
Структура некоторых металлов, находящихся в твердом состоянии, может при известной температуре испытывать превращения, которые представляют собой перегруппировку атомов и переход из одного вида кристаллической решетки в другой. Такое явление носит название аллотропии металлов. Различные кристаллические формы, в которые кристаллизуется один и тот же твердый металл при определенных температурах, называются аллотропическими модификациями. Аллотропические модификации обозначаются греческими буквами. Переход из одной модификации в другую происходит при определенной, постоянной температуре и сопровождается поглощением тепла (при нагреве) или выделением тепла (при охлаждении) и образованием новой кристаллической решетки.
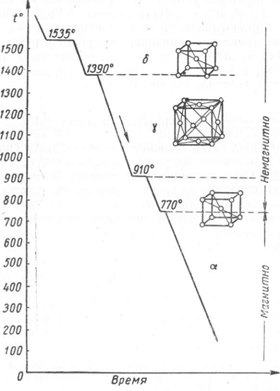
Рис. 15. Кривая охлаждения чистого железа
Чистое железо существует в нескольких модификациях. На кривой охлаждения чистого железа (рис. 15) видно, при каких температурах происходят аллотропические превращения железа. До температуры 910° железо имеет кристаллическую решетку в виде центрированного куба и называется альфа-железо a-Fe. .причем до 770° a-Fe магнитно, а выше 770° немагнитно. При температуре 910° кристаллическая решетка a-Fe меняется и переходит в гранецентрированную; эта модификация называется гамма-железо y-Fe и устойчива до температуры 1390°, при которой вновь превращается в решетку центрированного куба. Новая модификация называется дельта-железо 8-Fe. Аллотропические превращения имеют очень важное значение, так как металлы, испытывающие такие превращения, могут подвергаться термической обработке. Аллотропическим превращениям подвержены, кроме железа, и некоторые другие металлы, как, например, титан, марганец, кобальт, цирконий, олово.
4. Строение сплавов
Сплавом называется сложное вещество, полученное сплавлением двух или нескольких элементов. Элементы, составляющие сплав, называются компонентами сплава. В жидком состоянии сплав представляет раствор, в котором атомы одного компонента равномерно распределяются между атомами других компонентов, благодаря чему жидкий раствор обладает одинаковыми свойствами в любой своей части, как бы она ни была мала. Такие вещества называются однородными. Свойства любого жидкого раствора отличаются от свойств его компонентов, но каждый компонент оказывает влияние на характер свойств раствора. При тщательном исследовании жидких растворов оказывается, что физические, электрические и другие свойства этих растворов резко отличаются от свойств их компонентов и могут изменяться в зависимости от процентного содержания компонентов, т. е. от концентрации‘раствора.
Концентрацией раствора называется отношение веса растворимого вещества к весу всего раствора. Концентрация выражается обычно в процентах. При переходе сплава из жидкого состояния в твердое могут получаться различные виды взаимодействия компонентов. Основными видами взаимодействия компонентов являются: механическая смесь, химическое соединение и твердый раствор.
Механическая смесь представляет такой вид взаимодействия компонентов, при котором в процессе кристаллизации компоненты сплава не вступают в химическую реакцию и не растворяются один в другом, а сохраняют свои кристаллические решетки. Следовательно, структура сплава, являющегося механической смесью двух каких-либо компонентов, например, свинца и сурьмы, будет состоять из чрезвычайно мелких кристаллов свинца и кристаллов сурьмы.
В случае химического соединения взаимодействие компонентов сплава характеризуется образованием совершенно новой кристаллической решетки, не похожей на кристаллические решетки компонентов; при этом соотношение компонентов всегда будет строго определенным.
Твердый раствор отличается от механической смеси и химического соединения тем, что в нем сохраняется кристаллическая решетка металла-растворителя, в которой размещаются атомы всех компонентов сплава. Металл, кристаллическая решетка которого сохраняется после образования твердого раствора, называется растворителем. Твердые растворы могут быть двух видов: твердый раствор внедрения и твердый раствор замещения. В твердом растворе внедрения атомы растворенного вещества располагаются между атомами растворителя (рис. 16, а). В твердом растворе замещения атомы растворенного вещества частично замещают собой атомы растворителя в его кристаллической решетке (рис. 16,6).
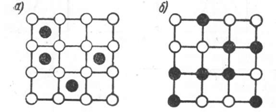
Рис. 16. Решетка твердого раствора:
а — внедрения; б — замещения
5. Диаграмма состояния сплавов (свинец — сурьма) и ее построение
Для изучения сплавов обычно пользуются диаграммами состояния сплавов. Диаграммы состояния сплавов заменяют собой все записи и кривые охлаждения сплава, полученные в результате Многочисленных наблюдений. Такая диаграмма дает возможность видеть все изменения строения сплава и его свойств, происходящие в зависимости от изменения концентрации и температуры. Любая точка диаграммы дает характеристику сплаза определенной концентрации и структуры. По диаграмме состояния сплавов можно определить температуру плавления и температуру затвердевания данного сплава при любой концентрации. Знание этих фактов способствует правильному выбору температур нагрева и охлаждения при термической и химико-термической обработках различных сплавов.
Для того чтобы уяснить, как строится диаграмма состояния сплавов, рассмотрим построение такой диаграммы для сплавов свинца и сурьмы. Возьмем чистые металлы свинец и сурьму и несколько их сплавов с содержанием сурьмы 5%, 10%, 13%, 20%, 40% и 80%.
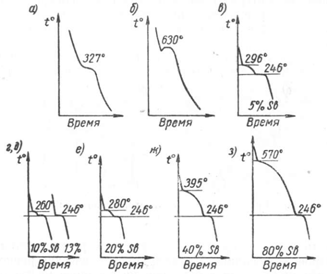
Рис. 17. Кривые охлаждения свинца, сурьмы и различных сплавов свинца с сурьмой
Чтобы определить критические точки взятых металлов и их сплавов, нагреем поочередно каждый металл и сплав до полного расплавления и с помощью термопары или пирометра внимательно проследим за процессом их охлаждения и построим кривые охлаждения (рис. 17). В процессе охлаждения расплавленного чистого свинца будут происходить следующие явления.
При температурах, лежащих выше 327°, свинец находится в жидком состоянии (рис. 17, а); при температуре 327° наблюдается процесс кристаллизации свинца с задержкой падения температуры до полного завершения кристаллизации; после окончания кристаллизации происходит дальнейшее охлаждение твердого свинца до температуры окружающей среды.
Аналогичные явления наблюдаются и в процессе охлаждения расплавленной чистой сурьмы (рис. 17, б), с той лишь разницей, что кристаллизация сурьмы начинается при температуре 630°.
Сплав, состоящий из 95% свинца и 5% сурьмы (рис. 17,в), имеет кривую охлаждения с двумя критическими точками, поэтому он затвердевает в интервале температур 296—246°. При температуре 296° из жидкого сплава начинают выделяться первые кристаллы чистого свинца. Кривая в этой точке имеет перегиб. По мере дальнейшего понижения температуры количество кристаллов свинца будет все более увеличиваться, а остающаяся часть жидкого сплава будет обогащаться сурьмой. Такое явление продолжается до тех пор, пока концентрация жидкого сплава не достигнет 13% сурьмы и 87% свинца; при такой концентрации весь сплав, оставшийся еще жидким, затвердеет при температуре 246°. Сплав, состоящий из 30% свинца и 10% сурьмы (рис. 17, г), затвердеет также в интервале температур 260—246°. При температуре 260° начинается выделение из жидкого сплава кристаллов свинца. При достижении концентрации жидкого сплава до 13% сурьмы и 87% свинца происходит затвердевание сплава при температуре 246° (рис. 17, д). Следовательно, при охлаждении вышеприведенных сплавов, прежде чем будет достигнута критическая температура 246°, весь лишний, избыточный сверх 87% свинец выделяется из жидкого сплава в виде кристаллов. По достижении состава 87% свинца и 13% сурьмы сплав переходит в твердое состояние при температуре 246°. Структура затвердевшего сплава такой концентрации состоит из правильно чередующихся между собой частиц свинца и сурьмы. Такая механическая смесь называется эвтектической. Все сплавы свинца с сурьмой, содержащие сурьмы меньше, чем 13%, будут всегда иметь избыток свинца и при охлаждении стремятся выделить этот избыток в виде твердых кристаллов свинца, чтобы при температуре 246° образовать эвтектику. Тогда, очевидно, в твердом состоянии такие сплавы будут иметь структуру свинец + эвтектика. Сплав, состоящий из 87% свинца и 13% сурьмы, имеет кривую охлаждения (рис. 17, д) с одной критической точкой. Этот сплав находится в жидком состоянии при температурах, лежащих выше 246°. При температуре 246° сплав полностью переходит в твердое состояние.
Такая структура твердого сплава представляет собой чистую эвтектику. Сплав, состоящий из 80% свинца и 20% сурьмы (рис. 17, е), при температурах выше 280° находится в жидком состоянии. При охлаждении сплава до температуры 280° из него начинают выделяться кристаллы твердой сурьмы, причем этот процесс будет продолжаться до тех пор, пока оставшийся жидкий сплав не примет эвтектического состава. При температуре 246° весь сплав затвердевает. Структура затвердевшего сплава будет состоять из кристаллов сурьмы и эвтектики. Сплав, состоящий из 60о/0 свинца и 40о/0 сурьмы (рис. 17, ж), выше температуры 395° Находится в жидком состоянии. При температуре 395° начинается процесс кристаллизации с выделением из жидкого раствора кристаллов избыточной сурьмы. По достижении эвтектического состава- (87о/0 свинца и 13% сурьмы) при температуре 246° весь сплав переходит в твердое состояние, образуя структуру, состоящую из кристаллов сурьмы и эвтектики.
Сплав, состоящий из 20% свинца и 80% сурьмы (рис. 17, з), находится в жидком состоянии выше температуры 570°. При температуре 570° начинается процесс выделения из жидкого сплава кристаллов избыточной сурьмы. По достижении эвтектического состава при температуре 246° весь сплав переходит в твердое состояние. Структура сплава состоит из кристаллов сурьмы и эвтектики. Приведенные наблюдения показывают, что все сплавы свинца с сурьмой, в которых содержание свинца меньше 87о/0, содержат избыток сурьмы и при охлаждении будут стремиться выделить этот избыток в процессе кристаллизации в виде твердых кристаллов сурьмы, чтобы при температуре 246° образовать эвтектику. Чем больше будет сурьмы в сплаве, тем при более высокой температуре начнет выделяться из него при охлаждении избыточная (против 13<>/0) сурьма. Сплавы свинца с сурьмой при наличии в них избыточной сурьмы образуют в твердом состоянии структуру, состоящую из кристаллов сурьмы и эвтектики.
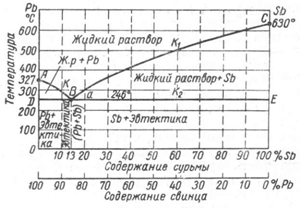
Рис. 18. Диаграмма состояния сплавов системы свинец—сурьма
Кривые охлаждения сплавов свинца и сурьмы с различным процентным содержанием Компонентов можно объединить в одну диаграмму состояния сплавов свинца с сурьмой. Для этого на горизонтальной оси (рис. 18) отложим содержание свинца и сурьмы в испытанных сплавах. Через точки, соответствующие 100% сурьмы и 100% свинца, проведем вертикальные прямые линии, на которых отложим температуры от 0 до 700°. Через точки, отвечающие составам испытанных сплавов, проведем пунктиром вертикальные линии. После этого переносим с кривых охлаждения критические точки на вертикальные линии диаграммы. Критическую точку чистого свинца (327°) обозначим буквой А, а критическую точку чистой сурьмы (630°) буквой С. Как известно из предыдущих наблюдений, каждый сплав имеет две критические точки, кроме эвтектического сплава. Критическую температуру эвтектического сплава обозначим буквой В. Соединим точки А и С плавными кривыми с точкой В так, чтобы кривые проходили через все верхние критические точки. Через все нижние критические точки проведем прямую линию, которая пройдет и через точку В, и обозначим ее левый конец буквой D, а правый конец буквой Е. Верхние критические точки являются точками начала затвердевания сплавов, а нижние критические точки — точками конца затвердевания сплавов. Линия ABC диаграммы называется линией ликвидуса (от латинского слова жидкий). Выше линии ABC все сплавы свинца и сурьмы находятся в жидком состоянии. Линия DBE называется линией солидуса (от латинского слова «твердый»). Ниже линии DBE все сплавы свинца с сурьмой находятся в твердом состоянии, причем ниже линии DB они будут состоять из кристаллов свинца и эвтектики и называются доэвтектическими, ниже точки В — из чистой эвтектики (так называемые эвтектические) и ниже линии BE — из кристаллов сурьмы и эвтектики (заэвтектические).
6. Структурные составляющие железоуглеродистых сплавов
Существуют различные структурные составляющие железоуглеродистых сплавов. Они имеют следующие названия: феррит, цементит, аустенит.
Ферритом называется химически чистое железо, а также твердый раствор углерода в железе. Растворимость углерода в железе чрезвычайно мала и обычно составляет 0,006—0,04%. Феррит устойчив до температуры 910°. Он обладает небольшой твердостью и малой прочностью. Твердость феррита зависит от размера зерна; пластичность феррита высокая.
Цементитом называется химическое соединение железа с углеродом. Цементит содержит 6,67% углерода (по весу) и представляет собой очень твердое и хрупкое кристаллическое вещество, которое при нагревании до высоких температур распадается на феррит и свободный углерод (углерод отжига). В белом чугуне содержится большое количество цементита. Цементит оказывает значительное влияние на механические свойства стали.
Механическая смесь феррита и цементита образует структуру стали, называемую перлитом. Перлит бывает двух видов: пластинчатый, или полосчатый, и зернистый. Пластинчатый перлит имеет вид перемежающихся ‘очень мелких пластинок феррита и цементита. Путем нагрева до определенных температур можно изменить строение пластинчатого перлита и получить так назы-ваёмый зернистый перлит, в котором цементит находится в виде круглых зерен, расположенных среди феррита.
Зернистый перлит обладает лучшими механическими свойствами, чем пластинчатый. Перлит по своим механическим свойствам занимает промежуточное положение между ферритом и цементитом. Сталь с содержанием углерода 0,83% имеет чистую перлитную структуру.
Аустенит представляет собой твердый раствор внедрения углерода в железе. Растворимость углерода в у-железе может достигать 1,7%. В обыкновенной углеродистой стали аустенит устойчив до температуры 723°. Ниже 723° он распадается на феррит и цементит. При температурах, лежащих ниже 723°, аустенит может сохраняться только в высоколегированных марганцовистых, хромоникелевых или никелевых сталях.
Эвтектическая смесь аустенита и цементита образует структуру стали, называемую ледебуритом. Ледебурит образуется при затвердевании железоуглеродистого сплава с содержанием углерода 4,3% при температуре 1130°. Ледебурит остается устойчивым до температуры 723°. Ниже этой температуры ледебурит изменяет свою структуру, так как входящий в его состав аустенит распадается на перлит, вследствие чего ледебурит при температурах ниже 723° будет состоять из перлита и цементита.
7. Диаграмма состояния железоуглеродистых сплавов
Стали и чугуны представляют собой сложные сплавы, содержащие, кроме железа и углерода, другие элементы — кремний, марганец, фосфор и серу, а также цветные металлы (в легированных сталях и чугунах). Главнейшей составной частью, определяющей характер и свойства железоуглеродистого сплава, является углерод. Структура и свойства стали и чугуна изменяются лишь при условии нагрева их до критических температур, зависящих от содержания углерода в этих сплавах. Критические температуры железоуглеродистых сплавов с разным содержанием углерода могут быть нанесены на специальную диаграмму, называемую диаграммой состояния сплавов системы железо — углерод.
Такая диаграмма (рис. 19) позволяет определить для каждого сплава стали и чугуна температуру его плавления, все превращения, испытываемые сплавом при охлаждении и нагревании, и структуру сплава при любой температуре. По горизонтальной оси диаграммы откладывается содержание углерода в процентах, а по вертикальной оси — температура. Каждая точка на диаграмме представляет собой определенный сплав при определенной температуре. Выше линии ACD все сплавы находятся в жидком состоянии. Линия АCD есть линия ликвидуса.
Чистое железо плавится и затвердевает в одной точке при температуре 1535°. Все остальные сплавы железа с углеродом плавятся и затвердевают в некотором промежутке температур, постепенно изменяющемся. Сплавы, содержащие от 0 до 4,39% углерода, начинают затвердевать по линии АС, выделяя твердые кристаллы аустенита. Сплавы, содержащие более 4,3% углерода, начинают затвердевать по линии CD, выделяя твердые кристаллы цементита Fe3C. Сплав, содержащий 4,3% углерода, затвердевает полностью в точке С, выделяя одновременно кристаллы аустенита и цементита, в результате чего образуется эвтектика, называемая ледебуритом. Линия AECF есть линия солидуса. Ниже этой линии все сплавы находятся в твердом состоянии. Область диаграммы, ограниченная линиями АС, СЕ, ЕА, представляет сплавы, состоящие из твердых кристаллов аустенита и жидкого сплава; область диаграммы, ограниченная линиями DC. CF, FD, включает сплавы, состоящие из твердых кристаллов цементита и жидкого сплава.
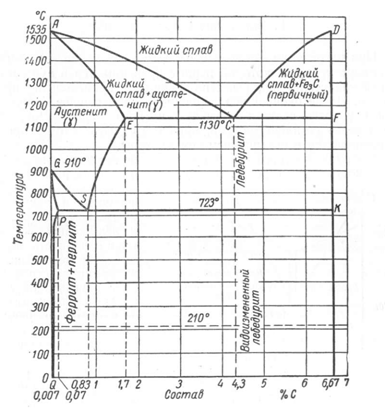
Рис. 19. Диаграмма состояния системы железо — углерод
Сплавы, находящиеся в области диаграммы, ограниченной линиями АЕ, ES, SG, состоят из аустенита. По линии ES начинает выделяться из аустенита цементит. Ниже линии PSK весь оставшийся аустенит распадается в точке 5 на феррит и цементит, образуя механическую смесь, называемую перлитом, причем в точке 5 сплав содержит углерода 0,83°/о. Такой сплав называется эвтектоидным. Линия GPQ показывает предел насыщения а-железа углеродом.
Стали с содержанием углерода от 0 до 0,83% называются до-эвтектоидными, стали с содержанием углерода 0,83°/о —эвтекго-идными и с содержанием углерода от 0,83 до 1,7% — заэвтекто-идными.
Чугун с содержанием углерода от 1,7 до 4,3% носит название доэвтектического чугуна, чугун при содержании углерода 4,3% называется эвтектическим, а с содержанием углерода от 4,3 до 6,67%—заэвтектическим.
8. Изменение структуры стали
При нагревании стали выше критической точки Aci (рис, 20) (температура, при которой перлит превращается в аустенит) в структуре стали, как известно, начинают происходить превращения. После окончания превращения дальнейшее нагревание или выдержка ведут к росту аустенитного зерна. Рост зерна происходит самопроизвольно, причем скорость этого процесса увеличивается с повышением температуры.
Рост аустенитного зерна протекает по-разному и зависит от склонности зерна к росту. В зависимости от этого различают стали наследственно крупнозернистые и наследственно мелкозернистые. Под наследственностью понимают склонность зерна к росту. Наследственно крупнозернистые стали обладают повышенной склонностью аустенитного зерна к росту, а наследственно мелкозернистые малой склонностью к росту.
Изменение размеров зерна при нагревании указанных сталей видно из рис. 20. При нагревании стали выше критической точки Асх размер зерна стали резко уменьшается. При дальнейшем нагревании аустенитное зерно в наследственно мелкозернистых сталях не растет до температур порядка 950—-1000°, после чего начинается быстрый рост зерна.
В наследственно крупнозернистых сталях зерно начинает расти сразу после перехода через критическую точку Ас. Размер аустенитного зерна имеет большое значение для получения окончательных результатов при термической обработке сталей. Превращение перлита ib аустенит сопровождается измельчением зерна. Образующееся при этом превращении зерно очень мелко. При обратном превращении аустенитного зерна в перлитное изменений в его размере почти не происходит (рис. 21). Следовательно, размер перлитного зерна зависит главным образом от размера аустенигного зерна. А так как аустенитное зерно растет только при нагревании, то, нагревая сталь до определенных температур, можно получить окончательно требуемый размер зерна стали. Размер действительного зерна стали, т. е. зерна, полученного в результате той или иной термической обработки, оказывает большое влияние на механические свойства стали.
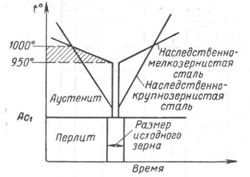
Рис. 20. Схема роста зерна в наследственно-мелкозернистой и в наследственно-крупнозернистой стали
Крупнозернистая сталь хорошо прокаливается и обрабатывается режущим инструментом, но в то же время она более склонна к закалочным деформациям, к образованию в ней трещин. Мелкозернистые стали обладают большей ударной вязкостью в сравнении с крупнозернистыми сталями, но меньшей прокаливае-мостью. Для изготовления изделий, которым требуется вязкая сердцевина при твердой поверхности, применяется мелкозернистая сталь.
При медленном охлаждении нагретой стали до аус-тенитного состояния аусте-нит превращается в перлит, феррит и цементит. При больших скоростях охлаждения — от 40 до 200° в секунду и более — в результате распада аустенита получаются структуры стали: сорбит, троостит и мартенсит.
Сорбит бывает двух видов: сорбит закалки и сорбит отпуска. Сорбит закалки состоит из чередующихся пластинок феррита и цементита, но пластинки цементита в нем значительно тоньше, чем в перлите. Сорбит тверже перлита, но обладает меньшей вязкостью. Сорбит отпуска получается в результате распада мартенсита в стали при отпуске ее в интервале температур 500—600°. В сорбите отпуска частицы цементита имеют шарообразную форму. Троостит, так же как и сорбит, различается двух видов: троостит закалки и ‘троостит отпуска.. Троостит представляет механическую смесь пластинок феррита и цементита, но более тонких, чем в сорбите. Троостит обладает большей твердостью по сравнению с сорбитом, но меньшей вязкостью. Троостит отпуска является продуктом распада мартенсита при отпуске его в интервале температур 350—450°.
Мартенсит представляет собой твердый раствор внедрения углерода. Кристаллы мартенсита имеют иглообразную форму. Он обладает высокой твердостью и хорошо сопротивляется износу; пластичность и вязкость его низкие.
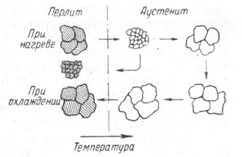
Рис. 21. Изменение размера зерна в процессе перекристаллизации