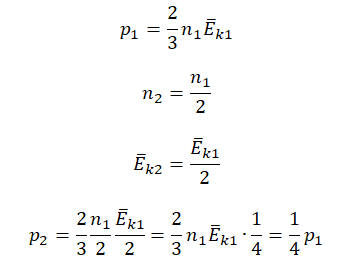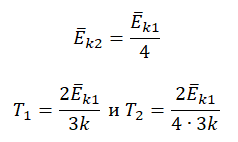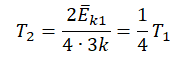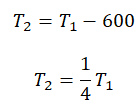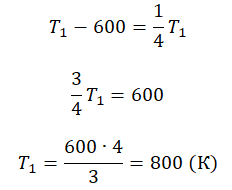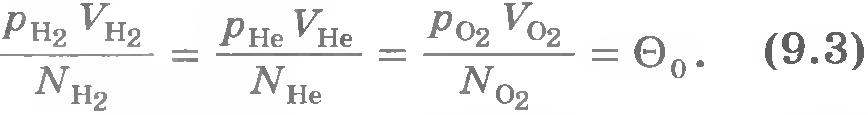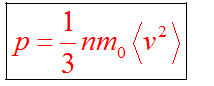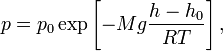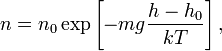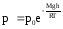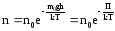Идеальный газ — газ, удовлетворяющий трем условиям:
- Молекулы — материальные точки.
- Потенциальная энергия взаимодействия молекул пренебрежительно мала.
- Столкновения между молекулами являются абсолютно упругими.
Реальный газ с малой плотностью можно считать идеальным газом.
Измерение температуры
Температуру можно измерять по шкале Цельсия и шкале Кельвина. По шкале Цельсия за нуль принимается температура, при которой происходит плавление льда. По шкале Кельвина за нуль принимается абсолютный нуль — температура, при котором давление идеального газа равно нулю, и его объем тоже равен нулю.
Обозначение температуры
- По шкале Цельсия — t. Единица измерения — 1 градус Цельсия (1 oC).
- По шкале Кельвина — T. Единица измерения — 1 Кельвин (1 К).
Цена деления обеих шкал составляет 1 градус. Поэтому изменение температуры в градусах Цельсия равно изменению температуры в Кельвинах:
∆t = ∆T
При решении задач в МКТ используют значения температуры по шкале Кельвина. Если в условиях задачи температура задается в градусах Цельсия, нужно их перевести в Кельвины. Это можно сделать по формуле:
T = t + 273
Если особо важна точность, следует использовать более точную формулу:
T = t + 273,15
Пример №1. Температура воды равна oC. Определить температуру воды в Кельвинах.
T = t + 273 = 2 + 273 = 275 (К)
Основное уравнение МКТ идеального газа
Давление идеального газа обусловлено беспорядочным движением молекул, которые сталкиваются друг с другом и со стенками сосуда. Основное уравнение МКТ идеального газа связывает давление и другие макропараметры (объем, температуру и массу) с микропараметрами (массой молекул, скоростью молекул и кинетической энергией).
Основное уравнение МКТ
Давление идеального газа пропорционально произведению концентрации молекул на среднюю кинетическую энергию поступательного движения молекулы.
p=23n−Ek
p — давление идеального газа, n — концентрация молекул газа, −Ek — средняя кинетическая энергия поступательного движения молекул.
Выражая физические величины друг через друга, можно получить следующие способы записи основного уравнения МКТ идеального газа:
|
p=13m0n−v2 |
m0— масса одной молекулы газа; n — концентрация молекул газа; −v2 — среднее значение квадрата скорости молекул газа. Среднее значение квадрата скорости не следует путать со среднеквадратичной скоростью v, которая равна корню из среднего значения квадрата скорости: v=√−v2 |
|
p=13ρ−v2 |
ρ — плотность газа |
|
p=nkT |
k — постоянная Больцмана (k = 1,38∙10–3 Дж/кг) T — температура газа по шкале Кельвина |
Пример №2. Во сколько раз уменьшится давление идеального одноатомного газа, если среднюю кинетическую энергию теплового движения молекул и концентрацию уменьшить в 2 раза?
Согласно основному уравнению МКТ идеального газа, давление прямо пропорционально произведению средней кинетической энергии теплового движения молекул и концентрации его молекул. Следовательно, если каждая из этих величин уменьшится в 2 раза, то давление уменьшится в 4 раза:
Следствия из основного уравнения МКТ идеального газа
Через основное уравнение МКТ идеального газа можно выразить скорость движения молекул (частиц газа):
v=√3kTm0=√3RTM
R — универсальная газовая постоянная, равная произведения постоянной Авогадро на постоянную Больцмана:
R=NAk=8,31 Дж/К·моль
Температура — мера кинетической энергии молекул идеального газа:
−Ek=32kT
T=2−Ek3k
Полная энергия поступательного движения молекул газа определяется формулой:
E=N−Ek
Пример №3. При уменьшении абсолютной температуры на 600 К средняя кинетическая энергия теплового движения молекул неона уменьшилась в 4 раза. Какова начальная температура газа?
Запишем формулу, связывающую температуру со средней кинетической энергией теплового движения молекул, для обоих случаев, с учетом что:
Следовательно:
Составим систему уравнений:
Отсюда:
Задание EF19012

Алгоритм решения
1.Указать, в каких координатах построен график.
2.На основании основного уравнения МКТ идеального газа и уравнения Менделеева — Клапейрона выяснить, как меняются указанные физические величины во время процессов 1–2 и 2–3.
Решение
График построен в координатах (V;Ek). Процесс 1–2 представляет собой прямую линию, исходящую из начала координат. Это значит, что при увеличении объема растет средняя кинетическая энергия молекул. Но из основного уравнения МКТ идеального газа следует, что мерой кинетической энергии молекул является температура:
T=2−Ek3
Следовательно, когда кинетическая энергия молекул растет, температура тоже растет.
Запишем уравнение Менделеева — Клапейрона:
pV=νRT
Так как количество вещества одинаковое для обоих состояния 1 и 2, запишем:
νR=p1V1T1=p2V2T2
Мы уже выяснили, что объем и температура увеличиваются пропорционально. Следовательно, давление в состояниях 1 и 2 равны. Поэтому процесс 1–2 является изобарным, давление во время него не меняется.
Процесс 2–3 имеет график в виде прямой линии, перпендикулярной кинетической энергии. Так как температуры прямо пропорциональна кинетической энергии, она остается постоянной вместе с этой энергией. Следовательно, процесс 2–3 является изотермическим, температура во время него не меняется. Мы видим, что объем при этом процессе уменьшается. Но так как объем и давление — обратно пропорциональные величины, то давление на участке 2–3 увеличивается.
Ответ:
• Участок 1–2 — изобарный процесс. Температура увеличивается, давление постоянно.
• Участок 2–3 — изотермический процесс. Температура постоянно, давление увеличивается.
pазбирался: Алиса Никитина | обсудить разбор
Задание EF17560
Первоначальное давление газа в сосуде равнялось р1. Увеличив объём сосуда, концентрацию молекул газа уменьшили в 3 раза, и одновременно в 2 раза увеличили среднюю энергию хаотичного движения молекул газа. В результате этого давление р2 газа в сосуде стало равным
Ответ:
а) 13p1
б) 2p1
в) 23p1
г) 43p1
Алгоритм решения
1.Записать исходные данные.
2.Записать основное уравнение МКТ идеального газа.
3.Составить уравнения для состояний 1 и 2.
4.Выразить искомую величину.
Решение
Исходные данные:
• Начальное давление: p0.
• Начальная концентрация молекул: n1 = 3n.
• Конечная концентрация молекул: n2 = n.
• Начальная средняя энергия хаотичного движения молекул: Ek1 = Ek.
• Конечная средняя энергия хаотичного движения молекул: Ek2 = 2Ek.
Основное уравнение МКТ:
p=23n−Ek
Составим уравнения для начального и конечного состояний:
p1=23n1−Ek1=233n−Ek=2n−Ek
p2=23n2−Ek2=23n2−Ek=43n−Ek
Отсюда:
n−Ek=p12=3p24
p2=4p16=23p1
Ответ: в
pазбирался: Алиса Никитина | обсудить разбор
Задание EF18416
Цилиндрический сосуд разделён неподвижной теплоизолирующей перегородкой. В одной части сосуда находится кислород, в другой – водород, концентрации газов одинаковы. Давление кислорода в 2 раза больше давления водорода. Чему равно отношение средней кинетической энергии молекул кислорода к средней кинетической энергии молекул водорода?
Алгоритм решения
1.Записать исходные данные.
2.Записать основное уравнение МКТ идеального газа.
3.Составить уравнения для обоих газов.
4.Найти отношение средней кинетической энергии молекул кислорода к средней кинетической энергии молекул водорода.
Решение
Анализируя условия задачи, можно выделить следующие данные:
• Концентрации кислорода и водорода в сосуде равны. Следовательно, n1 = n2 = n.
• Давление кислорода вдвое выше давления водорода. Следовательно, p1 = 2p, а p2 = p.
Запишем основное уравнение идеального газа:
p=23n−Ek
Применим его для обоих газов и получим:
p1=23n1−Ek1 или 2p=23n−Ek1
p2=23n2−Ek2 или p=23n−Ek2
Выразим среднюю кинетическую энергию молекул газа из каждого уравнения:
−Ek1=3pn
−Ek2=3p2n
Поделим уравнения друг на друга и получим:
−Ek1−Ek2=3pn·2n3p=2
Ответ: 2
pазбирался: Алиса Никитина | обсудить разбор
Задание EF18824
В одном сосуде находится аргон, а в другом – неон. Средние кинетические энергии теплового движения молекул газов одинаковы. Давление аргона в 2 раза больше давления неона. Чему равно отношение концентрации молекул аргона к концентрации молекул неона?
Алгоритм решения
1.Записать исходные данные.
2.Записать основное уравнение МКТ идеального газа.
3.Составить уравнения для обоих газов.
4.Найти отношение концентрации молекул аргона к концентрации молекул неона.
Решение
Анализируя условия задачи, можно выделить следующие данные:
• Средние кинетические энергии теплового движения молекул газов одинаковы. Следовательно, −Ek1=−Ek2=−Ek.
• Давление аргона в 2 раза больше давления неона. Следовательно, p1 = 2p, а p2 = p.
Запишем основное уравнение идеального газа:
p=23n−Ek
Применим его для обоих газов и получим:
p1=23n1−Ek1 или 2p=23n1−Ek
p2=23n2−Ek2 или p=23n2−Ek
Выразим концентрации молекул газа из каждого уравнения:
n1=3p−Ek
n2=3p2−Ek
Поделим уравнения друг на друга и получим:
n1n2=3p−Ek·2−Ek3p=2
Ответ: 2
pазбирался: Алиса Никитина | обсудить разбор
Алиса Никитина | Просмотров: 10.9k
Гипермаркет знаний>>Физика и астрономия>>Физика 10 класс>>Физика: Определение температуры
При тепловом равновесии средняя кинетическая энергия поступательного движения молекул всех газов одинакова. В этом вы скоро убедитесь.
Средняя кинетическая энергия молекул газа при тепловом равновесии. Возьмем сосуд, разделенный пополам перегородкой, проводящей тепло. В одну половину сосуда поместим кислород, а в другую — водород, имеющие разную температуру. Спустя некоторое время газы будут иметь одинаковую температуру, не зависящую от рода газа, т. е. будут находиться в состоянии теплового равновесия. Для определения температуры выясним, какая физическая величина в молекулярно-кинетической теории обладает таким же свойством.
Из курса физики 7 класса известно, что, чем быстрее движутся молекулы, тем выше температура тела. При нагревании газа в замкнутом сосуде давление газа возрастает. Согласно же основному уравнению молекулярно-кинетической теории (8.15) давление газа p прямо пропорционально средней кинетической энергии поступательного движения молекул: . При тепловом равновесии, если давление газа данной массы и его объем фиксированы, средняя кинетическая энергия молекул газа должна иметь строго определенное значение, как и температура.
Можно предположить, что при тепловом равновесии именно средние кинетические энергии молекул всех газов одинаковы. Конечно, это пока только предположение. Его нужно экспериментально проверить. Практически такую проверку произвести непосредственно невозможно, так как измерить среднюю кинетическую энергию молекул очень трудно. Но с помощью основного уравнения молекулярно-кинетической теории ее можно выразить через макроскопические параметры.
Так как концентрация молекул газа , то из уравнения (8.15) получаем
, или
Давление p и объем V измеряются непосредственно. Число молекул N можно определить, зная массу газа m, постоянную Авогадро NA и молярную массу M. Согласно формуле (8.8)
Если кинетическая энергия действительно одинакова для всех газов в состоянии теплового равновесия, то и величина p должна быть тоже одинаковой для всех газов. Только опыт может подтвердить или опровергнуть данное предположение.
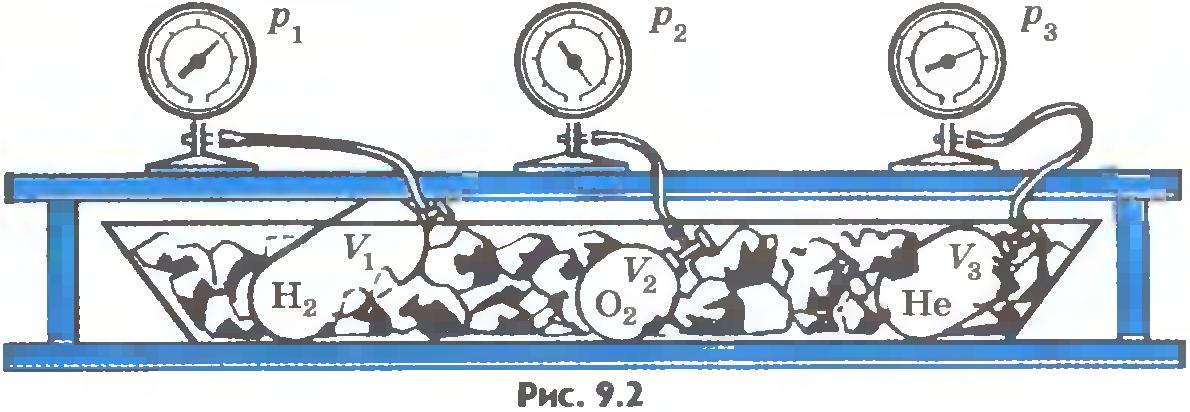
Газы в состоянии теплового равновесия. Опыт можно осуществить так. Возьмем несколько сосудов, заполненных различными газами, например водородом, гелием и кислородом. Сосуды имеют определенные объемы и снабжены манометрами. Это позволяет измерить давление в каждом сосуде. Массы газов известны, тем самым известно число молекул в каждом сосуде.
Приведем газы в состояние теплового равновесия. Для этого поместим их в тающий лед и подождем, пока не установится тепловое равновесие и давление газов перестанет меняться (рис.9.2). После этого можно утверждать, что все газы имеют одинаковую температуру 0°С. Давления газов p, их объемы V и число молекул N различны. Найдем отношение для водорода. Если, к примеру, водород, количество вещества которого равно 1 моль, занимает объем VH2=0,1 м3, то при температуре 0°С давление оказывается равным pH2=2,265•104 Па. Отсюда
Такое же значение отношения произведения давления газа на его объем к числу молекул получается и для всех других газов при температуре тающего льда. Обозначим это отношение через . Тогда
Таким образом, наше предположение оказалось верным.
Правда, соотношение (9.3) не является абсолютно точным. При давлениях в сотни атмосфер, когда газы становятся весьма плотными, отношение перестает быть строго определенным, не зависящим от занимаемых газами объемов. Оно выполняется для газов, когда их можно считать идеальными.
Если же сосуды с газами поместить в кипящую воду при нормальном атмосферном давлении, то упомянутое отношение по-прежнему будет одним и тем же для всех газов, но больше, чем предыдущее. Как показывает опыт,
Определение температуры. Можно, следовательно, утверждать, что величина растет с повышением температуры. Более того,
ни от чего, кроме температуры, не зависит. Ведь для идеальных газов
не зависит ни от рода газа, ни от его объема или давления, а также от числа частиц в сосуде и формы самого сосуда. Этот опытный факт позволяет рассматривать величину
как естественную меру температуры, определяемую через другие макроскопические параметры газа. В принципе можно было бы считать температурой и саму величину
и измерять температуру в энергетических единицах — джоулях. Однако, во-первых, это неудобно для практического использования (температуре 100°С соответствовала бы очень малая величина — порядка 10-21 Дж), а во-вторых, и это главное, уже давно принято выражать температуру в градусах.
Мы нашли способ получать значения температуры, не зависящие от свойств газов, которые при этом используются. Пока что температуру мы выразили в энергетических единицах.
???
1. На каком основании можно предполагать существование связи между температурой и кинетической энергией молекул?
2. Как связаны объем, давление и число молекул различных газов в состоянии теплового равновесия?
Г.Я.Мякишев, Б.Б.Буховцев, Н.Н.Сотский, Физика 10 класс
Материалы по физике, задание и ответы по классам, планы конспектов уроков по физике для 10 класса
Содержание урокаконспект урока
опорный каркас
презентация урока
акселеративные методы
интерактивные технологии Практика
задачи и упражнения
самопроверка
практикумы, тренинги, кейсы, квесты
домашние задания
дискуссионные вопросы
риторические вопросы от учеников Иллюстрации
аудио-, видеоклипы и мультимедиа
фотографии, картинки
графики, таблицы, схемы
юмор, анекдоты, приколы, комиксы
притчи, поговорки, кроссворды, цитаты Дополнения
рефераты
статьи
фишки для любознательных
шпаргалки
учебники основные и дополнительные
словарь терминов
прочие Совершенствование учебников и уроков
исправление ошибок в учебнике
обновление фрагмента в учебнике
элементы новаторства на уроке
замена устаревших знаний новыми Только для учителей
идеальные уроки
календарный план на год
методические рекомендации
программы
обсуждения Интегрированные уроки
Если у вас есть исправления или предложения к данному уроку, напишите нам.
Если вы хотите увидеть другие корректировки и пожелания к урокам, смотрите здесь — Образовательный форум.
Авторські права | Privacy Policy |FAQ | Партнери | Контакти | Кейс-уроки
© Автор системы образования 7W и Гипермаркета Знаний — Владимир Спиваковский
При использовании материалов ресурса
ссылка на edufuture.biz обязательна (для интернет ресурсов —
гиперссылка).
edufuture.biz 2008-© Все права защищены.
Сайт edufuture.biz является порталом, в котором не предусмотрены темы политики, наркомании, алкоголизма, курения и других «взрослых» тем.
Разработка — Гипермаркет знаний 2008-
Ждем Ваши замечания и предложения на email: 
По вопросам рекламы и спонсорства пишите на email: 
Видеоурок: Средняя кинетическая энергия молекул многоатомного газа
Лекция: Связь температуры газа со средней кинетической энергией поступательного теплового движения его части

Температура напрямую зависит от скорости движения молекул газа. Из механики: чем больше скорость материальной точки, тем больше её кинетическая энергия. Обобщив эти два понятия, можно сделать вывод, что
кинетическая энергия структурных единиц газа напрямую зависит от температуры.
Данное утверждение подтверждает следующая формула:
Е — средняя кинетическая энергия поступательного движения частиц
k — постоянная Больцмана
Т — абсолютная температура

Постоянная Больцмана — это константа, определяющая связь средней кинетической энергии структурных единиц вещества с температурой.
Уравнение состояния идеального газа
Автор статьи — профессиональный репетитор, автор учебных пособий для подготовки к ЕГЭ Игорь Вячеславович Яковлев
Темы кодификатора ЕГЭ: модель идеального газа, связь между давлением и средней кинетической энергией теплового движения молекул идеального газа, связь температуры газа со средней кинетической энергией его частиц, уравнение  , уравнение Менделеева—Клапейрона.
, уравнение Менделеева—Клапейрона.
Из трёх агрегатных состояний вещества наиболее простым для изучения является газообразное. В достаточно разреженных газах расстояния между молекулами намного больше размеров самих молекул (тогда как в жидкостях и твёрдых телах молекулы «упакованы» весьма плотно).Поэтому силы взаимодействия между молекулами таких газов очень малы.
Для описания разреженных газов в физике используется модель идеального газа. В рамках этой модели делаются следующие допущения.
1. Пренебрегаем размерами молекул. Иными словами, молекулы газа считаются материальными точками.
2. Пренебрегаем взаимодействием молекул на расстоянии.
3. Соударения молекул друг с другом и со стенками сосуда считаем абсолютно упругими.
Таким образом, идеальный газ — это газ, частицы которого являются не взаимодействующими на расстоянии материальными точками и испытывают абсолютно упругие соударения друг с другом и со стенками сосуда.
Средняя кинетическая энергия частиц газа
Оказывается, что ключевую роль в описании идеального газа играет средняя кинетическая энергия его частиц.
Частицы газа двигаются с разными скоростями. Пусть в газе содержится частиц, скорости которых равны
. Масса каждой частицы равна
. Кинетические энергии частиц:
Средняя кинетическая энергия частиц газа это среднее арифметическое их кинетических энергий:
Последний множитель — это средний квадрат скорости, обозначаемый просто :
Тогда формула для средней кинетической энергии приобретает привычный вид:
(1)
Корень из среднего квадрата скорости называется средней квадратической скоростью:
Основное уравнение МКТ идеального газа
Cвязь между давлением газа и средней кинетической энергией его частиц называется основным уравнением молекулярно-кинетической теории идеального газа. Эта связь выводится из законов механики и имеет вид:
(2)
где — концентрация газа (число частиц в единице объёма). С учётом (1) имеем также:
(3)
Что такое ? Произведение массы частицы на число частиц в единице объёма даёт массу единицы объёма, то есть плотность:
. Получаем третью разновидность основного уравнения:
(4)
Энергия частиц и температура газа
Можно показать, что при установлении теплового равновесия между двумя газами выравниваются средние кинетические энергии их частиц. Но мы знаем, что при этом становятся равны и температуры газов. Следовательно, температура газа — это мера средней кинетической энергии его частиц.
Собственно, ничто не мешает попросту отождествить эти величины и сказать, что температура газа — это средняя кинетическая энергия его молекул. В продвинутых курсах теоретической физики так и поступают. Определённая таким образом температура измеряется в энергетических единицах — джоулях.
Но для практических задач удобнее иметь дело с привычными кельвинами. Связь средней кинетической энергии частиц и абсолютной температуры газа даётся формулой:
(5)
где Дж/К — постоянная Больцмана.
Благодарим за то, что пользуйтесь нашими публикациями.
Информация на странице «Уравнение состояния идеального газа» подготовлена нашими редакторами специально, чтобы помочь вам в освоении предмета и подготовке к экзаменам.
Чтобы успешно сдать нужные и поступить в высшее учебное заведение или техникум нужно использовать все инструменты: учеба, контрольные, олимпиады, онлайн-лекции, видеоуроки, сборники заданий.
Также вы можете воспользоваться другими материалами из данного раздела.
Публикация обновлена:
08.05.2023
Основное уравнение молекулярно-кинетической теории идеального газа
Основное уравнение
молекулярно-кинетической теории
идеального газаустанавливает
связь между макроскопической величиной
— давлением, которое может быть измерено,
например манометром, и микроскопическими
величинами, характеризующими молекулу:
где
р — давление, m0—
масса молекулы, п — концентрация (число
молекул в единице объема), v2—
средний квадрат скорости молекул.
Если через Е
обозначить среднюю кинетическую энергию
поступательного движения молекулы
можно записать:
Давление идеального
газа пропорционально концентрации
молекул и средней кинетической энергии
их поступательного движения.
уравнение состояния
идеального газа (его
также называют уравнением
Клапейрона-Менделеева):
PV = nRT
где n –
число молей газа;
P – давление газа
(например, в атм;
V – объем газа (в
литрах);
T – температура
газа (в кельвинах);
R – газовая постоянная
(0,0821 л·атм/моль·K).
ИЗОПРОЦЕССЫ
Изопроцессы —
равновесные процессы, в которых один
из основных параметров сохраняется.
ИЗОБАРНЫЙ ПРОЦЕСС-
термодинамический
процесс,
происходящий в системе при постоянном
давлении
и постоянной массе идеального газа.
()
Для
изобарного процесса в идеальном газе
справедлив закон Гей-Люссака:
при
постоянном давлении объем данной массы
газа прямо пропорционален его
термодинамической температуре:или
.
Работа
газа при изобарном расширении:
.
Изменение
внутренней энергии:Количество
полученного тепла в соответствии с
первым началом термодинамики:.
Молярная
теплоемкость при изобарном процессе:.
ИЗОХОРНЫЙ ПРОЦЕСС
()-термодинамический
процесс,
который происходит при постоянном
объёме.
Для осуществления изохорного процесса
в газе или жидкости достаточно нагревать
(охлаждать) вещество в сосуде, который
не изменяет своего объёма.
Изохорный
процесс в идеальном газе описывается
законом Шарля:
при постоянном объеме
давление данной массы газа прямо
пропорционально его термодинамической
температуре:
или
.
Работа
газа при изохорном процессе равна
нулю: .
Все
полученное тепло идет на изменение
внутренней энергии в соответствии с
первым началом термодинамики:
.
Молярная
теплоемкость при изохорном процессе:.
ИЗОТЕРМИЧЕСКИЙ
ПРОЦЕСС ()-термодинамический
процесс,
происходящий в физической системе при
постоянной температуре.
Изотермический
процесс в идеальном газе подчиняется
закону Бойля — Мариотта:
для данной
массы газа при неизменной температуре
произведение значений давления и объема
есть величина постоянная:
или
.
Работа газа при
изотермическом расширении:
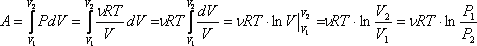
Изменение
внутренней энергии при изотермическом
процессе равно нулю:.
Все
полученное тепло идет на совершение
работы в соответствии с первым началом
термодинамики:.
-
Основное уравнение
МКТ. Статистическое толкование
температуры. Барометрическая формула.
Распределения Максвелла и Больцмана.
Основное уравнение
мкт имеет вид
Определение температуры в статистической физике в статистической физике температура определяется как производная от энергии системы по её энтропии:
,
где S — энтропия,
E — энергия термодинамической
системы. Введённая таким образом величина
T является одинаковой для различных тел
при термодинамическом равновесии. При
контакте двух тел тело с большим значением
T будет отдавать энергию другому.
Барометрическая
формула —
зависимость давления или плотности
газа от высоты в поле тяжести.
Для идеального
газа,
имеющего постоянную температуру
и
находящегося в однородном поле тяжести
(во всех точках его объёмаускорение
свободного падения
одинаково),
барометрическая формула имеет следующий
вид:
где
—
давление газа в слое, расположенном на
высоте,
—
давление на нулевом уровне (),
—молярная
масса
газа,
—газовая
постоянная,
—абсолютная
температура.
Из барометрической формулы следует,
что концентрация молекул
(или
плотность газа) убывает с высотой по
тому же закону:
где
—
масса молекулы газа,—постоянная
Больцмана.
Данное выражение
называется барометрической формулой.
Она позволяет найти атмосферное давление
в зависимости от высоты, или высоту,
если известно давление.
Закон Больцмана
о распределении частиц во внешнем
потенциальном поле.
Если
воспользоваться выражением р = nkT,
то можно привести барометрическую
формулу к виду:
здесь n
– концентрация молекул на высоте h,
n0
– то же у поверхности Земли. Так как М
= m0NA
, где m0
– масса
одной молекулы, а R
= k
NA,
то мы получим П = m0gh
– это потенциальная энергия одной
молекулы в поле тяготения. Поскольку
kT~‹εпост›,
то концентрация молекул на определенной
высоте зависит от соотношения П и ‹εпост›
Полученное выражение
называется распределением Больцмана
для внешнего потенциального поля. Из
него следует, что при постоянной
температуре плотность газа (с которой
связана концентрация) больше там, где
меньше потенциальная энергия его
молекул.
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #