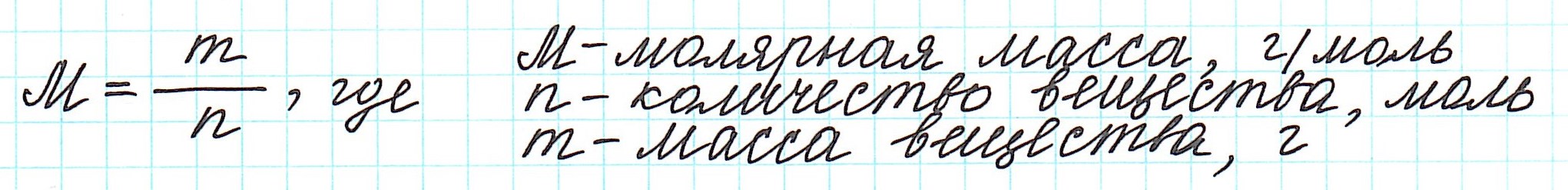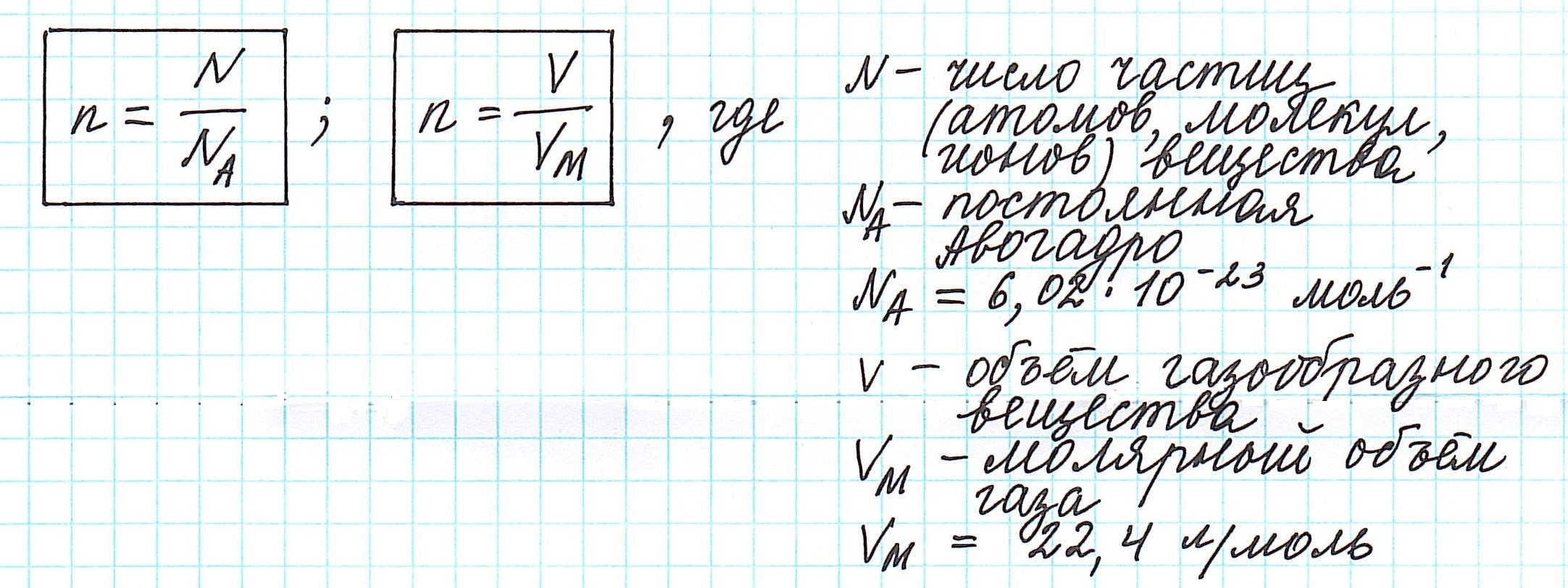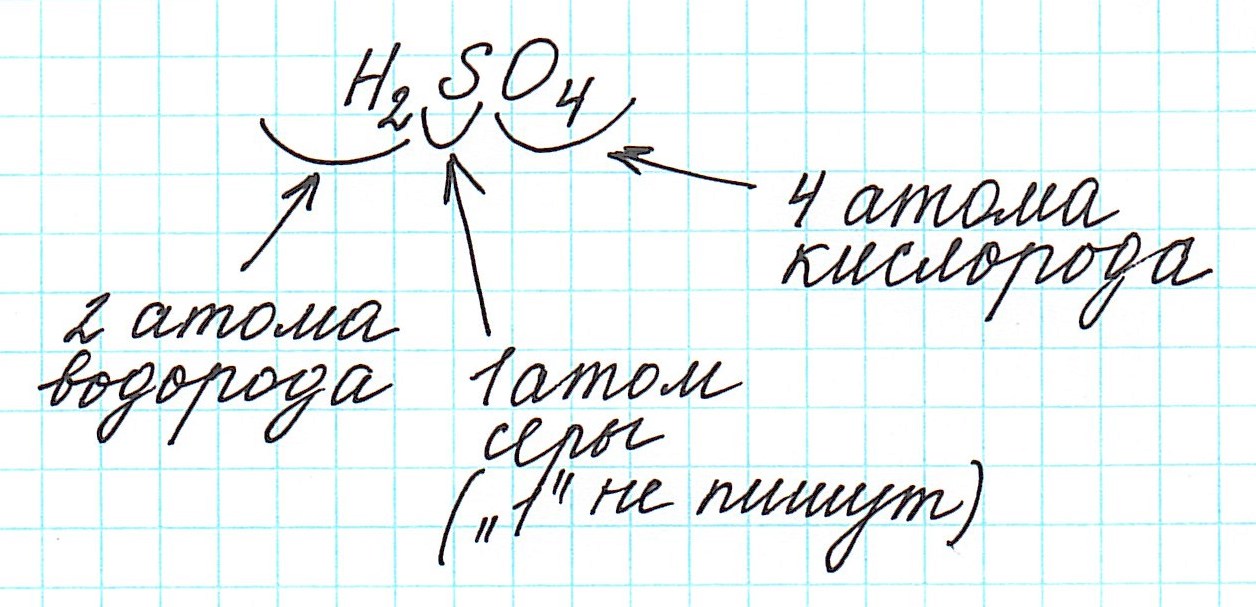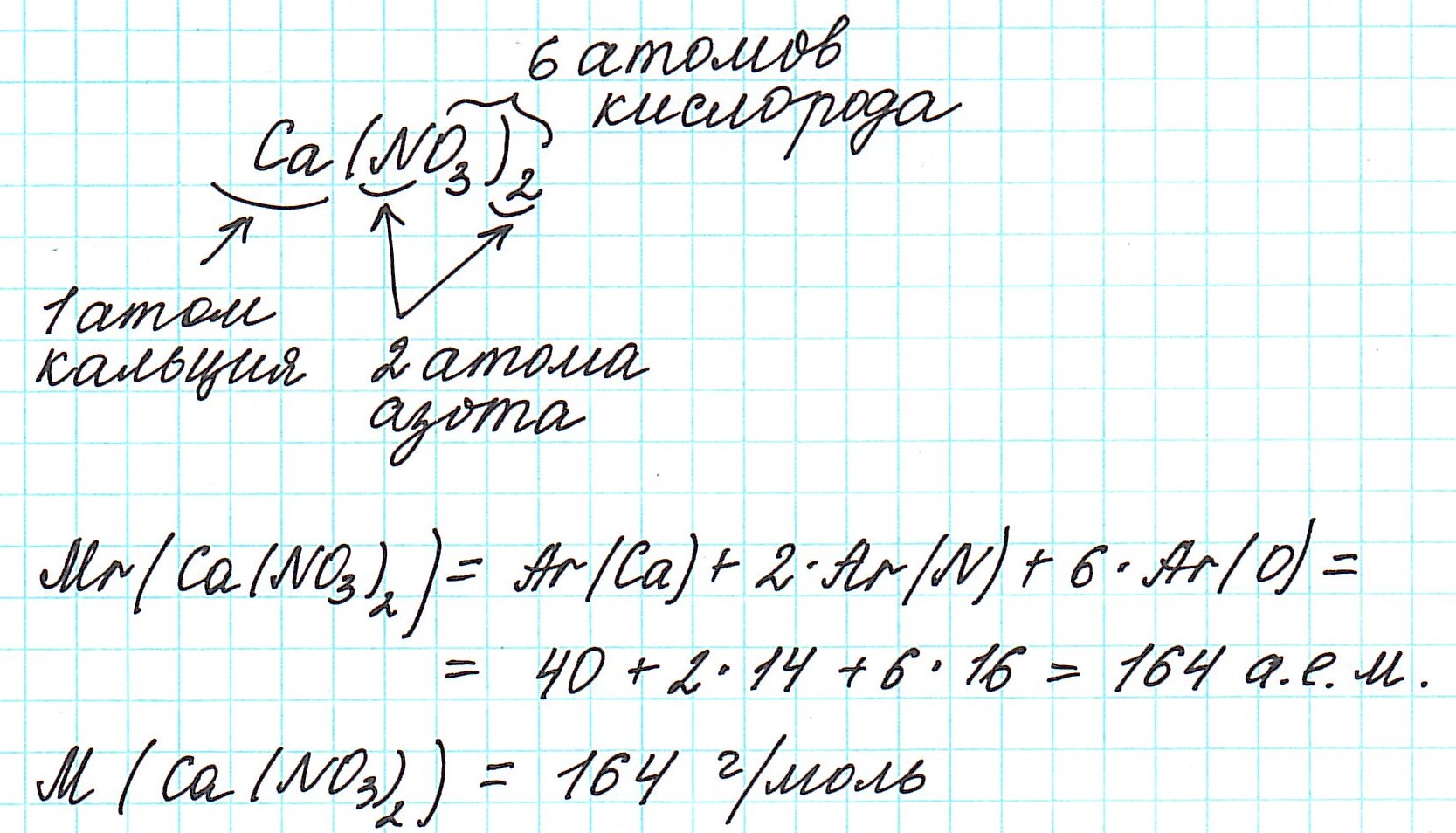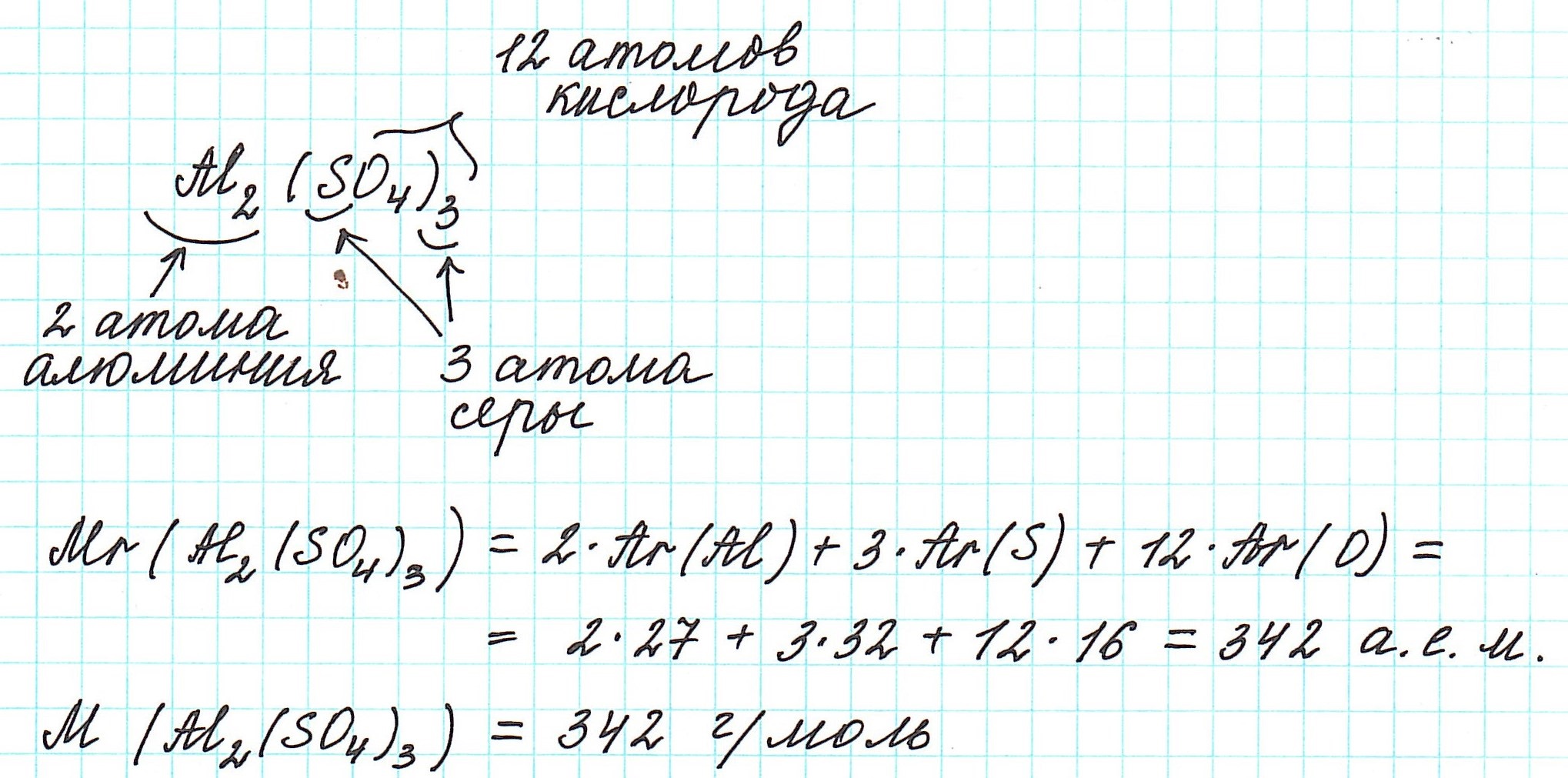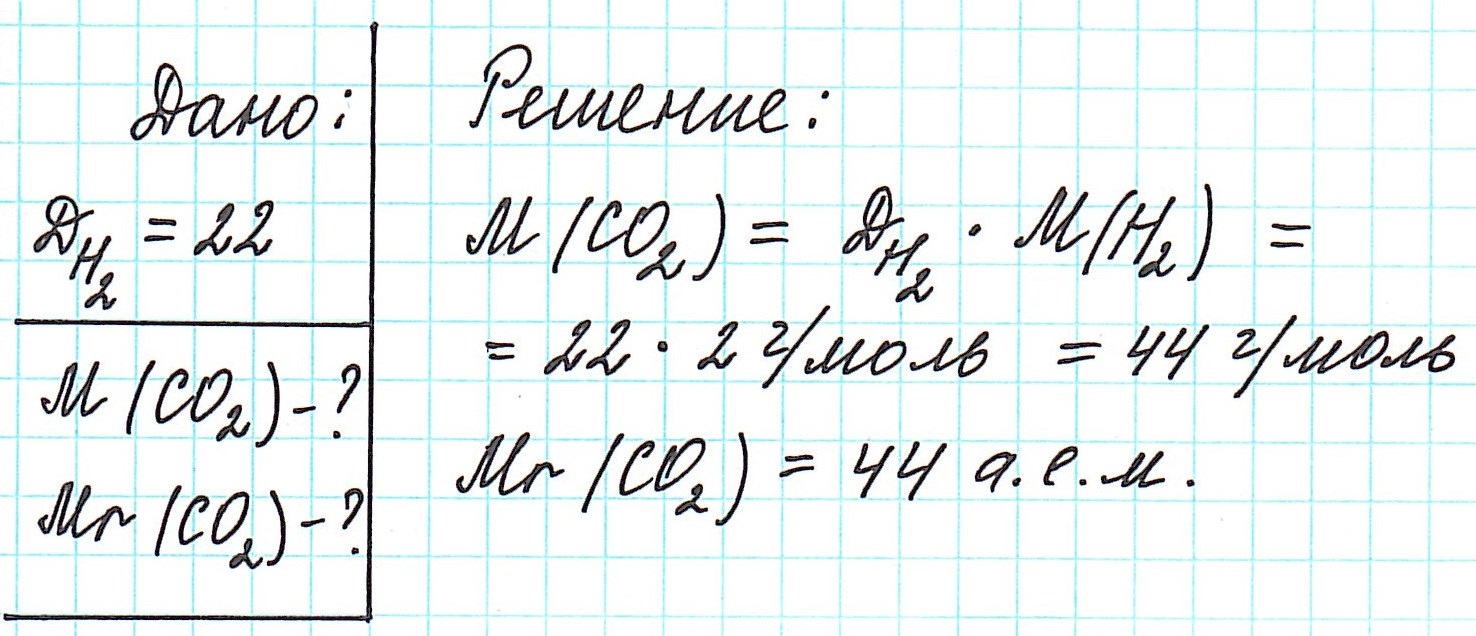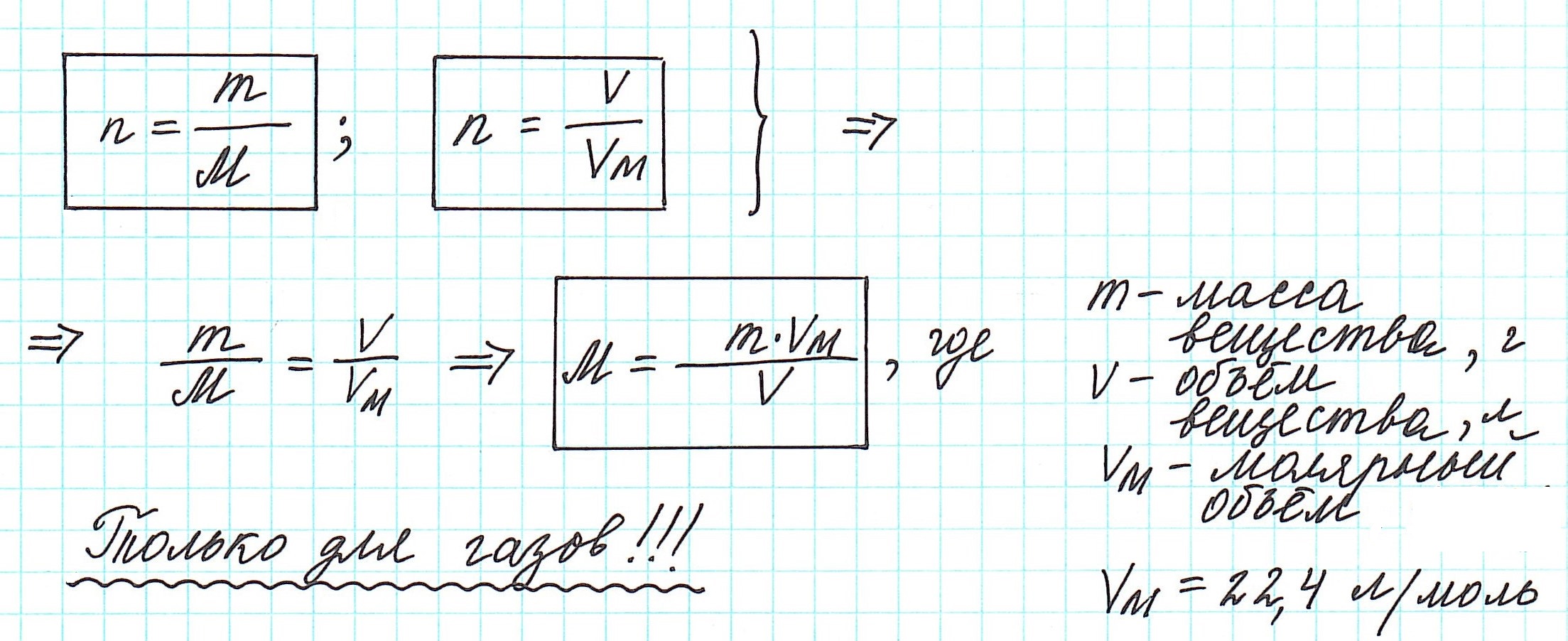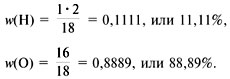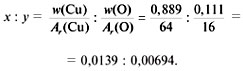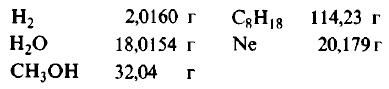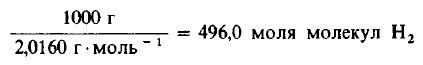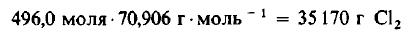В этой статье мы коснемся нескольких краеугольных понятий в химии, без которых совершенно невозможно
решение задач. Старайтесь понять смысл физических величин, чтобы усвоить эту тему.
Я постараюсь приводить как можно больше примеров по ходу этой статьи, в ходе изучения вы увидите множество примеров
по данной теме.

Относительная атомная масса — Ar
Представляет собой массу атома, выраженную в атомных единицах массы. Относительные атомные массы указаны в периодической
таблице Д.И. Менделеева. Так, один атом водорода имеет атомную массу = 1, кислород = 16, кальций = 40.
Относительная молекулярная масса — Mr
Относительная молекулярная масса складывается из суммы относительных атомных масс всех атомов, входящих в состав вещества.
В качестве примера найдем относительные молекулярные массы кислорода, воды, перманганата калия и медного купороса:
Mr (O2) = (2 × Ar(O)) = 2 × 16 = 32
Mr (H2O) = (2 × Ar(H)) + Ar(O) = (2 × 1) + 16 = 18
Mr (KMnO4) = Ar(K) + Ar(Mn) + (4 × Ar(O)) = 39 + 55 + (4 * 16) = 158
Mr (CuSO4*5H2O) = Ar(Cu) + Ar(S) + (4 × Ar(O)) + (5 × ((Ar(H) × 2) +
Ar(O))) = 64 + 32 + (4 × 16) + (5 × ((1 × 2) + 16)) = 160 + 5 * 18 = 250
Моль и число Авогадро
Моль — единица количества вещества (в системе единиц СИ), определяемая как количество вещества, содержащее столько же структурных единиц
этого вещества (молекул, атомов, ионов) сколько содержится в 12 г изотопа 12C, т.е. 6 × 1023.
Число Авогадро (постоянная Авогадро, NA) — число частиц (молекул, атомов, ионов) содержащихся в одном моле любого вещества.

Больше всего мне хотелось бы, чтобы вы поняли физический смысл изученных понятий. Моль — международная единица количества вещества, которая
показывает, сколько атомов, молекул или ионов содержится в определенной массе или конкретном объеме вещества. Один моль любого вещества
содержит 6.02 × 1023 атомов/молекул/ионов — вот самое важное, что сейчас нужно понять.
Иногда в задачах бывает дано число Авогадро, и от вас требуется найти, какое вам дали количество вещества (моль). Количество вещества в химии
обозначается N, ν (по греч. читается «ню»).
Рассчитаем по формуле: ν = N/NA количество вещества 3.01 × 1023 молекул воды и 12.04 × 1023 атомов углерода.
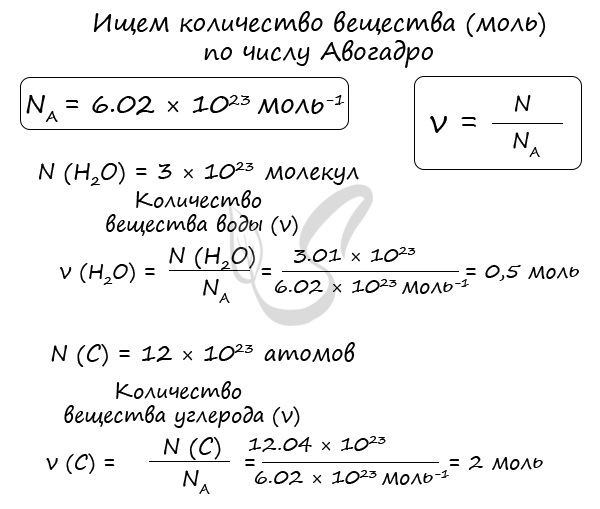
Мы нашли количества вещества (моль) воды и углерода. Сейчас это может показаться очень абстрактным, но, иногда не зная, как найти
количество вещества, используя число Авогадро, решение задачи по химии становится невозможным.
Молярная масса — M
Молярная масса — масса одного моля вещества, выражается в «г/моль» (грамм/моль). Численно совпадает с изученной нами ранее
относительной молекулярной массой.
Рассчитаем молярные массы CaCO3, HCl и N2
M (CaCO3) = Ar(Ca) + Ar(C) + (3 × Ar(O)) = 40 + 12 + (3 × 16) = 100 г/моль
M (HCl) = Ar(H) + Ar(Cl) = 1 + 35.5 = 36.5 г/моль
M (N2) = Ar(N) × 2 = 14 × 2 = 28 г/моль
Полученные знания не должны быть отрывочны, из них следует создать цельную систему. Обратите внимание: только что мы рассчитали
молярные массы — массы одного моля вещества. Вспомните про число Авогадро.
Получается, что, несмотря на одинаковое число молекул в 1 моле (1 моль любого вещества содержит 6.02 × 1023 молекул),
молекулярные массы отличаются. Так, 6.02 × 1023 молекул N2 весят 28 грамм, а такое же количество молекул
HCl — 36.5 грамм.
Это связано с тем, что, хоть количество молекул одинаково — 6.02 × 1023, в их состав входят разные атомы, поэтому и
массы получаются разные.

Часто в задачах бывает дана масса, а от вас требуется рассчитать количество вещества, чтобы перейти к другому веществу в реакции.
Сейчас мы определим количество вещества (моль) 70 грамм N2, 50 грамм CaCO3, 109.5 грамм HCl. Их молярные
массы были найдены нам уже чуть раньше, что ускорит ход решения.

ν (CaCO3) = m(CaCO3) : M(CaCO3) = 50 г. : 100 г/моль = 0.5 моль
ν (HCl) = m(HCl) : M(HCl) = 109.5 г. : 36.5 г/моль = 3 моль
Иногда в задачах может быть дано число молекул, а вам требуется рассчитать массу, которую они занимают. Здесь нужно использовать
количество вещества (моль) как посредника, который поможет решить поставленную задачу.
Предположим нам дали 15.05 × 1023 молекул азота, 3.01 × 1023 молекул CaCO3 и 18.06 × 1023 молекул
HCl. Требуется найти массу, которую составляет указанное число молекул. Мы несколько изменим известную формулу, которая поможет нам связать
моль и число Авогадро.

Теперь вы всесторонне посвящены в тему. Надеюсь, что вы поняли, как связаны молярная масса, число Авогадро и количество вещества.
Практика — лучший учитель. Найдите самостоятельно подобные значения для оставшихся CaCO3 и HCl.
Молярный объем
Молярный объем — объем, занимаемый одним молем вещества. Примерно одинаков для всех газов при стандартной температуре
и давлении составляет 22.4 л/моль. Он обозначается как — VM.
Подключим к нашей системе еще одно понятие. Предлагаю найти количество вещества, количество молекул и массу газа объемом
33.6 литра. Поскольку показательно молярного объема при н.у. — константа (22.4 л/моль), то совершенно неважно, какой газ мы
возьмем: хлор, азот или сероводород.
Запомните, что 1 моль любого газа занимает объем 22.4 литра. Итак, приступим к решению задачи. Поскольку какой-то газ
все же надо выбрать, выберем хлор — Cl2.


Моль (количество вещества) — самое гибкое из всех понятий в химии. Количество вещества позволяет вам перейти и к
числу Авогадро, и к массе, и к объему. Если вы усвоили это, то главная задача данной статьи — выполнена 

Относительная плотность и газы — D
Относительной плотностью газа называют отношение молярных масс (плотностей) двух газов. Она показывает, во сколько раз одно вещество
легче/тяжелее другого. D = M (1 вещества) / M (2 вещества).
В задачах бывает дано неизвестное вещество, однако известна его плотность по водороду, азоту, кислороду или
воздуху. Для того чтобы найти молярную массу вещества, следует умножить значение плотности на молярную массу
газа, по которому дана плотность.
Запомните, что молярная масса воздуха = 29 г/моль. Лучше объяснить, что такое плотность и с чем ее едят на примере.
Нам нужно найти молярную массу неизвестного вещества, плотность которого по воздуху 2.5

Предлагаю самостоятельно решить следующую задачку (ниже вы найдете решение): «Плотность неизвестного вещества по
кислороду 3.5, найдите молярную массу неизвестного вещества»

Относительная плотность и водный раствор — ρ
Пишу об этом из-за исключительной важности в решении
сложных задач, высокого уровня, где особенно часто упоминается плотность. Обозначается греческой буквой ρ.
Плотность является отражением зависимости массы от вещества, равна отношению массы вещества к единице его объема. Единицы
измерения плотности: г/мл, г/см3, кг/м3 и т.д.
Для примера решим задачку. Объем серной кислоты составляет 200 мл, плотность 1.34 г/мл. Найдите массу раствора. Чтобы не
запутаться в единицах измерения поступайте с ними как с самыми обычными числами: сокращайте при делении и умножении — так
вы точно не запутаетесь.

Иногда перед вами может стоять обратная задача, когда известна масса раствора, плотность и вы должны найти объем. Опять-таки,
если вы будете следовать моему правилу и относится к обозначенным условным единицам «как к числам», то не запутаетесь.
В ходе ваших действий «грамм» и «грамм» должны сократиться, а значит, в таком случае мы будем делить массу на плотность. В противном случае
вы бы получили граммы в квадрате 
К примеру, даны масса раствора HCl — 150 грамм и плотность 1.76 г/мл. Нужно найти объем раствора.

Массовая доля — ω
Массовой долей называют отношение массы растворенного вещества к массе раствора. Важно заметить, что в понятие раствора входит
как растворитель, так и само растворенное вещество.
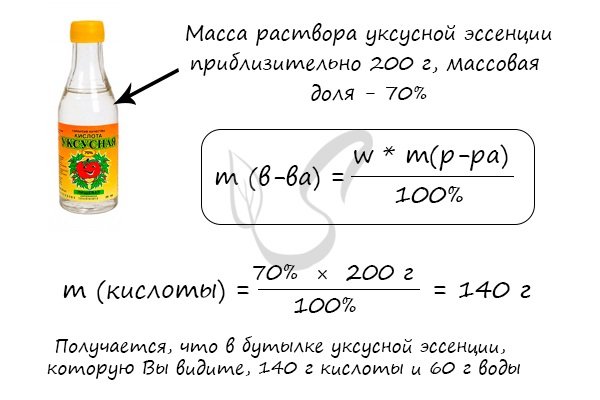
Массовая доля вычисляется по формуле ω (вещества) = m (вещества) / m (раствора). Полученное число будет показывать массовую долю
в долях от единицы, если хотите получить в процентах — его нужно умножить на 100%. Продемонстрирую это на примере.

Решим несколько иную задачу и найдем массу чистой уксусной кислоты в широко известной уксусной эссенции.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Как вычислить молярную массу вещества? В каких единицах она измеряется?
А еще есть относительная молекулярная масса. Почему она относительная и численно равна молярной массе? Может быть это одно и то же?
Вот сколько вопросов возникает сразу в отношении такого простого на первый взгляд понятия, как молярная масса.
Разберемся по порядку и научимся ее определять.
Содержание:
1.Относительная атомная масса
2.Почему атомная масса дробная?
3.Относительная молекулярная масса
4.Количество вещества и молярная масса
5.Как вычислить молярную массу вещества
Относительная атомная масса
Огромнейший вклад в развитие и обоснование понятия относительная атомная масса внесли в разное время французский ученый Гей-Люссак, итальянский ученый А.Авогадро и шведский ученый Й.Я. Берцелиус.
Не углубляясь в историю вопроса, вспомним, что любой химический элемент представляет собой определенную разновидность атомов. Сегодня мы знаем, что атомы химических элементов имеют свои особые характеристики.
И самая главная из них, определяющая практически все остальные, это заряд ядра. А так как заряд ядра обусловлен присутствием в нем протонов, а заряд одного протона равен +1, то и количество протонов, соответственно, также является важнейшей характеристикой атомов химических элементов.
Основную массу атома составляет ядро, которое кроме протонов содержит еще и нейтроны. Масса последних сопоставима с массой первых. Оболочку атома составляют электроны.
По числу частиц в атоме, а точнее, по их суммарной массе, атомы химических элементов можно условно разделить на тяжелые и легкие. Например, легким элементом является водород, так как его атомы имеют самую маленькую массу. А свинец — это уже тяжелый элемент. Масса его атома в 302 раза тяжелее массы атома водорода.
Но тем не менее, как бы мы не делили все атомы на тяжелые или легкие, абсолютная масса (mA) каждого из них ничтожно мала, как мала и масса составляющих их частиц. Например,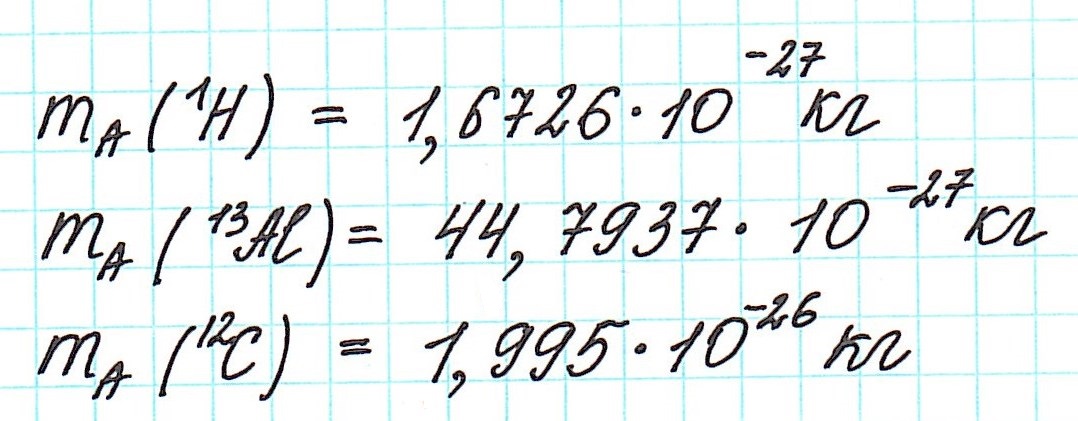
Величина, с которой сравнивают массу атома
Первоначально еще Дальтон сравнивал массы атомов с массой атома водорода, как самого легкого. Позднее появилась так называемая кислородная единица, равная 1/16 части массы атома кислорода. К ней перешли потому, что большинство атомов химических элементов образуют соединения с кислородом.
Однако, с развитием атомной физики и эта единица стала крайне неудобной. Все потому, что кислород в природе имеет несколько изотопов (а именно 3 устойчивых, всего же их 16). А изотопы, как известно, отличаются своей атомной массой. Из-за большого разнообразия изотопов и их различной устойчивости кислородная единица утратила свою актуальность.
В настоящее время (с 1961 года) общепринятой является углеродная единица, так называемая атомная единица массы (сокращенно а.е.м.). Она равна 1/12 части массы атома углерода (изотопа 12С).
Почему именно углерод? Да потому, что:
— у углерода всего 2 изотопа: 12С и 13С; причем первого 98,9%;
— количество органических веществ (их основу составляет, как известно, именно углерод) в сотни раз больше, чем неорганических;
— при переходе от кислородной единицы к углеродной уже посчитанные относительные атомные массы всех элементов изменились не существенно, что оказалось очень удобным.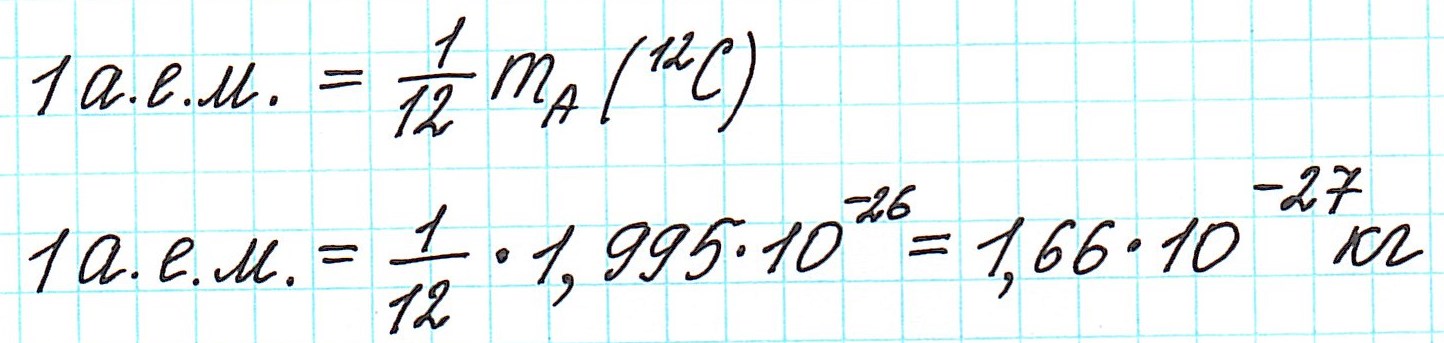
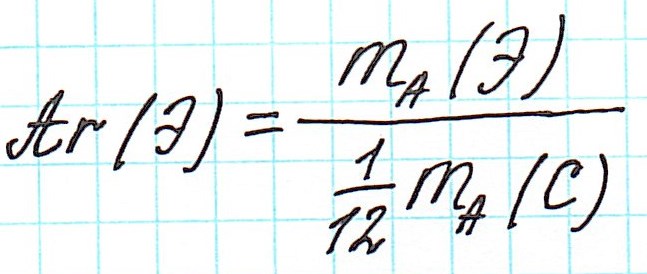
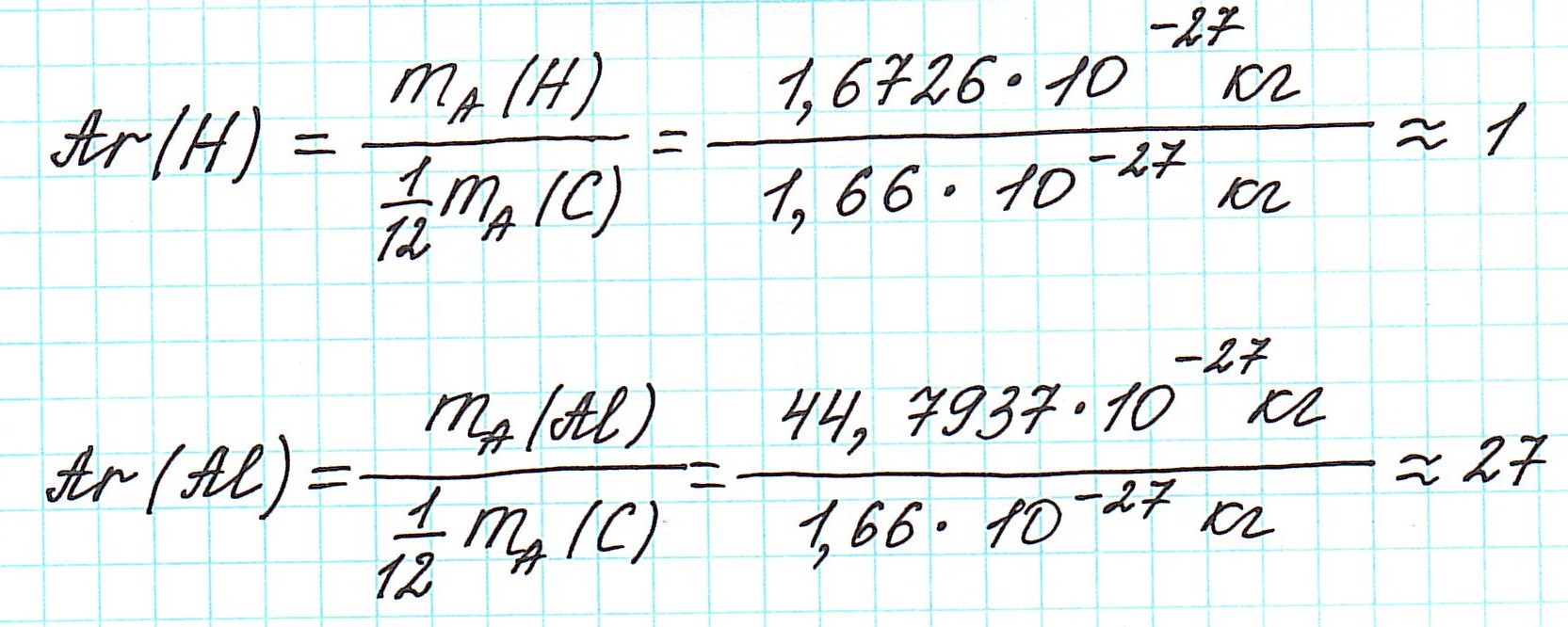
Почему атомная масса дробная?
Вернемся к строению атома.
Масса атома складывается из массы всех составляющих его частиц.
Массы протона и нейтрона приняты равными 1. А вот массой электрона обычно пренебрегают (по крайней мере в химии), так как даже относительная она безнадежно мала (0,0005485799090659(16) а.е.м.). То есть можно сказать, что масса атома определяется массой его ядра.
В составе ядра целое количество частиц. Например, в атоме одного из изотопов кислорода 8 протонов и 8 нейтронов. Значит, его Ar должна быть равна 16. Так почему же Ar представлена в периодической системе химических элементов в виде десятичной дроби? Для кислорода это Ar(О)=15,9994.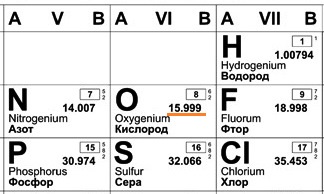
Например, химический элемент кислород в природе состоит на 99,76% из изотопа 16О, на 0,04% из изотопа 17О и на 0,20% из изотопа 18О. Таким образом, Ar для кислорода является средним значением, учитывающим относительное содержание его изотопов.
Относительная молекулярная масса
А как же найти относительную молекулярную массу?
Здесь не все так просто. Понятие «относительная молекулярная масса» не всегда применяется корректно. Правильнее было бы говорить о «формульной массе».
Дело в том, что молекулы характерны для веществ с ковалентными связями: вода H2O, серная кислота H2SO4, глюкоза C6H12O6 и т.д. И к ним в полной мере можно применить термин «относительная молекулярная масса».
Так как молекулы состоят из атомов, то относительная молекулярная масса (Mr) будет складываться из их относительных атомных масс. Например: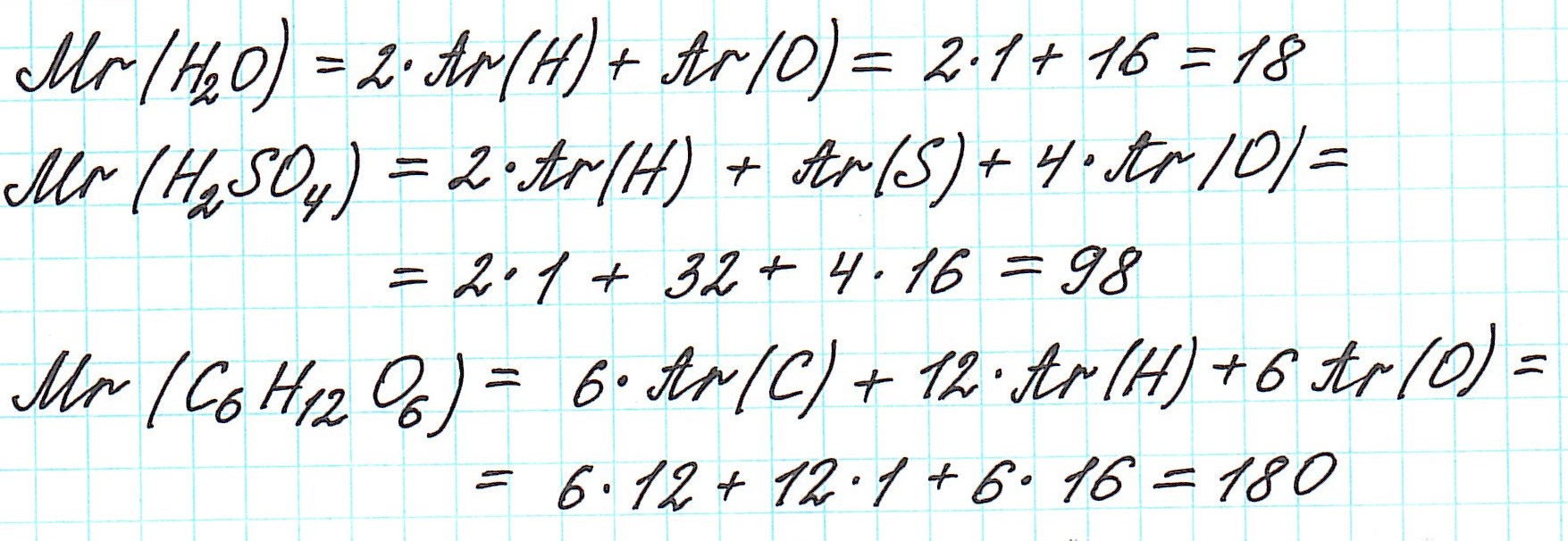
Например, формула NaCl показывает, что в кристалле хлорида натрия на один ион натрия Na+ приходится один ион хлора Cl—. На самом деле формула хлорида натрия должна выглядеть так: Na∞Cl∞. Поэтому запомним, что к ионным соединениям термины «молекула» и «молекулярная масса» не применимы.
В связи с этим для подобных веществ вычисляется формульная масса. А вычисляется она все по тому же принципу, что и молекулярная масса. Обозначается так же — Mr. Например, для хлорида натрия:
Точно так же, как относительную атомную массу (Ar), относительную молекулярную массу (Mr) будем сопоставлять с 1/12 частью атома изотопа углерода 12С.
В последующем говорим о Mr.
Количество вещества и молярная масса
В практических расчетах все-таки требуется вычислять массы, взятые в граммах, килограммах ато и в тоннах (если речь идет о каком-то производстве, например).
Как же поступают тогда?
Введена новая и тоже относительная величина – моль.
Точно было посчитано, что определенное количество атомов изотопа углерода 12С, а именно 6,02·1023, имеют массу ровно 12 г. Обратите внимание, что относительная молекулярная масса для этого же изотопа равна 12, но не грамм!
Количество вещества, которое содержит столько же частиц (атомов, ионов, молекул – в зависимости от строения), что и 12 г изотопа углерода 12С, назвали молем.
Один моль вещества (любого!) всегда содержит 6,02·1023 его частиц (постоянная Авогадро).
Ну, а так как атомы элементов отличаются по своей массе, то и 1 моль вещества тоже будет отличаться по массе.
Массу одного моля вещества называют молярной массой (М) и вычисляют в г/моль.
Таким образом, молярная масса и количество вещества связаны соотношением:
Можно также определить и такие отношения, связанные с количеством вещества:
Почему же относительная молекулярная и молярная массы равны?
Итак, относительная молекулярная и молярная массы, как следует из их определений – это не одно и то же.
Докажем, каким образом обе массы численно могут быть равны:
Как вычислить молярную массу вещества
Мы уже знаем, что относительная молекулярная масса складывается из относительных атомных масс.
При нахождении относительной молекулярной массы (Mr), а значит и молярной (М), выполняем следующие действия:
1) правильно записываем формулу вещества;
2) анализируем качественный состав (атомы каких элементов составляют вещество) и количественный состав (в каких количествах находятся эти атомы – смотрим по индексам, которые стоят справа внизу от знака химического элемента);
3) в периодической системе химических элементов находим элементы, атомы которых составляют вещество, и округляем относительную атомную массу, стоящую рядом со знаком элемента, до целого числа (! у хлора – до 35,5);
4) складываем относительные атомные массы всех элементов с учетом количества атомов.
Рассмотрим еще примеры:
Как вычислить молярную массу вещества, находящегося в газообразном состоянии
Определить молекулярную (а значит и молярную) массу газообразного вещества можно, используя закон Авогадро. Он гласит, что в равных объемах газов, взятых при одинаковой температуре, а также одинаковом давлении, содержится равное число молекул.
Это означает, что в данных условиях отношение масс газов друг к другу является отношением их молярных масс:


Запомните, что средняя молярная масса воздуха равна 29 г/моль.
Вычислить молярную массу вещества (а, значит, и относительную молекулярную), находящегося в газообразном состоянии, можно, используя молярный объем газа (VM):
Итак, подведем итог:
- Относительная молекулярная масса (Mr) показывает отношение массы молекулы к 1/12 части массы атома изотопа углерода 12С.
- Молярная масса (М) – масса одного моля вещества, равная отношению массы вещества к его количеству и выраженная в г/моль.
- Относительная молекулярная и молярная массы численно равны.
- Вычислить молярную массу вещества (и относительную молекулярную также) можно, используя значения относительных атомных масс, записанных в периодической системе.
Без вычисления молярной массы не обходится решение практически ни одной задачи. Если вы поняли, что такое молярная и относительная молекулярная массы и как их вычислять, но еще не умеете решать задачи с их применением, то самое время научиться.
Разбор простых типовых задач по химии в книге, которую вы можете совершенно БЕСПЛАТНО скачать здесь.
Чтобы самыми первыми узнавать о новых публикациях на сайте, присоединяйтесь к нашей группе ВКонтакте.
О.С.ГАБРИЕЛЯН,
И.Г.ОСТРОУМОВ,
А.К.АХЛЕБИНИН
СТАРТ В ХИМИЮ
7 класс
Продолжение. Начало см. в № 1, 2, 3, 4, 5/2006
Глава 2. Математика в химии
§ 10. Относительная атомная и
молекулярная массы

внимательно посмотрим на таблицу Д.И.Менделеева
и выберем один из элементов. Например, обитатель
шестой «квартиры» – углерод. Что изображено в
этой клетке? Знак (символ) химического элемента и
его название. В верхнем левом углу – порядковый
номер элемента, под символом элемента – его
название. А что означает записанное под
названием число 12,011?
Это число называется относительной атомной
массой элемента, в нашем случае – углерода.
Как вы помните, одно из важнейших свойств
атомов химических элементов – их масса.
Статья опубликована при поддержке группы компаний «Евроинжиниринг». Бензогенераторы, дизельгенераторы, снегоуборщики, блоки автоматического запуска, комплекты для ТО, предпусковые подогреватели, контейнеры для генераторов и другие товары от ведущих мировых производителей. Доставка по всей России, наличный и безналичный расчёт, гарантия качества. Доступна услуга выездного обслуживания бензиновых и дизельных генераторов. Всю подробную информацию Вы найдёте на сайте: http://energyprofessional.ru.
Размерность массы вам хорошо известна: ее
выражают в граммах, килограммах, миллиграммах.
Существуют, конечно, и другие единицы массы:
тонны, например, или центнеры. Однако в
повседневной жизни бывает удобно оперировать не
точной массой предмета, а сравнением ее с
чем-либо. Поскольку массы атомов и молекул
чрезвычайно малы, их сравнивают с массой атома
самого легкого элемента – водорода. Такое
сравнение позволяет утверждать, что масса атома
углерода в 12 раз больше массы атома водорода.
Масса атома кислорода больше массы атома
водорода в 16 раз, а масса атома железа – в 56 раз.
Величина, показывающая, во сколько раз масса
атома данного элемента больше массы атома
водорода, принятой за единицу, называется
относительной атомной массой элемента.
Относительную атомную массу элемента
обозначают символом Аr. Подстрочная
буква r – это первая буква английского слова relative,
что значит относительный. Например: Аr(Н) =
1,
Аr(С) = 12, Аr(N) = 14, Аr(О) = 16, Аr(Fe)
= 56, Аr(Cl) = 35,5.
Обычно относительные атомные массы всех
элементов округляют до целых чисел, кроме хлора
(Аr(Cl) = 35,5), хотя в таблице Д.И.Менделеева
они приведены с большей точностью.
Обратите внимание, что относительная атомная
масса хотя массой и называется, но размерности не
имеет.
Обладают ли массой молекулы веществ? Конечно!
Можете ли вы ответить на вопрос, во сколько раз
молекула воды тяжелее атома водорода? Это очень
просто: надо сложить относительные атомные массы
всех атомов, входящих в состав молекулы (рис. 56):
Mr(H2O) = 2Ar(H) + Ar(O)
= 2•1 + 16 = 18.
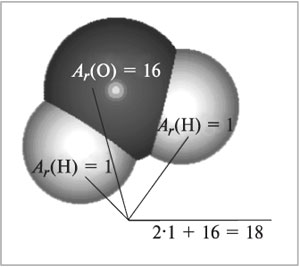 |
Рис. 56.
|
Величина Mr(H2O) – это относительная
молекулярная масса воды. Правильнее было бы
называть ее относительной формульной массой.
Во-первых, не все вещества состоят из молекул (мы
уже приводили в пример железо и графит).
Во-вторых, при расчете этой величины нужно
внимательно смотреть на формулу вещества и не
забывать про индексы, указывающие на число
атомов каждого элемента:
Mr(СH4) = Ar(С) + 4Ar(Н)
= 12 + 4•1 = 16,
Mr(SO2) = Ar(S) + 2Ar(O)
= 32 + 2•16 = 64.
Таблица относительных атомных масс Дж.Дальтона
была далека от совершенства, содержала довольно
много ошибок. Но благодаря ей стало возможным
определять формулы химических веществ по
соотношению масс входящих в их состав элементов.
Как это делалось, мы расскажем на следующем
уроке.
1.
Что такое относительная атомная масса? Почему
эта величина не имеет размерности?2. Что такое относительная молекулярная
масса? Как она рассчитывается?3. В состав молекулы фосфорной кислоты
входят три атома водорода, один атом фосфора и
четыре атома кислорода. Найдите относительную
молекулярную массу этого вещества.4. Рассчитайте относительные молекулярные
массы веществ по их формулам: Br2, H2O, CO2,
H2SO4, KOH, BaCl2. Значения
относительных атомных масс найдите по таблице
Д.И.Менделеева, округлите их до целых чисел (за
исключением хлора,
Ar(Cl) = 35,5).
5.
Атом серы образует с атомами кислорода два
сложных вещества (их называют оксидами) разного
состава. Относительная молекулярная масса
первого оксида равна 64, а второго – 80. Выведите
формулы этих оксидов.6. Не производя расчетов, а только на
основании значений относительных атомных масс
(найдите их по таблице Д.И.Менделеева) определите,
у какого из веществ, формулы которых приведены
ниже, наибольшая и наименьшая относительные
молекулярные массы: а) селеноводорода H2Se; б)
воды Н2О;
в) теллуроводорода H2Te; г) сероводорода H2S.
§11. Массовая доля элемента в сложном
веществе
С XVII в. химия перестала быть описательной
наукой. Ученые-химики стали широко использовать
измерение вещества. Все более
совершенствовалась конструкция весов,
позволяющих определять массы образцов. Для
газообразных веществ помимо массы измеряли
также объем и давление. Применение
количественных измерений дало возможность
понять сущность химических превращений,
определять состав сложных веществ.
Как вы уже знаете, в состав сложного вещества
входят два или более химических элементов.
Очевидно, что масса всего вещества слагается из
масс составляющих его элементов. Значит, на долю
каждого элемента приходится определенная часть
массы вещества.
Массовой долей элемента называется отношение
массы этого элемента в сложном веществе к массе
всего вещества, выраженное в долях единицы (или в
процентах):
Массовая доля элемента в соединении
обозначается латинской строчной буквой w
(«дубль-вэ») и показывает долю (часть массы),
приходящуюся на данный элемент в общей массе
вещества. Эта величина может выражаться в долях
единицы или в процентах. Конечно, массовая доля
элемента в сложном веществе всегда меньше
единицы (или меньше 100%). Ведь часть от целого
всегда меньше целого, как долька апельсина
меньше всего апельсина.
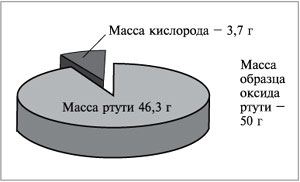
Например, в состав оксида ртути входят два
элемента – ртуть и кислород. При нагревании 50 г
этого вещества получается 46,3 г ртути и 3,7 г
кислорода (рис. 57). Рассчитаем массовую долю ртути
в сложном веществе:
|
|
Рис. 57.
|
Массовую долю кислорода в этом
веществе можно рассчитать двумя способами. По
определению массовая доля кислорода в оксиде
ртути равна отношению массы кислорода к массе
оксида:
Зная, что сумма массовых долей элементов в
веществе равна единице (100%), массовую долю
кислорода можно вычислить по разности:
w(O) = 1 – 0,926 = 0,074,
или
w(О) = 100% – 92,6% = 7,4%.
Для того чтобы найти массовые доли элементов
предложенным способом, необходимо провести
сложный и трудоемкий химический эксперимент по
определению массы каждого элемента. Если же
формула сложного вещества известна, та же задача
решается значительно проще.
Для расчета массовой доли элемента нужно его
относительную атомную массу умножить на число
атомов (n) данного элемента в формуле и
разделить на относительную молекулярную массу
вещества:
Например, для воды (рис. 58):
Mr(H2O) = 1•2 + 16 = 18,
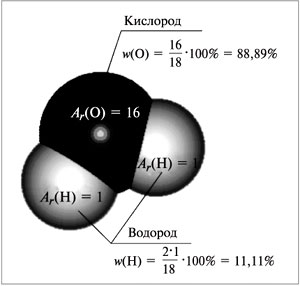 |
Рис. 58.
|
Далее рассмотрим решение задач на
вычисление массовых долей элементов в сложных
веществах.
Задача 1. Рассчитайте массовые доли
элементов в аммиаке, формула которого NH3.
Дано:
вещество аммиак NH3.
Найти:
w(N), w(H).
Решение
1) Рассчитаем относительную молекулярную массу
аммиака:
Mr(NH3) = Ar(N) + 3Ar(H)
= 14 + 3•1 = 17.
2) Найдем массовую долю азота в веществе:
3) Вычислим массовую долю водорода в аммиаке:
w(H) = 1 – w(N) = 1 – 0,8235 = 0,1765, или 17,65%.
Ответ. w(N) = 82,35%, w(H) = 17,65%.
Задача 2. Рассчитайте массовые доли
элементов в серной кислоте, имеющей формулу H2SO4.
Дано:
серная кислота H2SO4.
Найти:
w(H), w(S), w(O).
Решение
1) Рассчитаем относительную молекулярную массу
серной кислоты:
Mr(H2SO4) = 2Ar(H)
+ Ar(S) + 4Ar(O) = 2•1 + 32 + 4•16 = 98.
2) Найдем массовую долю водорода в веществе:
3) Вычислим массовую долю серы в серной кислоте:
4. Рассчитаем массовую долю кислорода в
веществе:
w(O) = 1 – (w(H) + w(S)) = 1 – (0,0204 +
0,3265) = 0,6531, или 65,31%.
Ответ. w(H) = 2,04%, w(S) = 32,65%, w(O) = 65,31%.
Чаще химикам приходится решать обратную
задачу: по массовым долям элементов определять
формулу сложного вещества. То, как решаются
подобные задачи, проиллюстрируем одним
историческим примером.
Из природных минералов – тенорита и куприта –
были выделены два соединения меди с кислородом
(оксиды). Они отличались друг от друга по цвету и
массовым долям элементов. В черном оксиде
массовая доля меди составляла 80%, а массовая доля
кислорода – 20%. В оксиде меди красного цвета
массовые доли элементов составляли
соответственно 88,9% и 11,1%. Каковы же формулы этих
сложных веществ? Проведем несложные
математические расчеты.
Пример 1. Расчет химической формулы черного
оксида меди (w(Cu) = 0,8 и w(О) = 0,2).
1) Обозначим формулу вещества с помощью
индексов х, у – по числу атомов химических
элементов в его составе: СuxOy.
2) Отношение индексов равно отношению частных
от деления массовой доли элемента в соединении
на относительную атомную массу элемента:
3) Полученное соотношение нужно привести к
соотношению целых чисел: индексы в формуле,
показывающие число атомов, не могут быть
дробными. Для этого полученные числа разделим на
меньшее (т.е. любое) из них:
Получилась формула – СuO.
Пример 2. Расчет формулы красного оксида
меди по известным массовым долям w(Cu) = 88,9% и w(O)
= 11,1%.
Дано:
w(Cu) = 88,9%, или 0,889,
w(O) = 11,1%, или 0,111.
Найти:
формулу.
Решение
1) Обозначим формулу оксида СuxOy.
2) Найдем соотношение индексов x и y:
3) Приведем соотношение индексов к отношению
целых чисел:
Ответ. Формула соединения – Cu2O.
А теперь немного усложним задачу.
Задача 3. По данным элементного
анализа состав прокаленной горькой соли,
использовавшейся еще алхимиками в качестве
слабительного средства, следующий: массовая доля
магния – 20,0%, массовая доля серы – 26,7%, массовая
доля кислорода – 53,3%.
Дано:
w(Mg) = 20,0%, или 0,2,
w(S) = 26,7%, или 0,267,
w(O) = 53,3%, или 0,533.
Найти:
формулу.
Решение
1) Обозначим формулу вещества с помощью
индексов x, y, z: MgxSyOz.
2) Найдем соотношение индексов:
3) Определим значение индексов x, y, z:
Ответ. Формула вещества – MgSO4.
1.
Что называется массовой долей элемента в сложном
веществе? Как рассчитывается эта величина?2. Рассчитайте массовые доли элементов в
веществах: а) углекислом газе CO2;
б) сульфиде кальция СаS; в) натриевой селитре NaNO3;
г) оксиде алюминия Al2O3.3. В каком из азотных удобрений массовая
доля питательного элемента азота наибольшая: а)
хлориде аммония NH4Cl; б) сульфате аммония (NH4)2SO4;
в) мочевине (NH2)2CO?
4.
В минерале пирите на 7 г железа приходится 8 г
серы. Вычислите массовые доли каждого элемента в
этом веществе и определите его формулу.5. Массовая доля азота в одном из его оксидов
равна 30,43%, а массовая доля кислорода – 69,57%.
Определите формулу оксида.
6. В средние века из золы костра выделяли
вещество, которое называли поташ и использовали
для варки мыла. Массовые доли элементов в этом
веществе: калий – 56,6%, углерод – 8,7%, кислород –
34,7%. Определите формулу поташа.
найди число атомов каждого элемента в молекуле оксида углерода, если массовая доля углерода в нём равна (42,86) %, а массовая доля кислорода — (57,14) %.
1. Примем массу оксида равной (100) г. Масса углерода в такой порции равна (42,86) г, а масса кислорода — (57,14) г.
2. Находим относительные атомные массы элементов в Периодической таблице:
3. Обозначаем число атомов углерода как (x), а число атомов кислорода — (y), и записываем отношение масс:
.
4. Получаем выражение:
5. Находим отношение (x : y):
.
В молекуле оксида углерода на (1) атом углерода приходится (1) атом кислорода.
В уроке 5 «Моль и молярная масса» из курса «Химия для чайников» рассмотрим моль как единицу измерения количества вещества; дадим определение числу Авогадро, а также научимся определять молярную массу и решать задачи на количество вещества. Базой для данного урока послужат основы химии, изложенные в прошлых уроках, так что если вы изучаете химию с нуля, то рекомендую их просмотреть хотя бы мельком.
Единица измерения количества вещества
До этого урока мы обсуждали лишь индивидуальные молекулы и атомы, а их массы мы выражали в атомных единицах массы. В реальной жизни с индивидуальными молекулами работать невозможно, потому что они ничтожно малы. Для этого химики взвешивают вещества ни в а.е.м., а в граммах.
Чтобы перейти от молекулярной шкалы измерения масс в лабораторную шкалу, используют единицу измерения количества вещества под названием моль. 1 моль содержит 6,022·1023 частиц (атомов или молекул) и является безразмерной величиной. Число 6,022·1023 носит название Число Авогадро, которое определяется как число частиц, содержащихся в 12 г атомов углерода 12C. Важно понимать, что 1 моль любого вещества содержит всегда одно и то же число частиц (6,022·1023).
Как уже было сказано, термин «моль» применяется не только к молекулам, но также и к атомам. Например, если вы говорите о моле гелия (He), то это означает, что вы имеет количество равное 6,022·1023 атомов. Точно так же, 1 моль воды (H2O) подразумевает количество равное 6,022·1023 молекул. Однако чаще всего моль применяют именно к молекулам.
Молярная масса вещества
Молярная масса – это масса 1 моля вещества, выраженная в граммах. Молярную массу одного моля любого химического элемента без труда находят из таблицы Менделеева, так как молярная масса численно равна атомной массе, но размерности у них разные (молярная масса имеет размерность г/моль). Запишите и запомните формулы для вычисления молярной массы, количества вещества и числа молекул:
- Молярная масса формула M=m/n
- Количество вещества формула n=m/M
- Число молекул формула N =NA·n
где m — масса вещества, n — количество вещества (число молей), М — молярная масса, N — число молекул, NA — число Авогадро. Благодаря молярной массе вещества химики могут вести подсчет атомов и молекул в лаборатории просто путем их взвешивания. Этим и удобно использование понятия моль.
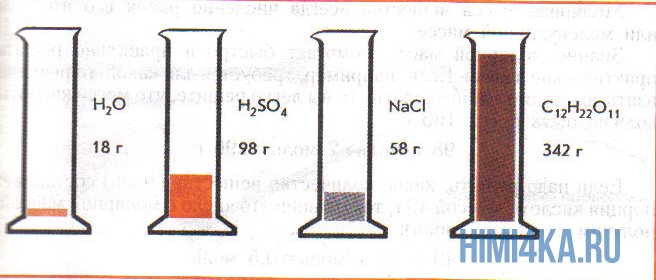
На рисунке изображены четыре колбы с различными веществами, но в каждой из них всего 1 моль вещества. Можете перепроверить, используя формулы выше.
Задачи на количество вещества
Пример 1. Сколько граммов Н2, Н2O, СН3ОН, октана (С8Н18) и газа неона (Ne) содержится в 1 моле?
Решение: Молекулярные массы (в атомных единицах массы) перечисленных веществ приведены в таблице Менделеева. 1 моль каждого из названных веществ имеет следующую массу:
Поскольку массы, указанные в решении примера 1, дают правильные относительные массы взвешиваемых молекул, указанная масса каждого из перечисленных веществ содержит одинаковое число молекул. Этим и удобно использование понятия моля. Нет даже необходимости знать, чему равно численное значение моля, хотя мы уже знаем, что оно составляет 6,022·1023; эта величина называется числом Авогадро и обозначается символом NA. Переход от индивидуальных молекул к молям означает увеличение шкалы измерения в 6,022·1023 раз. Число Авогадро представляет собой также множитель перевода атомных единиц массы в граммы: 1 г = 6,022·1023 а.е.м. Если мы понимаем под молекулярной массой массу моля вещества, то ее следует измерять в граммах на моль; если же мы действительно имеем в виду массу одной молекулы, то она численно совпадает
с молекулярной массой вещества, но выражается в атомных единицах массы на одну молекулу. Оба способа выражения молекулярной массы правильны.
Пример 2. Сколько молей составляют и сколько молекул содержат 8 г газообразного кислорода O2?
Решение: Выписываем из таблицы Менделеева атомную массу атома кислорода (O), которая равна 15,99 а.е.м, округляем до 16. Так как у нас молекула кислорода, состоящая из двух атомов O, то ее атомная масса равна 16×2=32 а.е.м. Хорошо, а теперь переводим ее в молярную массу: 32 а.е.м = 32 г/моль. Это означает, что 1 моль (6,022·1023 молекул) O2 имеет массу 32 грамма. Ну и в заключении по формулам выше находим количество вещества (моль) и число молекул, содержащихся в 8 граммах O2:
- n = m / M = 8г / 32г/моль = 0,25 моль
- N = NA × n = 6,022·1023 × 0,25 = 1,505·1023 молекул
Пример 3. 1 молекула Н2 реагирует с 1 молекулой Сl2, в результате чего образуются 2 молекулы газообразного хлористого водорода НСl. Какую массу газообразного хлора необходимо использовать, чтобы он полностью прореагировал с 1 килограммом (кг) газообразного водорода?
Решение: Молекулярные массы H2 и Cl2 равны 2,0160 и 70,906 г/моль соответственно. Следовательно, в 1000 г H2 содержится
Даже не выясняя, сколько молекул содержится в одном моле вещества, мы можем быть уверены, что 496 моля Cl2 содержат такое же число молекул, как и 496,0 моля, или 1000 г, H2. Сколько же граммов Cl2 содержится в 496 молях этого вещества? Поскольку молекулярная масса Cl2 равна 70,906 г/моль, то
Пример 4. Сколько молекул H2 и Cl2 принимает участие в реакции, описанной в примере 3?
Решение: В 496 молях любого вещества должно содержаться 496 моля × 6,022·1023 молекул/моль, что равно 2,99·1026 молекул.
Чтобы наглядно показать, сколь велико число Авогадро, приведем такой пример: 1 моль кокосовых орехов каждый диаметром 14 сантиметров (см) мог бы заполнить такой объем, какой занимает наша планета Земля. Использование молей в химических расчетах рассматривается в следующей главе, но представление об этом пришлось ввести уже здесь, поскольку нам необходимо знать, как осуществляется переход от молекулярной шкалы измерения масс к лабораторной шкале.
Надеюсь урок 5 «Моль и молярная масса» был познавательным и понятным. Если у вас возникли вопросы, пишите их в комментарии.