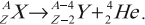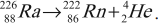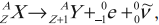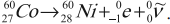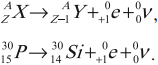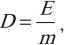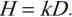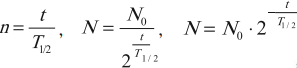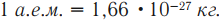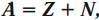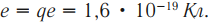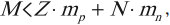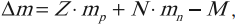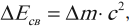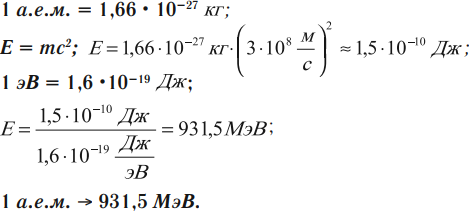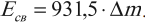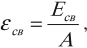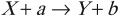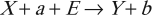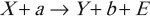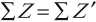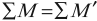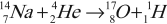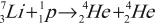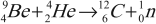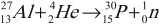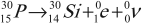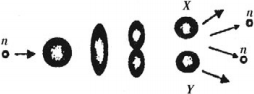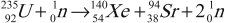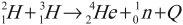Согласно протонно-нейтронной модели строения атомного ядра, заряд ядра должен быть равен сумме зарядов всех протонов, которые входят в его состав. Так как заряд протона равен элементарному заряду, то можно считать, что:
(q) — заряд ядра,
(e) — элементарный заряд,
()
Z
() — количество протонов в ядре.
Количество протонов в ядре
Z
называется зарядовым числом атомного ядра.
Экспериментально было доказано, что число Z совпадает с порядковым номером химического элемента в Периодической системе Менделеева.
Обрати внимание!
Количество протонов в ядре атома совпадает с номером химического элемента в Периодической системе химических элементов и называется зарядовым числом (
Z
).
Массовое число
Количество нейтронов в ядре атома принято обозначать N. Тогда количество протонов и нейтронов в ядре атома можно вычислить как:
A=Z+N.
— количество нуклонов в атоме называется массовым числом.
Изотопы
Химические свойства атома определяются зарядовым числом, так как это число указывает на номер атома в периодической системе, т. е. определяет, какой именно это химический элемент. Физические свойства атома могут быть разными в зависимости от массового числа. Действительно, экспериментально было доказано, что ядра одного и того же химического элемента могут обладать разными массами. Например, в природе существует несколько видов атомов водорода: водород, дейтерий и тритий. Масса дейтерия приблизительно в два, а трития — в три раза больше массы водорода.
Атомы одного и того же химического элемента, но с разными массами, называются изотопами.
Так как изотопы — это атомы одного и того же химического элемента, то зарядовое число у изотопов одинаковое, а массовые числа различные. Это означает, что ядра изотопов содержат одинаковое число протонов и разное количество нейтронов.
Изотопы принято обозначать:
XZA, где
XZA — химический элемент,
A — массовое число,
Z — зарядовое число.
Пример:
— водород,
H12
— дейтерий,
H13
— тритий.
407
атомного ядра
и элементарных
частиц
Глава 32
Элементы физики
атомного ядра
§251. Размер, состав и заряд атомного ядра. Массовое и зарядовое числа
Э.
Резерфорд, исследуя прохождение -частиц
с энергией в несколько мегаэлектрон-вольт
через тонкие пленки золота (см. §208),
пришел к выводу о том, что атом состоит
из положительно заряженного ядра и
окружающих его электронов. Проанализировав
эти опыты, Резерфорд также показал, что
атомные ядра имеют размеры примерно
10-14—10-15
м (линейные размеры атома примерно
10—10
м).
Атомное
ядро состоит из элементарных частиц
— протонов
и нейтронов (протонно-нейтронная
модель ядра была предложена советским
физиком Д. Д. Иваненко (р. 1904), а впоследствии
развита В. Гейзенбергом).
Протон
(р)
имеет
положительный заряд, равный заряду
электрона, и массу покоя mp=1,6726•10-27
кг
1836me,
где me
— масса
электрона. Нейтрон (n)
—
нейтральная частица с массой покоя
mn=1,6749•10-27кг
1839me,.
Протоны и нейтроны называются нуклонами
(от
лат. nucleus
—
ядро). Общее число нуклонов в атомном
ядре называется массовым
числом А.
Атомное
ядро характеризуется зарядом
Ze,
где
е
—
заряд протона, Z
—
зарядовое
число ядра,
равное числу протонов в ядре и
совпадающее с порядковым номером
химического элемента в Периодической
системе элементов Менделеева. Известные
в настоящее время 107 элементов таблицы
Менделеева имеют зарядовые числа ядер
от Z=1
до
Z=107.
Ядро
обозначается тем же символом, что и
нейтральный атом: AZХ,
где X
—
символ химического элемента, Z
—
атомный номер (число протонов в ядре),
А
— массовое
число (число нуклонов в ядре).
Сейчас
протонно-нейтронная модель ядра не
вызывает сомнений. Рассматривалась
также гипотеза о протонно-электронном
строении ядра, но она не выдержала
экспериментальной проверки. Так, если
придерживаться этой гипотезы, то
массовое число А
должно
представлять собой число протонов в
ядре, а разность между массовым числом
и числом электронов должна быть равна
заряду ядра. Эта модель согласовывалась
со значениями изотопных масс и зарядов,
но противоречила значениям спинов и
магнитных моментов ядер, энергии связи
ядра и т. д. Кроме того, она оказалась
несовместимой с соотношением
неопределенностей (см. §215). В результате
гипотеза о протонно-электронном строении
ядра была отвергнута.
Так как атом
нейтрален, то заряд ядра определяет и
число электронов в атоме. От числа же
электронов зависит их распределение
по состояниям в атоме, от которого, в
свою очередь, зависят химические
свойства атома. Следовательно, заряд
ядра определяет специфику данного
химического элемента, т. е. определяет
число электронов в атоме, конфигурацию
их электронных оболочек, величину и
характер внутриатомного электрического
поля.
Ядра
с одинаковыми Z,
но
разными А
(т.
е. с разными числами нейтронов N
=
408
А —
Z)
называются
изотопами,
а
ядра с одинаковыми A,
но разными Z
—
изобарами.
Например,
водород (Z=1)
имеет
три изотопа: 11Н
— протий (Z=1,
N=0),
21Н
— дейтерий (Z=1,
N=1),
31Н
— тритий (Z=
1,
N=
2), олово — десять, и т. д. В подавляющем
большинстве случаев изотопы одного и
того же химического элемента обладают
одинаковыми химическими и почти
одинаковыми физическими свойствами
(исключение составляют, например,
изотопы водорода), определяющимися
в основном структурой электронных
оболочек, которая является одинаковой
для всех изотопов данного элемента.
Примером ядер-изобар могут служить ядра
104Be,
105B,
106C.
В
настоящее время известно более 2000
ядер, отличающихся либо Z,
либо
A,
либо тем и другим.
Радиус
ядра задается
эмпирической формулой
R
=R0A1/3,
(251.1)
где
R0=(1,3—1,7)
10-15м.
Однако при употреблении этого термина
необходимо соблюдать осторожность
(из-за его неоднозначности, например
из-за размытости границы ядра). Из формулы
(251.1) вытекает, что объем ядра
пропорционален числу нуклонов в ядре.
Следовательно, плотность ядерного
вещества примерно одинакова для всех
ядер (1017
кг/м3).
Соседние файлы в папке Трофимова
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- Подробности
- Обновлено 18.06.2019 18:07
- Просмотров: 363
1. Как называются протоны и нейтроны вместе?
Протоны и нейтроны называются нуклонами.
То есть атомные ядра состоят из нуклонов.
В 1932 году Д.Д. Иваненко и В. Гейзенберг предложили протонно-нейтронную модель строения ядер.
2. Что называется массовым числом и какой буквой оно обозначается?
Массовым числом называется общее число нуклонов в ядре атома.
Массовое число численно равно массе ядра, выраженной в атомных единицах массы и округлённой до целых чисел.
Массовое число обозначается буквой А.
3. Что можно сказать о числовом значении массы атома (в а.е.м.) и его массовом числе?
Массовое число равно с точностью до целых (поскольку масса каждого нуклона примерно равна 1 а.е.м.) числу атомных единиц массы, содержащихся в массе атома.
2. Что называется зарядовым числом и какой буквой оно обозначается?
Зарядовым числом называется число протонов в ядре.
Зарядовое число численно равно заряду ядра, выраженному в элементарных электрических зарядах.
(Заряд каждого протона равен элементарному электрическому заряду. )
Зарядовое число обозначается буквой Z.
Для каждого химического элемента зарядовое число равно атомному (порядковому) номеру в таблице Д. И. Менделеева.
4. Как называется и какой буквой обозначается число протонов в ядре?
Число протонов в атоме обозначается буквой Z и называется зарядовым числом.
5. Что можно сказать о зарядовом числе, заряде ядра (выраженном в элементарных электрических зарядах) и порядковом номере в таблице Д. И. Менделеева для любого химического элемента?
Зарядовое число равно заряду ядра, выраженному в элементарных электрических зарядах.
Зарядовое число атома равно его порядковому номеру в таблице Менделеева.
6. Как в общем виде принято обозначать ядро любого химического элемента?
Ядро любого химического элемента в общем виде обозначается .
где Х — символ химического элемента.
7. Какой буквой обозначают число нейтронов в ядре?
Число нейтронов в ядре обозначают буквой N.
8. Какой формулой связаны между собой массовое число, зарядовое число и число нейтронов в ядре?
A = Z + N
где
A — массовое число или иначе общее число протонов и нейтронов в ядре,
Z — зарядовое число или иначе число протонов ядре,
N — число нейтронов в ядре.
9. Как с точки зрения протонно нейтронной модели ядра объясняется существование ядер с одинаковыми зарядами и различными массами?
У одного и того же химического элемента встречаются атомы с различными по массе ядрами.
Такие атомы
называются изотопами.
Атомы изотопов имеют одинаковый заряд и поэтому один и тот же порядковый номер в таблице Д. И. Менделеева.
Изотопы — это разновидности одного химического элемента, различающиеся по массе атомных ядер
Ядра изотопов содержат одинаковое число протонов, но различное число нейтронов.
Например:
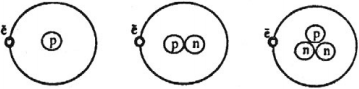
Существует три изотопа водорода: протий, дейтерий и тритий.
Ядро протия вообще не имеет нейтронов — оно состоит из 1 протона.
Ядро дейтерия состоит из двух частицы: 1 протон и 1 нейтрон.
Ядро трития состоит из трёх частиц: 1 протон и 2 нейтрона.
Следующая страница — смотреть
Назад в «Оглавление» — смотреть
Практически сразу после
открытия нейтрона советским физиком Дмитрием Иваненко и немецким учёным
Вернером Гейзенбергом была предложена протонно-нейтронная модель атомного ядра.
Согласно ей, ядра всех химических элементов (за исключением водорода) состоят
из двух видов частиц: протонов и нейтронов. Протоны и нейтроны называют
нуклонами (от латинского «нуклеус» — ядро), а ядра атомов — нуклидами.
Общее число нуклонов в ядре
называют массовым числом и обозначают
буквой А. Оно ставится вверху перед буквенным обозначением химического
элемента.
Например, массовое число
кислорода равно 16, а углерода — 12.
Мы уже говорили о том, что массовое
число принято выражать в атомных единицах массы (сокращённо, а. е. м.) и
округлять до целых чисел. Напомним также, что атомную единицу массы
выражают через массу атома углерода; она равна 1/12 части массы атома углерода:
Число протонов в ядре
соответствует порядковому или атомному номеру элемента в таблице Менделеева и
называется зарядовым числом,
поскольку оно определяет заряд ядра. Обозначается зарядовое число буквой Z.
В наших примерах, зарядовое
число кислорода равно восьми, а углерода — 6.
Как видно из приведённых
примеров, зарядовое число ставится внизу перед буквенным обозначением элемента.
Напомним, что заряд протона положителен
и равен элементарному электрическому заряду. Следовательно, зарядовое число
численно равно заряду ядра, выраженному в элементарных электрических зарядах.
Так как атом в целом
электрически нейтрален, то зарядовое число определяет одновременно и число
электронов в атоме.
Число нейтронов в ядре обозначают большой буквой N. Нетрудно
догадаться, что оно равно разнице между массовым и зарядовым числом:
Таким образом, ядро любого
атома обозначается буквенным символом элемента. Вверху указывается значение его
массового числа, а внизу — зарядового.
В общем случае любой
химический элемент периодической таблицы Дмитрия Ивановича Менделеева можно
представить в виде:
где под X
подразумевается символ химического элемента.
Ещё раз уточним, каким образом
определяется число протонов, электронов и нейтронов в ядре атома любого
химического элемента. Во-первых, необходимо посмотреть в таблице Менделеева
порядковый номер интересующего нас химического элемента. Таким образом мы
найдём зарядовое число, то есть количество протонов и электронов в ядре. Затем,
всё в той же таблице, необходимо посмотреть атомную массу этого элемента и
округлить её до целых. Тем самым мы найдём массовое число, то есть общее
количество нуклонов в ядре. И наконец, чтобы определить количество нейтронов в
ядре атома, мы должны будем вычесть из массового числа зарядовое.
На основе новой,
протонно-нейтронной модели строения атомных ядер, было дано объяснение многим
экспериментальным фактам. Так, например, ещё в 1906—1907 годах учёными было
выявлено, что продукт радиоактивного распада урана — ионий и продукт
радиоактивного распада тория — радиоторий имеют те же химические свойства, что
и торий, но отличаются от него атомной массой и характеристиками радиоактивного
распада. При этом атомы обладали одинаковыми химическими свойствами, а отделить
их друг от друга было невозможно никакими химическими методами. Впервые, на
существование таких атомов обратил внимание Фредерик Содди в 1910 году. Он
предложил называть такие разновидности атомов одного и того же химического
элемента изотопами (что по-гречески означает «равноместные»), так как по
своим химическим свойствам они должны быть помещены в одну и ту же клетку
таблицы Менделеева.
На основании многих
экспериментов, было установлено, что изотопы одинаково вступают в химические
реакции и образуют одинаковые соединения. Это говорило о том, что число
электронов в электронных оболочках, а, значит, и заряд ядра у изотопов
одинаковы. Следовательно, ядра изотопов различаются только числом нейтронов.
Иными словами, химические свойства элементов определяются не атомной массой, а
зарядовым числом ядра. Действительно, например, нуклиды водорода-три и гелия-три
имеют близкие по величине атомные массы, но принципиально разные химические
свойства.
Из всех известных на
сегодняшний день изотопов (а они есть у всех химических элементов) только изотопы
водорода имеют названия:
Протий является самым
распространённым изотопом в природе, а его ядро содержит только один протон.
Изотоп дейтерия (его ещё называют тяжёлой водой), содержит в своём ядре один
протон и один нейтрон. Соответственно, у трития — один протон и два нейтрона. В
настоящее время в лабораториях получены изотопы водорода и с большим числом
нейтронов: тремя, четырьмя, пятью и даже шестью.
Следует отметить, что у разных
атомов существует разное количество изотопов. Например, у урана их 26, но
самыми распространёнными в природе являются два — это уран-235 (около 0,7 %), и
уран-238 (чуть более 99 %). Вы, наверное, обратили внимание на то, что мы не
называли зарядового числа изотопов урана. Дело в том, что обычно изотопы
называют по их массовым числам, так как зарядовые числа у них одинаковые.
Отметим, что изотопы бывают
устойчивые (или стабильные) и неустойчивые (то есть радиоактивные). Стабильные
изотопы сохраняются сколь угодно долго.
А нестабильные изотопы со
временем превращаются в другие химические элементы в результате радиоактивных
превращений.
В настоящее время известно
около 280 стабильных изотопов химических элементов и более 2 тыс. радиоактивных
изотопов.
Как правило, природные
элементы представляют собой смесь нескольких изотопов, поэтому возникает
задача их разделения. Как мы уже знаем, магнитное поле искривляет траекторию
движения заряженных частиц. На этом свойстве магнитного поля основано действие
устройства, называемого масс-спектрографом, который используется для
разделения изотопов по массовому числу.
Закрепления материала.
В заключении отметим, что предложенная
Иваненко и Гейзенбергом протонно-нейтронная модель строения ядра впоследствии
полностью была подтверждена экспериментально. Однако оставался нерешённым ещё
один вопрос: почему ядра атомов не распадаются на отдельные нуклоны?
Действительно, ведь мы знаем, что ядра атомов являются весьма устойчивыми
образованиями, хотя в их состав входят одинаково заряженные частицы — протоны.
А поскольку размеры ядер очень малы, то между протонами должны существовать
огромные силы электрического отталкивания — порядка 230 ньютонов, что для
частиц с массой порядка 10–27 степени килограмм является очень
большой силой. Поэтому возникает вопрос: какое взаимодействие препятствует
взаимному отталкиванию между одноимённо заряженными частицами?
Мы знаем, что, кроме
электромагнитных сил, в природе существуют также гравитационные силы. Может
быть, стабилизирующую роль в ядрах играет именно гравитационное взаимодействие
между нуклонами?
Нет, так как расчёты
показывают, что сила гравитационного притяжения между двумя протонами в ядре
пренебрежимо мала по сравнению с силой электростатического отталкивания. Этот
результат позволяет сделать вывод о том, что между ядерными частицами,
по-видимому, действуют силы особой природы, радикально отличающиеся от
гравитационных и электромагнитных сил. Эти силы принято называть ядерными
силами. А так как ядерное взаимодействие во много раз превосходит
электромагнитное, то его ещё называют сильным взаимодействием.
Другой особенностью ядерных
сил является то, что они очень быстро убывают с увеличением расстояния между
ядерными частицами. Проще говоря, они действуют на расстояниях, сравнимыми с
размерами самих ядер.
Физика атомного ядра
Содержание
- Радиоактивность. Альфа-распад. Бета-распад. Гамма-излучение
- Закон радиоактивного распада
- Нуклонная модель ядра. Заряд ядра. Массовое число ядра
- Энергия связи нуклонов в ядре. Ядерные силы
- Ядерные реакции. Деление и синтез ядер
- Основные формулы по теме «Физика атомного ядра»
Радиоактивность. Альфа-распад. Бета-распад. Гамма-излучение
Радиоактивность – способность некоторых атомных ядер самопроизвольно превращаться в другие ядра с испусканием различных видов радиоактивных излучений.
Виды радиоактивности:
- естественная радиоактивность – это радиоактивность, которая наблюдается у неустойчивых изотопов, существующих в природе и имеющих в таблице Менделеева порядковый номер больше 83;
- искусственная радиоактивность – это радиоактивность, которая наблюдается у изотопов, полученных посредством ядерных реакций в лабораторных условиях.
Явление естественной радиоактивности открыл в 1896 году французский физик А. Беккерель. Проводя опыты с солями урана, он заметил, что они самопроизвольно испускают лучи неизвестной природы, которые проходят через бумагу, дерево, металлические пластины и делают воздух проводником электричества.
Радиоактивность данного химического элемента не зависит от того, является ли химический элемент чистым или входит в состав какоголибо химического соединения. Радиоактивность не зависит от внешних условий: температуры, освещения, давления. Это означает, что радиоактивность представляет собой внутреннее свойство атомов радиоактивного элемента.
Виды радиоактивных излучений
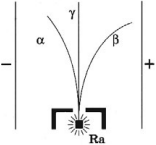
Излучение радиоактивных веществ имеет сложный характер и состоит из трех видов излучений. Если радиоактивное излучение пропустить через электрическое и магнитное поля, то оно распадается на три части, две из них отклоняются в противоположные стороны, а третий не отклоняется.
- ( alpha )-излучение представляет собой ядра атомов гелия ( {}^4_2He ), движущиеся со скоростью 107 м/с, несет положительный заряд;
- ( beta )-излучение представляет собой поток быстрых электронов, движущихся со скоростями, близкими к скорости света, несет отрицательный заряд;
- ( gamma )-излучение представляет собой электромагнитное излучение с длиной волны 10-12 м, заряда не имеет.
При одинаковой энергии частиц разные виды излучений неодинаково взаимодействуют с веществом.
Вследствие сильного ионизирующего действия глубина проникновения ( alpha )-частиц в твердых телах обычно очень мала. ( beta )-частицы менее эффективно взаимодействуют с атомами вещества, поэтому их проникающая способность больше, чем у ( alpha )-частиц. ( gamma )-кванты взаимодействуют с электронными оболочками атомов и имеют самую большую проникающую способность. Для защиты от ( gamma )-излучения необходимы защитные стены или оболочки толщиной несколько десятков сантиметров или даже метров.
Радиоактивный распад – самопроизвольный распад атомов радиоактивного вещества, в результате которого ядра одних химических элементов превращаются в ядра других химических элементов.
Превращения атомных ядер, которые сопровождаются испусканием ( alpha )- и ( beta )-частиц, называются соответственно ( alpha )— и ( beta )-распадом. Термина «( gamma )-распад» не существует, так как ( alpha )— и ( beta )-распад сопровождаются γ-излучением.
Распадающееся ядро Х называется материнским ядром, ядро продукта распада Y – дочерним ядром.
Правила радиоактивного смещения
Это правила, позволяющие установить, какое ядро возникает в результате распада данного материнского ядра.
- ( alpha )-распад:
Если при радиоактивном превращении испускаются ( alpha )-частицы, то в результате такого превращения образуется ядро элемента, находящегося в таблице Менделеева на две клетки раньше исходного ядра плюс ядро атома гелия ( {}^4_2He ) (или ( alpha )-частица):
- ( beta )-распад.
Если при радиоактивном превращении испускаются ( beta )-частицы, то в результате такого превращения образуется ядро элемента, находящегося в таблице Менделеева:
– при ( beta^- )-распаде в следующей после исходного ядра клетке плюс электрон и антинейтрино (частица, не имеющая заряда и масса покоя которой равна нулю):
– при ( beta^+ )-распаде в предшествующей исходному ядру клетке плюс позитрон и нейтрино (частица, не имеющая заряда и масса покоя которой равна нулю):
( gamma )-излучение сопровождает ( alpha )- и ( beta )-распады, а также возникает при ядерных реакциях, торможении частиц, их распаде и т. д.
( gamma )-излучение испускается дочерним ядром, которое в момент своего образования оказывается в возбужденном состоянии, а затем переходит в невозбужденное состояние.
Спектр ( gamma )-излучения является линейчатым.
Биологическое действие радиоактивных излучений
При облучении вещества ( alpha )-, ( beta )-, ( gamma )-частицами происходит возбуждение или ионизация атомов вещества. При этом сами частицы могут тормозиться, что сопровождается рентгеновским излучением. Кроме того, частицы могут упруго или неупруго соударяться с атомами вещества. Все это может привести к изменению свойств облучаемого вещества и к отрицательному воздействию на живые организмы. Вредное действие излучений на организм связано с образованием свободных химических радикалов и с мутацией в клетках, которые могут оказывать влияние на потомство, приводить к лучевой болезни и образованию злокачественных опухолей.
Методы защиты от внешнего радиоактивного облучения:
- удаление от источника излучения на большое расстояние;
- ограничение времени пребывания на загрязненной местности или вблизи радиоактивных источников;
- ограждение радиоактивных источников экранами из материалов, эффективно поглощающих радиоактивные излучения (графит, свинец, кадмий, бор).
Методы защиты от внутреннего радиоактивного облучения:
- дозиметрический контроль воздуха, осадков в близлежащей местности;
- дозиметрический контроль продуктов питания;
- применение веществ, ослабляющих воздействие радиоактивных излучений на организм.
В дозиметрии различают поглощенную и эквивалентную дозы.
Поглощенная доза равна энергии радиоактивного излучения, поглощенного единицей массы вещества.
Обозначение – ( D ), единица измерения в СИ – грей (Гр).
где ( E ) – энергия излучения; ( m ) – масса вещества.
Для характеристики биологического воздействия на организм используется коэффициент качества излучения ( (k) ), или коэффициент относительной биологической активности.
( k ) = 1 для ( gamma )-квантов, ( k ) = 3 для тепловых нейтронов, ( k ) = 10 для нейтронов с энергией порядка 0,5 МэВ.
Эквивалентная доза равна произведению коэффициента качества излучения и поглощенной дозы.
Обозначение – ( H ), единица измерения в СИ – зиверт (Зв).
1 зиверт – это эквивалентная доза, при которой поглощенная доза равна 1 Гр при коэффициенте качества, равном 1.
Естественный фон составляет 2 мЗв за год.
Предельно допустимая доза – 5 мЗв за год.
При дозе 0,5 Зв наступает острое лучевое поражение организма.
При дозе 3–5 Зв – смертельный исход.
Допустимая доза облучения за среднее время жизни человека (70 лет) составляет 0,35 Зв.
Закон радиоактивного распада
Если имеется большое количество одинаковых радиоактивных ядер, то вероятность распада каждого из них в любой момент времени одинакова. Радиоактивный распад любого ядра является случайным процессом, поэтому момент его распада предсказать невозможно.
Однако для большого числа частиц, находящихся в образце вещества, выполняется статистический закон радиоактивного распада.
Закон радиоактивного распада:
число нераспавшихся атомных ядер при естественном радиоактивном распаде экспоненциально уменьшается с течением времени.
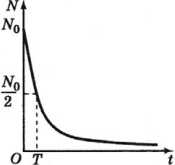
Период полураспада – это время, в течение которого распадается половина способных к распаду ядер.
В начальный момент времени ( t ) = 0, число атомных ядер ( N_0 ).
Через промежуток времени, равный периоду полураспада ( t=T_{1/2} ), число атомных ядер ( N=frac{N_0}{2} ).
Через промежуток времени, равный двум периодам полураспада ( t=2T_{1/2} ), число атомных ядер ( N=frac{N_0}{4}=frac{N_0}{2^2} ).
Через промежуток времени, равный ( n ) периодам полураспада ( t=nT_{1/2} ), число атомных ядер ( N=frac{N_0}{2^n} ).
где ( N ) – число нераспавшихся атомных ядер к моменту времени ( t ); ( N_0 ) – начальное число атомных ядер; ( T_{1/2} ) – период полураспада.
На рисунке период полураспада соответствует времени, в течение которого число радиоактивных ядер (активность) уменьшается вдвое.
Нуклонная модель ядра. Заряд ядра. Массовое число ядра
Элементарные частицы:
- протон
Обозначение – ( p ), заряд ( q_p ) = 1,6·10-19 Кл, масса ( m_p ) = 1,67·10-27 кг. - нейтрон
Обозначение – ( n ), заряд отсутствует, масса ( m_n ) = 1,66·10-27 кг. - электрон
Обозначение – ( e ), заряд ( q_e ) = –1,6·10-19 Кл, масса ( m_e ) = 9,1·10-31 кг.
Нуклон – это частица, входящая в состав атомного ядра.
Атомное ядро любого химического элемента состоит из протонов и нейтронов.
Массовое число – это число, которое определяет количество протонов и нейтронов в ядре и равно округленному до целого значению массы атомного ядра в а.е.м.
Обозначение – ( A ), единица измерения – 1 атомная единица массы (а.е.м.).
Массовое число равно сумме количества протонов и нейтронов в ядре:
где ( A ) – массовое число; ( Z ) – количество протонов в ядре; ( N ) – количество нейтронов в ядре.
Зарядовое число – это число, которое показывает количество протонов в ядре.
Зарядовое число равно сумме зарядов протонов, входящих в состав ядра, выраженной в элементарных электрических зарядах.
Элементарный электрический заряд равен заряду электрона:
( Z ) – порядковый номер химического элемента в периодической таблице Менделеева.
Если некоторый химический элемент обозначить ( {}^A_ZX ), это означает, что в его ядре ( Z ) – протонов и ( N=A-Z ) – нейтронов.
Измерения массы атомов показали, что практически все химические элементы имеют изотопы.
Изотопы – это атомы одного и того же химического элемента, имеющие одинаковое количество протонов, но отличающиеся количеством нейтронов в ядре.
Изотопы имеют:
- одинаковый атомный номер ( Z ) (одинаковое число протонов);
- различные массовые числа ( A ) (различное число нуклонов);
- одинаковое строение электронных оболочек;
- близкие химические свойства.
Изотопы бывают:
- стабильные – это изотопы, которые сохраняются сколь угодно долго;
- радиоактивные – это изотопы, которые превращаются в ядра других элементов с течением времени.
Изотопы водорода: водород имеет два стабильных изотопа – водород ( {}^1_1H ), дейтерий ( {}^2_1H ) и один радиоактивный изотоп тритий ( {}^3_1H ).
Энергия связи нуклонов в ядре. Ядерные силы
Между нуклонами ядра действуют самые мощные силы природы – ядерные силы.
Ядерные силы – это силы притяжения, связывающие протоны и нейтроны в атомном ядре и обеспечивающие существование устойчивых ядер.
Свойства ядерных сил:
- являются силами притяжения;
- являются короткодействующими силами (действуют на малых расстояниях, не превышающих 2·10-15 м; на таком расстоянии ядерные силы больше кулоновских приблизительно в 100 раз);
- обладают свойством зарядовой независимости (ядерные силы, действующие между двумя протонами, двумя нейтронами и между протоном и нейтроном, одинаковы);
- имеют свойство насыщения (каждый нуклон взаимодействует только с ограниченным числом ближайших к нему нуклонов, а не со всеми нуклонами ядра);
- не являются центральными (не действуют по линии, соединяющей центры взаимодействующих нуклонов).
Массу ядра можно точно определить с помощью масс-спектрографов, которые разделяют заряженные частицы с разными удельными зарядами с помощью электрических и магнитных полей.
Опытным путем было установлено, что благодаря действию сил притяжения масса ядра всегда меньше суммы масс протонов и масс нейтронов, входящих в состав этого ядра:
где ( M ) – масса ядра.
Дефект масс – это величина, равная разности суммы масс входящих в ядро нуклонов и массы ядра:
где ( Delta m ) – дефект масс.
Благодаря ядерным силам ядра атомов обладают огромной энергией связи.
Энергия связи – это энергия, которую необходимо затратить, чтобы разделить ядро на составляющие его нуклоны, или энергия, которая выделяется при образовании ядра из отдельных нуклонов:
где ( Delta E_{св} ) – энергия связи, ( c ) – скорость света.
Если в формуле энергии связи массы протона и нейтрона выражены в килограммах, а скорость света – в метрах в секунду, то энергия связи будет измерена в джоулях. Однако в физике атома и атомного ядра энергию ядер и элементарных частиц чаще выражают в мегаэлектронвольтах (МэВ).
Энергетический эквивалент 1 а.е.м.
Поэтому энергию связи можно рассчитать следующим образом:
В этом случае энергия связи измеряется в мегаэлектронвольтах (МэВ).
Для характеристики прочности ядра используется величина, которая называется удельной энергией связи.
Удельная энергия связи – это энергия связи ядра, приходящаяся на один нуклон ядра:
где ( A ) – массовое число.
Удельная энергия связи неодинакова для разных химических элементов и даже для изотопов одного и того же химического элемента. Удельная энергия связи нуклона в ядре меняется в среднем в пределах от 1 МэВ у легких ядер до 8,6 МэВ у ядер средней массы (с массовым числом ( A ) ≈ 100). У тяжелых ядер (( A ) ≈ 200) удельная энергия связи нуклона меньше, чем у ядер средней массы, приблизительно на 1 МэВ, так что их превращение в ядра среднего веса (деление на 2 части) сопровождается выделением энергии в количестве около 1 МэВ на нуклон, или около 200 МэВ на ядро. Превращение легких ядер в более тяжелые ядра дает еще больший энергетический выигрыш в расчете на нуклон.
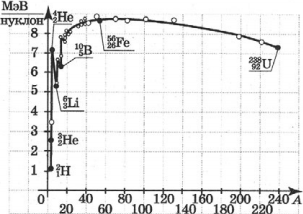
Зависимость удельной энергии связи от массового числа установили экспериментально. Из рисунка хорошо видно, что, не считая самых легких ядер, удельная энергия связи примерно постоянна и равна 8 МэВ/нуклон. Отметим, что энергия связи электрона и ядра в атоме водорода, равная энергии ионизации, почти в миллион раз меньше этого значения. Кривая на рисунке имеет слабо выраженный максимум. Максимальную удельную энергию связи (8,6 МэВ/нуклон) имеют элементы с массовыми числами от 50 до 60, т. е. железо и близкие к нему по порядковому номеру элементы. Ядра этих элементов наиболее устойчивы.
У тяжелых ядер удельная энергия связи уменьшается за счет возрастающей с увеличением ( Z ) кулоновской энергии отталкивания протонов. Кулоновские силы стремятся разорвать ядро.
Ядерные реакции. Деление и синтез ядер
Атомные ядра при взаимодействиях испытывают превращения. Эти превращения сопровождаются увеличением или уменьшением кинетической энергии участвующих в них частиц.
Ядерные реакции – это изменения атомных ядер при взаимодействии их с элементарными частицами или друг с другом.
Ядерные реакции происходят, когда частицы вплотную приближаются к ядру и попадают в сферу действия ядерных сил. Одноименно заряженные частицы отталкиваются друг от друга, поэтому сближение положительно заряженных частиц с ядрами (или ядер друг с другом) возможно, если этим частицам (или ядрам) сообщена достаточно большая кинетическая энергия. Эта энергия сообщается протонам, ядрам дейтерия, α-частицам и другим более тяжелым ядрам с помощью ускорителей.
Для осуществления ядерных реакций такой метод гораздо эффективнее, чем использование ядер гелия, испускаемых радиоактивными элементами. Во-первых, с помощью ускорителей частицам может быть сообщена энергия порядка 105 МэВ, т. е. гораздо большая той, которую имеют ( alpha )-частицы (максимально 9 МэВ). Во-вторых, можно использовать протоны, которые в процессе радиоактивного распада не появляются (это целесообразно потому, что заряд протонов вдвое меньше заряда α-частиц, и поэтому действующая на них сила отталкивания со стороны ядер тоже в 2 раза меньше). В-третьих, можно ускорить ядра более тяжелые, чем ядра гелия.
Наиболее распространенный вид ядерной реакции:
где ( X ) и ( Y ) – исходное и конечное ядра; ( a ) и ( b ) – бомбардирующая и испускающая частицы.
Эндотермическая реакция – это реакция с поглощением энергии:
Экзотермическая реакция – это реакция с выделением энергии:
При ядерных реакциях выполняются следующие законы.
- Закон сохранения электрического заряда:
сумма электрических зарядов атомных ядер и частиц до реакции равна сумме электрических зарядов атомных ядер и частиц после реакции:
- Закон сохранения массового числа:
сумма нуклонов атомных ядер и частиц до реакции равна сумме нуклонов атомных ядер и частиц после реакции:
- Закон сохранения энергии.
Примеры ядерных реакций
- Первое наблюдавшееся превращение ядра (Ю. Резерфорд, 1919):
- Первая ядерная реакция на быстрых протонах (1932):
- Открытие нейтрона (Дж. Чедвик, 1932):
- Первое искусственное получение радиоактивного распада и открытие позитрона. Радиоактивный распад под действием ( alpha )-частиц наблюдал Ф. Жолио-Кюри:
Изотоп фосфора оказался радиоактивным: его ядро распадается с испусканием позитрона и нейтрино:
Классификация ядерных реакций
Ядерные реакции классифицируются:
- по роду участвующих в них частиц – реакции под действием нейтронов, заряженных частиц, ( gamma )-квантов;
- по энергии вызывающих их частиц – реакции при малых, средних, высоких энергиях;
- по роду участвующих в них ядер – реакции на легких ядрах (А < 50), средних ядрах (50 < А < 100) и тяжелых ядрах (А > 100);
- по характеру происходящих ядерных превращений – реакции с испусканием нейтронов, заряженных частиц, реакции захвата.
Деление ядер – это деление атомного ядра урана на несколько более легких ядер (осколков), чаще всего на два ядра, близких по массе.
- Делиться могут только ядра некоторых тяжелых элементов.
- При делении ядер испускаются нейтроны и ( gamma )-лучи.
- При делении ядер выделяется большая энергия.
Механизм деления ядер (капельная модель)
В тяжелых ядрах действуют значительные ядерные силы, которые удерживают ядро от распада. Под влиянием поглощенного нейтрона ядро возбуждается и начинает деформироваться, приобретая вытянутую форму. Оно растягивается до тех пор, пока силы отталкивания половинок ядра не начинают преобладать над силами притяжения, действующими в перешейке. В результате ядро разрывается на два осколка X и Y.
Под действием сил кулоновского отталкивания осколки разлетаются со скоростью, равной приблизительно 1/30 скорости света. Одновременно испускается излучение высокой частоты.
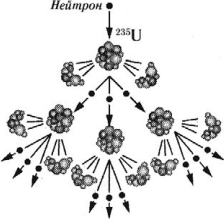
Цепная ядерная реакция – ядерная реакция деления тяжелых ядер нейтронами, в результате которой число нейтронов возрастает и поэтому может возникнуть самоподдерживающийся процесс деления.
В 1939 году было обнаружено, что при попадании нейтрона в ядро изотопа урана-235 происходит деление ядра на два или три осколка с испусканием 2–3 нейтронов:
Эти нейтроны способны вызвать деление 2–3 новых ядер урана с испусканием 4–9 новых нейтронов и т. д., процесс может продолжаться самостоятельно, вовлекая все большее число новых ядер.
Условия протекания цепной ядерной реакции:
- должны отсутствовать примеси, поглощающие нейтроны;
- количество вещества, способного делиться, должно быть достаточным для того, чтобы образующиеся нейтроны могли соударяться с другими ядрами, не покидая объем, не испытывая взаимодействия;
- скорость нейтронов должна быть достаточной, чтобы вызвать деление ядер.
Минимальное количество вещества, необходимое для осуществления цепной ядерной реакции, называется критической массой.
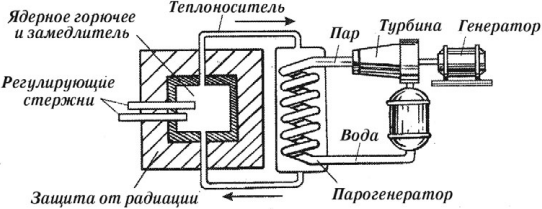
Устройства, в которых осуществляются управляемые цепные ядерные реакции, называются ядерными реакторами.
Основные элементы ядерного реактора:
- Ядерное горючее (сырьевые и делящиеся вещества в реакторах – изотопы урана, плутоний, торий).
- Замедлитель и отражатель нейтронов, которые способствуют увеличению числа медленных нейтронов, наиболее эффективных для развития цепной реакции деления (графит, тяжелая или обычная вода).
- Регулирующие стержни, которые вводят в активную зону реактора для поддержания стационарного режима реактора, так как быстрое развитие реакции сопровождается выделением большого количества тепла и перегревом реактора; стержни выполнены из материалов, сильно поглощающих тепловые нейтроны (из бора, кадмия).
- Теплоноситель, который необходим для отвода тепла, образующегося в реакторе (вода, жидкий натрий и др.).
- Защитные устройства, которые применяют для защиты персонала, обслуживающего реактор, от действия на организм нейтронных потоков и ( gamma )-лучей.
Термоядерный синтез
График зависимости удельной энергии связи нуклонов в ядре от массового числа показывает, что кроме реакции деления тяжелых ядер с выделением энергии идут реакции синтеза легких ядер.
Синтез ядер – это слияние ядер в одно ядро, сопровождающееся выделением энергии.
Для осуществления реакции синтеза легких ядер требуются высокие энергии сливающихся частиц, так как необходимо преодолеть кулоновское отталкивание. Этого можно достичь за счет высокой температуры вещества.
Термоядерная реакция – это реакция синтеза легких атомных ядер в более тяжелые, происходящая при сверхвысоких температурах (порядка 107 К и выше).
В природе термоядерные реакции происходят в недрах звезд.
При термоядерном синтезе энергетический выход на единицу массы топлива оказывается выше, чем при реакции деления тяжелых ядер урана.
Пример реакции синтеза:
Синтез гелия из тяжелых изотопов водорода – дейтерия и трития – происходит при температуре около 5·107 К.
При синтезе 1 г гелия из дейтерия и трития выделяется 4,2·1011 Дж – такая же энергия выделяется при сгорании 10 т дизельного топлива.
Термоядерный синтез может стать одним из возможных альтернативных источников энергии. Поиск таких источников энергии важен, так как запасы нефти и газа на Земле ограничены.
В настоящее время ведется испытание установок для осуществления управляемых термоядерных реакций синтеза гелия из водорода. Запасы водорода на Земле практически неисчерпаемы. Количество дейтерия в океанической воде составляет примерно 4·1011 т, чему соответствует энергетический запас 1017 МВт·год. Наиболее заманчивой является возможность извлечения энергии дейтерия, содержащегося в обычной воде.
Основные формулы по теме «Физика атомного ядра»
Физика атомного ядра
3.1 (61.75%) 137 votes