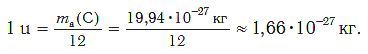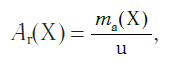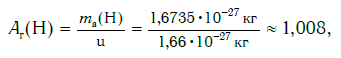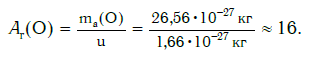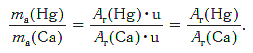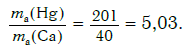Бронштейн М.П. Как был взвешен атом //Квант. — 1970. — № 2. — С. 26-35.
По специальной договоренности с редколлегией и редакцией журнала «Квант»
Предисловие
К концу прошлого века в физике и химии утвердилась, как тогда говорили, гипотеза об атомах и молекулах — мельчайших частицах, из которых составлены все тела окружающего нас мира. В химии атомная гипотеза позволила понять и очень удобно описывать химические реакции: всякая реакция — это просто соединение атомов в молекулы или, наоборот, разложение молекул на атомы или группы атомов. Из анализа состава различных молекул химики сумели выяснить, что атомы разных элементов обладают различными массами. Им даже удалось узнать, во сколько раз один атом тяжелее или легче другого; уже к началу второй половины XIX столетия были известны так называемые атомные веса всех открытых к тому времени химических элементов, то есть числа, показывающие, во сколько раз атом данного химического элемента тяжелее самого легкого из атомов — водорода. Знаменитый русский химик Д. И. Менделеев, расположив химические элементы в порядке возрастания атомных весов, показал в 1869 году, что они образуют определенную систему, в которой свойства элементов периодически повторяются (периодическая система). В физике гипотеза об атомах и молекулах играла не менее важную роль. Она позволила физикам составить себе ясное представление о множестве самых различных явлений. Она помогла понять, что такое тепло и холод, почему тела при нагревании расширяются, почему всякое вещество может быть твердым, жидким и газообразным и многое другое. Чтобы все это понять, нужно было только дополнительно предположить, что атомы и молекулы непрерывно и беспорядочно движутся и что между ними действуют силы притяжения и отталкивания. Но при всем этом атомы оставались только некоторым представлением в головах людей. Их не только никто не видел, потому что они очень малы, но никто не знал, насколько они малы, каковы массы атомов, сколько атомов в том или ином теле. Нельзя сказать, чтобы не делались попытки все это как-то узнать. Но эти попытки не приводили к убедительным результатам. У некоторых ученых появилась даже уверенность в том, что об атомах и молекулах ничего и нельзя будет узнать, потому что их на самом деле не существует. Эти ученые полагали, что атомы — это нечто вроде меридианов и параллелей на географической карте: ими удобно пользоваться, но реально в природе их нет. Физики, однако, не теряли надежду доказать реальность атомов и молекул, взвесить их, сосчитать их число, определить их размеры.
В предлагаемом отрывке из книги выдающегося советского физика-теоретика Матвея Петровича Бронштейна «Атомы, электроны, ядра» рассказывается о том, как впервые удалось измерить массу атомов и даже сосчитать их. Эта книга, изданная в 1935 году небольшим тиражом (всего 10 000 экземпляров), давно уже стала библиографической редкостью.
Публикацию подготовил профессор А.К. Кикоин. Сделанные им добавления взяты в прямые скобки.
Как был взвешен атом
… И в конце концов атом действительно удалось взвесить. Этому помогло одно очень странное явление, открытое еще в первой половине XIX века и на которое физики в свое время не обратили должного внимания. Это явление называется брауновским движением.
В 1828 году знаменитый английский ботаник Роберт Браун проделал одно в высшей степени интересное наблюдение. Испытывая только что присланный ему новый усовершенствованный микроскоп с ахроматическим объективом, Роберт Браун вздумал рассмотреть с помощью этого микроскопа ничтожную каплю жидкости, содержащуюся в крохотных зернышках пыльцы растений. В такой жидкости всегда имеется большее количество микроскопических твердых частиц. Как удивлен был Браун, когда увидел, что эти частицы не остаются на месте, а движутся, движутся непрерывно, точно исполняя какой-то фантастический танец! Когда в поле зрения микроскопа было видно много таких частиц, то получалось такое же впечатление, как от тучи каких-то мельчайших мошек. Твердые частицы микроскопических размеров, находящиеся в жидкости, движутся, как если бы они были живыми… Но уже Роберт Браун, который первым наблюдал это хаотическое движение микроскопических частиц, получившее свое название от его имени, пришел к другому заключению: частицы движутся не потому, что они живые… Так утверждал Браун, и это было подтверждено многочисленными последующими наблюдениями.
Можно было бы думать, что брауновское движение микроскопических частиц вызывается какими-то потоками в самой жидкости, связанными с разностью давлений в различных точках жидкости. Всякому приходилось наблюдать движение пылинок в воздухе, освещенном падающими сбоку солнечными лучами. Это движение действительно связано с такими токами воздуха, но брауновское движение имеет совершенно другой характер. В самом деле, если внимательно наблюдать за движением пылинок в солнечном луче, то легко заметить, что соседние пылинки, попавшие в одну и ту же небольшую струю воздуха, движутся в одну и ту же сторону. А если наблюдать за брауновским движением микроскопических частиц, то оказывается, что между направлением движения соседних частиц нет решительно ничего общего: частицы движутся совершенно независимо друг от друга, даже если им случается подойти друг к другу на самое крохотное расстояние, равное диаметру отдельной частички. Значит, совсем не от токов жидкости происходит это непостижимое и фантастическое движение микроскопических твердых частичек.
Во второй половине XIX века брауновское движение подробно исследовал французский физик Гуи. Он проделал целый ряд опытов, которые убедили его в том, что причина брауновского движения скрыта в самой жидкости. Не от внутренних токов жидкости, вызванных ничтожными разностями температур, и не от внешних толчков и сотрясений происходит брауновское движение. Гуи пробовал сравнивать брауновское движение в лаборатории, расположенной на шумной улице, цо которой проезжают тяжелые экипажи, с тем же брауновским движением, наблюдаемым ночью в глухом подвале в деревне. Разницы не получалось никакой. Толчки от экипажей заметны, но они сказываются не на хаотическом движении брауновских частиц, а на движении всей капельки, жидкости в целом: двигаясь, как целое, капелька увлекает за собой все частицы в одном и том же направлении, и это движение очень легко отличить от накладывающегося на него хаотического движения брауновских частиц, происходящего по всем возможным направлениям.
Гуи убедительно доказал, что брауновское движение, как уже предполагал и сам Браун, нисколько не связано с тем, что жидкость, в которой оно наблюдается, взята из живого существа — из растения: искусственно приготовленные жидкости с взвешенными в них микроскопическими частицами, в которых нет ничего живого, тоже обнаруживают брауновское движение. В 1881 году польский физик Бодашевский показал, что брауновское движение происходит и в газах, а не только в жидкостях.
Для того чтобы наблюдать брауновское движение, он рассматривал при боковом освещении микроскопические частички, образующие табачный дым. Крохотные частички угля, из которых состоит дым, плясали во все стороны совершенно таким же образом, как плясали твердые частички, наблюдавшиеся Робертом Брауном в жидкости.
Настоящую причину брауновского движения угадал в 70-х годах прошлого столетия бельгиец Карбонель. Его объяснение, гениальное по своей простоте, состоит в следующем: микроскопические частицы движутся потому, что они испытывают толчки со стороны невидимых молекул и атомов окружающей их жидкости. Рассматривая движение брауновских частичек, мы получаем некоторое представление о том, как движутся невидимые молекулы жидкости, совершенно таким же образом, как мы угадываем о волнении на море, когда, стоя далеко от берега, видим качание лодки, швыряемой волнами во все стороны. Брауновское движение является поэтому мостом, соединяющим невидимый мир атомов и молекул с миром, доступным восприятию при помощи наших органов чувств.
Почему брауновское движение можно наблюдать только в том случае, когда частички очень малы? Очень просто, отвечает на этот вопрос Карбонель; если поверхность частицы велика, то количество толчков, получаемых ею справа, всегда окажется приблизительно равным количеству толчков, получаемых ею же слева, и ничтожное различие в количестве толчков будет совершенно недостаточно для того, чтобы сдвинуть с места большую и тяжелую частицу. Если же частица имеет ничтожную массу и ничтожные размеры, то в хаосе молекулярных движений жидкости всегда может случиться, что с одной стороны частицы будет в данный момент случайно больше толчков, чем с другой, а поэтому легкоподвижная частица двинется в ту сторону, куда ее толкнут молекулы. Через какой-то очень короткий промежуток времени избыток молекулярных толчков будет сдвигать брауновскую частицу уже по другому направлению, еще через какой-то короткий промежуток времени — по третьему и т. д.
Если это предложенное Карбонелем объяснение правильно, то чем частицы легче и мельче, тем брауновское движение должно быть интенсивнее. Так и есть в действительности — уже Браун сумел это заметить. Кроме того, ведь мы знаем, что движение молекул жидкости происходит тем быстрее, чем выше температура; и в самом деле, Гуи нашел, что при повышении температуры брауновское движение делается все интенсивнее и интенсивнее. Когда Жигмонди изобрел ультрамикроскоп и смог наблюдать ничтожнейшие частицы золота в коллоидном растворе (диаметр частиц меньше миллионной доли сантиметра), то брауновское движение этих частиц оказалось таким быстрым, что получилось какое-то сплошное мелькание. Жигмонди описывает свое первое впечатление так: «Это какое-то непрерывное прыганье, пляска, скакание, столкновения и разлетания, так что трудно разобраться в этой путанице»…
Распределение зернышек по высоте в гуммигутовой эмульсии
Мы переходим теперь к рассказу о классических работах, которые сделал французский физик Жан Перрен (1908 г.). В этих работах было окончательно проверено и установлено,что брауновское движение в жидкостях вызвано движением молекул и тем самым дано решающее доказательство действительного существования молекул и атомов.
Перрен брал кусочки резиновой смолы «гуммигута» и растирал их рукой в воде, пока она не становилась ярко-желтого цвета. После этого Перрен брал немножко такой жидкости под микроскоп. Под микроскопом оказывалась, что гуммигут на самом деле не растворился в воде, а распался на множество шаровидных мелких зернышек, которые разбрелись по всему объему воды. Зернышки эти очень различны по размерам. А Перрену хотелось иметь такую жидкость, в которой были бы совершенно одинаковые по размерам частицы гуммигута. Для этого он воспользовался «центрифугой» (центробежной машиной), такой же самой, какой пользуются на крупных молочных фермах для отделения сливок от молока или же в медицинских лабораториях для удаления кровяных шариков из крови, после чего остается однородная жидкость — кровяная плазма. Центрифуга Перрена делала 2500 оборотов в минуту, и возникающая при этом центробежная сила выбрасывала из жидкости зернышки гуммигута. Перпендикулярно к оси центрифуги были расположены стеклянные пробирки, в которых содержалась эмульсия гуммигута (так называется вода с взвешенными в ней частичками гуммигута).
Первыми выпадали тяжелые частицы, а вслед за ними и легкие. Это давало возможность отделить частицы друг от друга по весу (а значит, и по размерам, потому что все частицы сделаны из одного и того же материала, и поэтому, чем больше их масса, тем больше и размеры).
Это очень кропотливая и тяжелая работа: приходится работать целый месяц для того, чтобы из одного килограмма гуммигута получить несколько десятых или даже сотых долей грамма круглых зерен нужной величины. Таким образом, Перрен сумел получить несколько порций эмульсии с диаметром зерен в 0,5, 0,46, 0,37, 0,21 и 0,14 микрона (микрон — это тысячная доля миллиметра).
С помощью таких эмульсий Жан Перрен произвел множество замечательных опытов, о которых мы здесь и расскажем. Он поместил каплю эмульсии с определенным диаметром зерен в плоскую ванночку (кюветку) с глубиной 0,1 мм. Кюветка была затем покрыта тонким покровным стеклышком, края которого были залиты парафином: таким образом, капля оказалась размазанной в сосуде, в котором она герметически заперта, так что никакое испарение уже невозможно.
Перрен сперва поставил свою кюветку набок и стал смотреть на нее в микроскоп. В поле зрения микроскопа оказалась тонкая вертикальная водяная стенка, внутри которой распределялись участвующие в брауновском движении зернышки гуммигута. Распределение зернышек сперва было однородным, но потом, с течением времени, распределение изменилось и в конце концов стало таким: очень много зернышек внизу, а по мере продвижения вверх их становится все меньше и меньше (см. рисунок). Число зернышек в одном кубическом микроне уменьшается с увеличением высоты и притом по некоторому вполне определенному закону.
Этот закон уменьшения плотности эмульсии с высотой Перрен захотел исследовать. Для этого он положил кюветку на дно, и после того как частицы расположились по высоте подобно тому, как в кювете, стоящей вертикально, стал смотреть на кюветку сверху в микроскоп, имевший очень маленькую глубину поля зрения: в микроскоп было видно все, что происходит в тонком слое глубиной в один микрон. Передвигая микроскоп вверх и вниз, можно было помещать этот слой то выше, то ниже. Перрен стал работать так: поставил микроскоп на какой-то высоте и начал считать, сколько зернышек виднеется в поле зрения на этой высоте, затем передвинул микроскоп на новую высоту и снова сосчитал число зернышек и т. д. Заметим, что при этом числом зернышек считается среднее из нескольких наблюдений, потому что зернышки движутся совершенно хаотически и, следовательно, их число в поле зрения микроскопа бывает то больше, то меньше в зависимости от случая. Поэтому на одной и той же высоте Перрен производил подсчет зернышек много раз и затем уже вычислял значение, характерное для каждой такой высоты.
Фотографии гуммигутовой эмульсии, сделанные Ж. Перреном через микроскоп
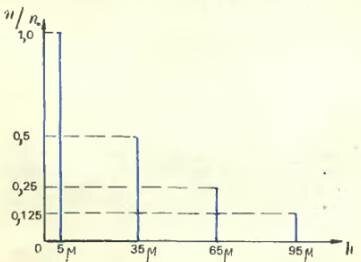
Приведем результаты одного из опытов Перрена. Глубина кюветки была, как мы уже говорили, 100 микрон (то есть 0,1 мм). Отсчеты производились на высотах 5, 35, 65 и 95 микрон над уровнем донышка кюветки. Оказалось, что среднее число частиц на высоте 35 микрон составляет половину того, которое было на высоте 5 микрон, число частиц на высоте 65 микрон было равно половине числа частиц на высоте 35 микрон, а число частиц на высоте 95 микрон равнялось половине числа частиц на высоте 65 микрон. Иными словами, при поднятии вверх на каждые 30 микрон число частиц в данном объеме (соответствующем глубине и ширине выбранного поля зрения) уменьшалось вдвое. Поэтому математический закон убывания плотности (числа частиц в данном объеме, а значит, и в каждой единице объема) с высотой может быть словами выражен так: если высоты образуют арифметическую прогрессию, то числа зерен образуют геометрическую прогрессию.
Результаты опытов Перрена
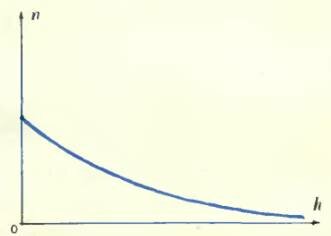
Такой закон убывания плотности зерен с высотой должен был сильно поразить и заинтересовать Перрена: ведь по такому же самому закону спадает плотность при поднятии в нашей атмосфере. Блэз Паскаль, знаменитый французский ученый, живший в XVII столетии и впервые применивший к изучению атмосферы барометр, изобретенный итальянцем Торричелли, обнаружил закон, по которому спадает с увеличением высоты плотность атмосферного воздуха. Этот закон, получивший название барометрической формулы, гласит то же самое: плотность каждого из газов, составляющих атмосферу, убывает вместе с увеличением высоты в геометрической прогрессии.
Так изменяется количество молекул воздуха с высотой
[Закон этот можно выразить и математически, в виде формулы.
Предположим, что на какой-то высоте h0 над Землей в каждом кубическом сантиметре содержится n0 молекул какого-то газа. На какой-то другой, большей высоте h таких же молекул в одном кубическом сантиметре будет, конечно, меньше, например n. Тогда барометрическая формула может быть записана в таком виде:
(~lg frac{n_0}{n} = Amg (h — h_0)) [1]. (1)
Здесь А — это некоторая постоянная величина, одинаковая для всех газов (при данной температуре), а m — масса молекулы того газа, о котором идет речь, g — ускорение силы тяжести.
Сразу видно, что в левой части равенства стоит отношение чисел частиц в единице объема (правда, под знаком логарифма), а в правой — разность высот. Это и означает, что если высоты образуют арифметическую прогрессию, то числа частиц образуют прогрессию геометрическую.
Выберем такую разность высот h — h0, чтобы число частиц n на высоте h было вдвое меньше числа частиц n0 на высоте h0. Тогда формула (1) примет вид
(~lg 2 = Amg (h — h_0)) . (2)
В таблице логарифмов легко найти, что lg 2 = 0,30103, так что
(~0,30103 = Amg (h — h_0)) . (3)
Если бы было известно численное значение постоянной А, то, подсчитав число частиц в единице объема n и n0 на высотах h и h0, легко было бы вычислить и массу молекулы m, то есть взвесить ее. Правда, сосчитать молекулы мы тоже не можем, но ведь нам и не надо знать каждое из чисел n и n0 в отдельности. Нужно знать только их отношение. А его легко найти, если измерить барометром давления на высотах h и h0: отношение давлений как раз и равно отношению чисел частиц в единице объема. Но дело в том, что величина А во времена Перрена не была известна (именно опыты Перрена и позволили определить ее). Поэтому Перрен мог рассуждать так: известно, например, что] при поднятии на 5 км количество кислорода, находящегося в кубическом сантиметре, уменьшается вдвое; при поднятии на следующие 5 км оно уменьшается еще вдвое и т. д. и т. д. Это — тот же закон, по которому уменьшается с высотой число зернышек гуммигута в кубическом сантиметре эмульсии, но только здесь иные масштабы — вместо 30 микрон здесь мы имеем 5 км. Отчего же здесь получаются другие масштабы?
Слой гуммигутовой эмульсии в 100 микрон — это, в сущности, такая .же атмосфера, но только состоящая не из молекул кислорода или азота, а из зернышек гуммигута, которые уже достаточно велики, чтобы их можно было видеть в микроскоп. Вследствие большей массы этих зернышек (по сравнению с молекулами газа) уменьшение плотности с высотой происходит быстрее, чем в обыкновенной атмосфере, окружающей нашу Землю, а именно (в случае гуммигутовых зернышек диаметром 0,21 микрона) плотность уменьшается вдвое при поднятии на 30 микрон. «Эмульсия,— говорит Перрен, — это атмосфера в миниатюре, тяготеющая к Земле. В масштабе такой атмосферы высота Альп представилась бы несколькими микронами, а отдельные холмы стали бы равны молекулам». Для нас всего важнее, что молекулы этой миниатюрной «атмосферы» — зернышки гуммигута — могут быть взвешены, а это . позволяет вычислить и массу молекул обыкновенного газа. Так Перрен сумел сделать то, что казалось совершенно невозможным, — взвесить молекулы и атомы.
[Из формулы (3) видно, что произведение массы молекулы m на разность высот, между которыми число молекул в единице объема изменяется вдвое, во всех случаях (то есть для любых частиц) равно одной и той же величине (~frac{0,30103}{A}).
Поэтому, если для гуммигутовых зерен разность высот меньше, чем для кислорода в атмосфере, то это потому, что масса гуммигутового зернышка больше массы молекулы кислорода и как раз во столько раз, во сколько раз 5 км больше, чем 30 микрон.]
Проделаем нехитрый расчет… 5 км в 166 миллионов раз больше, чем 30 микрон. Значит, масса гуммигутового зернышка с диаметром 0,21 микрона превышает массу кислородной молекулы в 166 миллионов раз.
Сколько же весит такой гуммигутовый шарик? Это нетрудно рассчитать, если измерить предварительно массу кубического сантиметра гуммигута. При этом расчете не следует забывать, что в опытах Перрена зернышки гуммигута находились в воде, а значит, по закону Архимеда каждый кубический сантиметр гуммигута терял в весе ровно столько, сколько весит кубический сантиметр воды, то есть 1 г. Значит, каждый кубический сантиметр гуммигута был в воде на один грамм легче, чем в воздухе. В результате всех расчетов (которые мы пропускаем) получается, что масса зернышка (с поправкой на закон Архимеда) была равна 8,5·10-15 г. И она в 166 миллионов раз больше массы молекулы кислорода. Значит, масса молекулы кислорода равна 5,1·10-23 г. А так как молекула кислорода в 32 раза тяжелее атома водорода (молекулярный вес кислорода равен 32), то масса атома водорода — этого самого легкого из всех атомов — равна 1,6·10-24 г. В грамме водорода содержится, следовательно, 6·1023 атомов.
[Так атомы и молекулы были не только взвешены, но и сосчитаны!]
Эти цифры, найденные Перреном, позволили связать употреблявшуюся в то время единицу атомного веса — массу атома водорода — с граммом. Масса атома водорода, выраженная в граммах, получилась настолько ничтожной, что ее никак невозможно себе представить, тем не менее она получилась вполне определенной. Атом был взвешен. Важнейшая задача атомной физики была решена.
[Заметим здесь, что цифры, полученные Перреном, конечно, не очень точны. Впоследствии были найдены другие способы определения масс атомов и молекул, и теперь мы располагаем более правильными значениями масс. По современным данным масса атома водорода, например, равна 1,673·10-24 г, а молекулы кислорода — 5,314·10-23 г. Как видите, эти цифры не так уж сильно отличаются от тех, что впервые были получены Перреном.]
Вот какой результат получил Перрен, изучая распределение зернышек гуммигута в гуммигутовой эмульсии в зависимости от высоты. Но всего любопытнее то обстоятельство, что точно такой же результат был выведен с помощью тех же гуммигутовых шариков, но совершенно иным путем, о котором мы также скажем несколько слов.
Брауновское движение
Брауновское движение в гуммигутовой эмульсии совершается необыкновенно быстро. Нет никакой возможности проследить за движением отдельного гуммигутового зернышка. Поэтому Перрен и не пытался этого делать, а поступал следующим образом: он отмечал на чертеже положение гуммигутового зернышка через определенные промежутки времени, например через каждые 30 секунд, и полученные точки соединял прямыми линиями (хотя на самом деле гуммигутовое зернышко за это время двигалось не по прямой, а по причудливой ломаной линии). Полученные рисунки дают возможность судить о беспорядочности, хаотичности брауновского движения вообще. Но Перрен делал эти рисунки не только для того, чтобы получить наглядную иллюстрацию к брауновскому движению. Его интересовала количественная сторона дела. Знаменитый Альберт Эйнштейн, который был тогда еще молодым человеком, написал (в 1905 — 1906 годах) замечательные работы, где он вывел формулу, определяющую для заданного промежутка времени среднее смещение гуммигутового зернышка относительно его первоначального положения в жидкости. Мы не станем здесь приводить эту замечательную формулу, заметим только, что в эту формулу входит величина, равная числу атомов водорода в одном грамме. Поэтому, сравнивая формулу Эйнштейна с рисунками Перрена, определяющими перемещение частицы за 30 секунд, можно вычислить эту величину. Так и сделал Перрен, и у него получилось, что число атомов водорода в одном грамме равно 6·1023, то есть получилось такое же число, как и раньше.
Совпадение двух чисел, которые были получены совершенно различными способами, является лучшим доказательством правильности всех сделанных предположений. Значит; молекулы и атомы действительно существуют, а не только являются удобной для химиков выдумкой. Такое заключение вынуждены были сделать даже те, которые долго и упорно не хотели признавать существования атомов.
… Вековой спор между сторонниками и противниками атомов закончился, таким образом, победой сторонников атомной теории. И в настоящее время мы можем с уверенностью утверждать, что все вещи на свете — и вода, и камни, и растения, и животные, и воздух, и железо и т. д. и т. д.— все это состоит из мельчайших невидимых глазу атомов.
Задачи к статье
- Пользуясь приведенными в статье данными, найдите, на какой высоте давление уменьшается вдвое. Воздух легче кислорода в отношении 28,8 : 32.
- P0 — давление воздуха на уровне моря, P1 — на высоте h. Каково давление воздуха на высотах: 2h, 3h, nh? Считать, что температура воздуха и ускорение свободного падения не меняются с высотой, и поэтому постоянная А не зависит от высоты.
- Найдите высоту над поверхностью Земли, где давление воздуха равно 0,25 и 0,125 атмосферного. Постройте кривую зависимости давления воздуха от высоты.
Ответы
- 5,55 км.
-
(~P_2 = P_1 left( frac{P_1}{P_0} right)) ,
-
(~P_3 = P_2 left( frac{P_1}{P_0} right) P_1 left( frac{P_1}{P_0} right)^2) ,
-
(~P_n = P_1 left( frac{P_1}{P_0} right)^{n — 1}) .
-
- 11,1 км; 16,65 км. Удобно воспользоваться результатом задачи 1. Давление пропорционально плотности воздуха.
Примечания
-
↑ Если k — это число «шагов», за которое мы поднимаемся на высоту h, а Δh — высота «шага», то (~h = h_0 + (k — 1) Delta h), а (~n = n_0 left( frac 1q right)^{k — 1}), где (~frac 1q) — знаменатель прогрессии, которую составляет плотность газа (q > 1). Из этих двух формул, исключив k, мы найдем, что
(~lg frac{n_0}{n} = frac{lg q}{Delta h} (h — h_0)) . (*)
Аналогичную формулу можно записать и для другого газа; величины, относящиеся к нему, мы снабдим штрихом:
(~lg frac{n’_0}{n’} = frac{lg q’}{Delta h’} (h’ — h’_0)) . (**)
Очень важным оказывается то обстоятельство, что, если плотности первого и второго газов уменьшились в одно и то же число раз, то есть (~frac{n_0}{n} = frac{n’_0}{n’}), то отношение разностей высот, при которых это произошло, (~frac{h — h_0}{h’ — h’_0}) в точности равно обратному отношению масс молекул этих газов:
(~frac{h — h_0}{h’ — h’_0} = frac{m’}{m}) .
Разделим почленно уравнение (*) на уравнение (**):
(~1 = frac{lg q (h — h_0)Delta h’}{lg q’ (h’ — h’_0)Delta h} ) , или
(~frac{lg q}{lg q’} = frac{Delta h m}{Delta h’ m’} ) .
Таким образом, (~lg q sim Delta h m). Это дает возможность записать, что
(~lg q = A_1 Delta h m) .
где A1 — это некоторая постоянная величина, не зависящая от величины шага и одинаковая для всех газов (при данной температуре).
Теперь барометрическую формулу (*) мы можем записать в таком виде:
(~lg frac{n_0}{n} = A_1mg (h — h_0)) .
ОТНОСИТЕЛЬНАЯ АТОМНАЯ МАССА. Английский ученый Джон Дальтон (1766–1844) на своих лекциях демонстрировал студентам выточенные из дерева модели атомов, показывая, как они могут соединяться, образуя различные вещества. Когда одного из студентов спросили, что такое атомы, он ответил: «Атомы – это раскрашенные в разные цвета деревянные кубики, которые изобрел мистер Дальтон».
Конечно, Дальтон прославился не своими «кубиками» и даже не тем, что в двенадцатилетнем возрасте стал школьным учителем. С именем Дальтона связано возникновение современной атомистической теории. Впервые в истории науки он задумался о возможности измерения масс атомов и предложил для этого конкретные способы. Понятно, что непосредственно взвесить атомы невозможно. Дальтон рассуждал только о «соотношении весов мельчайших частиц газообразных и других тел», то есть об относительных их массах. И поныне, хотя масса любого атома в точности известна, ее никогда не выражают в граммах, так как это исключительно неудобно. Например, масса атома урана – самого тяжелого из существующих на Земле элементов – составляет всего 3,952·10–22 г. Поэтому массу атомов выражают в относительных единицах, показывающих, во сколько раз масса атомов данного элемента больше массы атомов другого элемента, принятого в качестве стандарта. Фактически это и есть «соотношение весов» по Дальтону, т.е. относительная атомная масса.
В качестве единицы массы Дальтон принял массу атома водорода, а для нахождения масс других атомов он использовал найденные разными исследователями процентные составы различных соединений водорода с другими элементами. Так, по данным Лавуазье, в воде содержится 15% водорода и 85% кислорода. Отсюда Дальтон нашел относительную атомную массу кислорода – 5,67 (в предположении, что в воде на один атом водорода приходится один атом кислорода). По данным английского химика Уильяма Остина (1754–1793) о составе аммиака (80% азота и 20% водорода) Дальтон определил относительную атомную массу азота, равную 4 (также в предположении о равном числе атомов водорода и азота в этом соединении). А из данных по анализу некоторых углеводородов Дальтон приписал углероду значение 4,4. В 1803 Дальтон составил первую в мире таблицу относительных атомных масс некоторых элементов. В дальнейшем эта таблица претерпела очень сильные изменения; основные из них произошли еще при жизни Дальтона, что видно из следующей таблицы, в которой приведены данные из учебников, изданных в разные годы, а также в официальном издании ИЮПАК – Международного союза теоретической и прикладной химии (International Union of Pure and Applied Chemistry).
| Таблица 1. | |||||
| Элемент | Н | Не | С | N | О |
| Дальтон, 1803 | 1 | – | 4,5 | 4 | 5,66 |
| Бецелиус, 1826 | 1 | – | 12,26 | 14,18 | 16,02 |
| Жерар, 1842 | 1 | – | 12 | 14 | 16 |
| Менделеев, 1906 | 1,008 | 4,0 | 12,0 | 14,04 | 16,000 |
| Бьеррум, 1933 | 1,007 | 4,002 | 12,0 | 14,008 | 16,0000 |
| Сиборг, 1945 | 1,008 | 4,003 | 12,010 | 14,008 | 16,000 |
| ИЮПАК, 1993 | 1,00794 | 4,002602 | 12,011 | 14,00674 | 15,9994 |
Прежде всего, обращают на себя внимание непривычные атомные массы у Дальтона: они в несколько раз отличаются от современных! Это объясняется двумя причинами. Первая – неточность эксперимента в конце 18 – начале 19 в. Когда Гей-Люссак и Гумбольдт уточнили состав воды (12,6% Н и 87,4% О), Дальтон изменил значение атомной массы кислорода, приняв ее равной 7 (по современным данным в воде 11,1% водорода). По мере совершенствования методов измерения уточнялись атомные массы и многих других элементов. При этом за единицу измерения атомных масс сначала выбирали водород, потом – кислород, а в настоящее время – углерод.
Вторая причина более серьезная. Дальтон не знал, в каком соотношении находятся атомы разных элементов в различных соединениях, поэтому он принял наиболее простую гипотезу о соотношении 1:1. Так считали многие химики, пока не были надежно установлены и приняты химиками правильные формулы для состава воды (Н2О) и аммиака (NH3), многих других соединений. Для установления формул газообразных веществ использовался закон Авогадро, позволяющий определять относительную молекулярную массу веществ. Для жидких и твердых веществ использовали другие способы (см. МОЛЕКУЛЯРНОЙ МАССЫ ОПРЕДЕЛЕНИЕ). Особенно просто было устанавливать формулы соединений элементов переменной валентности, например, хлорида железа. Относительная атомная масса хлора уже была известна из анализа ряда его газообразных соединений. Теперь, если принять, что в хлориде железа число атомов металла и хлора одинаково, то для одного хлорида относительная атомная масса железа получалась равной 27,92, а для другого – 18,62. Отсюда следовало, что формулы хлоридов FeCl2 и FeCl3, и Ar(Fe) = 55,85 (среднее из двух анализов). Вторая возможность – формулы FeCl4 и FeCl6, и Ar(Fe) = 111,7 – была исключена как маловероятная. Относительные атомные массы твердых веществ помогало находить эмпирическое правило, сформулированное в 1819 французскими учеными П.И.Дюлонгом и А.Т.Пти: произведение атомной массы на теплоемкость – величина постоянная. Особенно хорошо правило Дюлонга – Пти выполнялось для металлов, что позволило, например, Берцелиусу уточнить и исправить атомные массы некоторых из них.
При рассмотрении относительных атомных масс химических элементов, приводящихся в периодической таблице, можно заметить, что для разных элементов они даются с разной точностью. Например, для лития – с 4 значащими цифрами, для серы и углерода – с 5, для водорода – с 6, для гелия и азота – с 7, для фтора – с 8. Отчего такая несправедливость?
Оказывается, точность, с которой определяется относительная атомная масса данного элемента, зависит не столько от точности измерений, сколько от «природных» факторов, не зависящих от человека. Они связаны с непостоянством изотопного состава данного элемента: в разных образцах соотношение изотопов не вполне одинаковое. Например, при испарении воды молекулы с легкими изотопами (см. ЭЛЕМЕНТЫ ХИМИЧЕСКИЕ) водорода переходят в газовую фазу чуть быстрее, чем молекулы тяжелой воды, содержащие изотопы 2Н. В результате в водяных парах изотопа 2Н немного меньше, чем в жидкой воде. Многие организмы также разделяют изотопы легких элементов (для них разница в массах более существенна, чем для тяжелых элементов). Так, при фотосинтезе растения отдают предпочтение легкому изотопу 12С. Поэтому в живых организмах, а также произошедших от них нефти и угле содержание тяжелого изотопа 13С понижено, а в углекислом газе и образовавшемся из него карбонатах, наоборот, – повышено. Микроорганизмы, восстанавливающие сульфаты, также накапливают легкий изотоп 32S, поэтому в осадочных сульфатах его больше. В «остатках» же, не усвоенных бактериями, доля тяжелого изотопа 34S больше. (Кстати, анализируя соотношение изотопов серы, геологи могут отличить осадочный источник серы от магматического. А по соотношению изотопов 12С и 13С можно даже отличить тростниковый сахар от свекловичного!)
Итак, для многих элементов приводить очень точные значения атомных масс просто не имеет смысла, поскольку они немного меняются от одного образца к другому. По точности, с какой приводятся атомные массы, можно сразу сказать, происходит ли в природе «разделение изотопов» данного элемента и насколько сильно. А вот, например, для фтора атомная масса приводится с очень высокой точностью; значит, атомная масса фтора в любом его земном источнике постоянна. И это неудивительно: фтор относится к так называемым элементам-одиночкам, которые в природе представлены одним-единственным нуклидом.
В периодической таблице массы некоторых элементов стоят в скобках. Это относится главным образом к актинидам, стоящим после урана (так называемые трансурановые элементы), к еще более тяжелым элементам 7-го периода, а также к нескольким более легким; среди них технеций, прометий, полоний, астат, радон, франций. Если сравнить таблицы элементов, напечатанные в разные годы, то окажется, что эти числа время от времени меняются, иногда в течение всего нескольких лет. Некоторые примеры приведены в таблице.
Причина изменений в таблицах заключается в том, что указанные элементы радиоактивны, у них нет ни одного стабильного изотопа. В таких случаях принято приводить либо относительную атомную массу наиболее долгоживущего нуклида (например, для радия), либо массовые числа; последние приводятся в скобках. Когда открывают новый радиоактивный элемент, то получают вначале лишь один из многих его изотопов – конкретный нуклид с определенным числом нейтронов. Исходя из теоретических представлений, а также экспериментальных возможностей, стараются получить нуклид нового элемента с достаточным временем жизни (с таким нуклидом легче работать), однако удавалось это «с первого захода» не всегда. Как правило, при дальнейших исследованиях выяснялось, что существуют и могут быть синтезированы новые нуклиды с бoльшим временем жизни, и тогда проставленное в Периодической таблице элементов Д.И.Менделеева число надо было заменять. Сопоставим массовые числа некоторых трансуранов, а также прометия, взятые из книг, изданных в разные годы. В скобках в таблице приведены современные данные для периодов полураспада. В старых изданиях вместо принятых в настоящее время символов элементов 104 и 105 (Rf – резерфордий и Db – дубний) фигурировали Ku – курчатовий и Ns – нильсборий.
| Таблица 2. | ||||
| Элемент Z | Год издания | |||
| 1951 | 1958 | 1983 | 2000 | |
| Pm 61 | 147 (2,62 года) | 145 (18 лет) | 145 | 145 |
| Pu 94 | 239 (24100 лет) | 242 (3,76.105 лет) | 244 (8,2.107 лет) | 244 |
| Am 95 | 241 (432 года) | 243 (7370 лет) | 243 | 243 |
| Cm 96 | 242 (163 сут) | 245 (8500 лет) | 247 (1,58.107 лет) | 247 |
| Bk 97 | 243 (4,5 час) | 249 (330 сут) | 247 (1400 лет) | 247 |
| Cf 98 | 245 (44 мин) | 251 (900 лет) | 251 | 251 |
| Es 99 | – | 254 (276 сут) | 254 | 252 (472 сут) |
| Fm 100 | – | 253 (3 сут) | 257 (100,5 сут) | 257 |
| Md 101 | – | 256 (76 мин) | 258 (52 сут) | 258 |
| No 102 | – | – | 255 (3,1 мин) | 259 (58 мин) |
| Lr 103 | – | – | 256 (26 сек) | 262 (3,6 час) |
| Rf 104 | – | – | 261 (78 сек) | 261 |
| Db 105 | – | – | 261 (1,8 сек) | 262 (34 сек) |
Как видно из таблицы, все приведенные в ней элементы радиоактивные, их периоды полураспада намного меньше возраста Земли (несколько млрд. лет), поэтому в природе этих элементов нет и получены они искусственно. По мере совершенствования техники эксперимента (синтез новых изотопов и измерение времени их жизни) иногда удавалось найти нуклиды, живущие в тысячи и даже миллионы раз дольше известных до этого. Например, когда в 1944 на циклотроне в Беркли были поставлены первые опыты по синтезу элемента № 96 (впоследствии его назвали кюрием), то единственная имевшаяся тогда возможность получения этого элемента заключалась в облучении a-частицами ядер плутония-239: 239Pu + 4He ® 242Cm + 1n. Полученный нуклид нового элемента имел период полураспада около полугода; он оказался очень удобным компактным источником энергии, и позднее его использовали с этой целью, например, на американских космических станциях «Сервейор». В настоящее время получен кюрий-247, который имеет период полураспада 16 млн. лет, что в 36 млн. раз превышает время жизни первого известного нуклида этого элемента. Так что изменения, вносимые время от времени в таблицу элементов, могут быть связаны не только с открытием новых химических элементов!
В заключение – о том, как узнали, в каком соотношении присутствуют в элементе разные изотопы? Например, о том, что в природном хлоре на долю 35Cl приходится 75,77% (остальное – изотоп 37Cl)? В данном случае, когда в природном элементе всего два изотопа, решить задачу поможет такая аналогия.
В 1982 в результате инфляции стоимость меди, из которых чеканились одноцентовые монеты США, превысила номинал монеты. Поэтому с этого года монеты делают из более дешевого цинка и лишь сверху покрывают тонким слоем меди. При этом содержание дорогой меди в монете снизилось с 95 до 2,5%, а масса – с 3,1 до 2,5 г. Через несколько лет, когда в обращении находилась смесь монет двух типов, преподаватели химии сообразили, что эти монеты (на глаз они почти неразличимы) – прекрасное пособие для их «изотопного анализа», либо по массе, либо по числу монет каждого типа (аналогия массовой или мольной доли изотопов в смеси). Будем рассуждать так: пусть у нас имеется 210 монет, среди которых есть и легкие, и тяжелые (это соотношение не зависит от числа монет, если их достаточно много). Пусть также общая масса всех монет равна 540 г. Если бы все эти монеты были «легкой разновидности», то общая их масса была бы равна 525 г, что на 15 г меньше действительной. Почему так? Потому что не все монеты легкие: есть среди них и тяжелые. Замена одной легкой монеты на тяжелую приводит к увеличению общей массы на 0,6 г. Нам же надо увеличить массу на 40 г. Следовательно, легких монет имеется 15/0,6 = 25. Таким образом, в смеси 25/210 = 0,119 или 11,9% легких монет. (Конечно, со временем «изотопное соотношение» монет разного типа будет меняться: легких будет все больше, тяжелых – все меньше. Для элементов же соотношение изотопов в природе постоянно.)
Точно так же и в случае изотопов хлора или меди: известна средняя атомная масса меди – 63,546 (ее определили химики, анализируя различные соединения меди), а также массы легкого 64Cu и тяжелого 65Cu изотопов меди (эти массы определили физики, используя свои, физические, методы). Если элемент содержит более двух стабильных изотопов, их соотношение определяется другими методами.
Наши монетные дворы – Московский и Санкт-Петербургский тоже, оказывается, чеканили разные «изотопные разновидности» монет. Причина та же – подорожание металла. Так, 10- и 20-рублевые монеты в 1992 чеканились из немагнитного медно-никелевого сплава, а в 1993 – из более дешевой стали, и эти монеты притягиваются магнитом; по внешнему виду они практически не различаются (кстати, часть монет этих годов отчеканены «не в том» сплаве, такие монеты очень редкие, а некоторые стоят дороже золота!). В 1993 чеканились также 50-рублевые монеты из медного сплава, и в том же году (гиперинфляция!) – из стали, покрытой латунью. Правда, массы наших «изотопных разновидностей» монет отличаются не так сильно, как у американских. Тем не менее, точное взвешивание кучи монет дает возможность рассчитать, сколько в них монет каждого сорта – по массе, либо по числу монет, если подсчитано общее их число.
Илья Леенсон
Иван, большое спасибо за ответ!
Ваша ссылка достаточно интересна, но хотелось бы узнать чуть больше.
В уроке по этой ссылке опять отталкиваются от относительных атомных масс. А заданный вопрос, что в «В вопросы к уроку», который звучит как «А откуда ученые нашли что масса 1/12 углерода равна 1,66*10 в -24» , так никто и не разъяснил.
По поводу определения массовых долей элементов в формуле воды, видимо, нужно было в закрытых объемах синтезировать воду из водорода и кислорода, а потом подсчитать массы газов вступивших в реакцию. Это один из методов на который Вы указали, но, видимо, есть и другие. И как все же определили массу атома углерода и еще с такой точностью.
В уроке 2 «Относительная атомная масса химических элементов» из курса «Химия для чайников» рассмотрим разные способы выражения массы химических элементов. Напоминаю, что в прошлом уроке «Атомы и химические элементы» мы рассмотрели, кто и когда высказал идею о том, что все вокруг состоит из атомов; также выяснили, что из себя представляет химический элемент и каким образом обозначается.
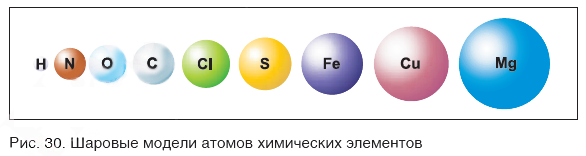
Чем различаются атомы разных элементов между собой? Вы уже знаете: массой, размерами и строением. На рисунке 30 показаны шаровые модели атомов некоторых химических элементов, конечно, не в реальных размерах, а многократно увеличенные. В действительности атомы настолько малы, что их невозможно рассмотреть даже в самые лучшие оптические микроскопы.
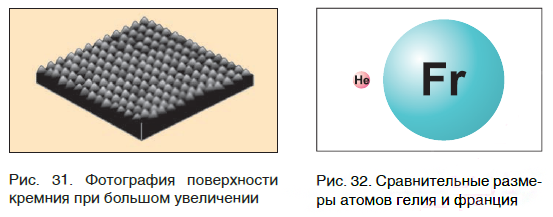
На заметку: В конце XX в. у ученых появились более совершенные микроскопы, позволяющие достигать увеличения в несколько десятков миллионов раз. Они называются туннельными микроскопами. На рисунке 31 показана фотография поверхности кремния. На ней отчетливо видны отдельные атомы, расположенные на поверхности этого вещества.
Размеры и масса атомов
Современная наука обладает методами, позволяющими определять размеры и массы атомов. Так, например, самый легкий атом — атом водорода. Его масса равна 0,0000000000000000000000000016735 кг. Самым маленьким является атом гелия He. Диаметр этого атома равен приблизительно 0,00000000098 м. Записывать и читать такие числа затруднительно, поэтому обычно их представляют в более удобном виде: 1,6735·10−27 кг и 9,8·10−10 м. Атомы большинства химических элементов по своим размерам значительно больше атома гелия. Самый большой из них — атом элемента франция Fr. Его диаметр в 7 раз больше диаметра атома гелия (рис. 32).
Еще больше различаются атомы разных элементов по массе. Масса атома обозначается символом ma и выражается в единицах массы СИ (кг). Так, например, масса атома углерода равна: ma(С) = 19,94·10−27 кг, а атома кислорода — ma(О) = 26,56·10−27 кг. Масса атома самого тяжелого из существующих на Земле элементов — урана U — почти в 237 раз больше массы атома водорода.
Атомная единица массы
Пользоваться такими маленькими величинами масс атомов при расчетах неудобно. К тому же, когда в XIX в. начало формироваться атомно- молекулярное учение, ученые еще не представляли реальных размеров и масс атомов. Поэтому на практике вместо истинных масс атомов стали применять их относительные значения. Они рассчитывались по массовым отношениям простых веществ в реакциях друг с другом. Химики предположили, что эти отношения пропорциональны массам соответствующих атомов. Именно так в начале XIX в. Дж. Дальтон ввел понятие относительной атомной массы, приняв за единицу сравнения массу самого легкого атома — водорода.
В настоящее время в качестве такой единицы сравнения используется 1/12 часть массы атома углерода (рис. 33). Она получила название атомной единицы массы (а. е. м.). Ее международное обозначение — u (от английского слова «unit» — единица):
Атомная единица массы — это 1/12 часть массы атома углерода, которая равна 1,66·10−27 кг.
Относительная атомная масса
Сравнивая средние массы атомов различных элементов с атомной единицей массы, получают значения относительных атомных масс химических элементов.
Относительная атомная масса элемента — это физическая величина, которая показывает, во сколько раз масса атома данного химического элемента больше 1/12 части массы атома углерода.
Относительная атомная масса обозначается символами Ar (А — первая буква английского слова «atomic» —атомный, r — первая буква английского слова «relative», что значит относительный), следовательно:
где Х — символ данного элемента.
Например, относительная атомная масса водорода:
а кислорода:
Как видите, относительная атомная масса показывает, во сколько раз масса атома данного элемента больше атомной единицы массы u.
В таблице Менделеева приведены относительные атомные массы всех элементов. В расчетах при решении задач мы будем пользоваться округленными до целых значениями этих величин (см. урок 1).
Внимание! Очень часто относительную атомную массу называют просто атомной массой. Однако следует отличать атомную массу — величину относительную (например, Ar(О) = 16) — от массы атома — величины, выражаемой в единицах массы — килограммах (ma(O) = 26,56·10−27 кг) или атомных единицах массы (ma(O) = 16·u).
Пример. Во сколько раз атом ртути тяжелее атома кальция?
Решение. Относительные атомные массы элементов равны: Ar(Hg) = 201 и Ar(Ca) = 40.
Масса атома ртути равна: ma(Hg) = Ar(Hg)·u (кг).
Масса атома кальция равна: ma(Са) = Ar(Са)·u (кг).
Другими словами, отношение масс атомов этих элементов равно отношению их относительных атомных масс. Следовательно, отношение масс атомов ртути и кальция равно:
Ответ: в 5,03 раза.
Краткие выводы урока:
- Атомная единица массы представляет собой 1/12 часть массы атома углерода.
- Относительная атомная масса химического элемента равна отношению массы его атома к 1/12 части массы атома углерода.
- Относительная атомная масса химического элемента является величиной безразмерной и показывает, во сколько раз масса атома данного элемента больше атомной единицы массы.
Надеюсь урок 2 «Относительная атомная масса химических элементов» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Определить вес одного атома должно быть достаточно просто, верно? Нужно просто поместить атом на весы, которые обладают максимальной чувствительностью и все — у нас есть измерения!
А как тогда насчет всех мертвых клеток кожи? Они имеют толщину в триллионы атомов, отслаиваются от вашей руки и падают вниз на весы, хороня ваш атом в куче других атомов. Между тем, другие атмосферные частицы летая вокруг, будут подпрыгивать на наших весах и отскакивать от них вперед и назад. Все это будет мешать нашим измерениям, верно?
Да, это так. В связи с этим, возникает очень непростой вопрос — а как нам изолировать один атом, чтобы узнать его вес?
Насколько маленький атом?
Вы, вероятно, знаете, что все состоит из крошечных частиц, называемых атомами; сам атом состоит из еще более мелких частиц, а именно протонов, нейтронов и электронов. Вы также, наверное, слышали, что атомы маленькие, но задумывались ли вы о том, насколько они на самом деле малы?
Чтобы немного лучше понять их размер, давайте рассмотрим яблоко. Предположим, что яблоко состоит только из атомов азота (что неправда, но для уменьшения сложности проблемы, мы примем это). Пусть каждый из этих атомов азота будет размером с чернику. Насколько большое должно тогда быть яблоко?
Оно было бы того же размера, что и планета Земля. Это просто безумие, не так ли? Это становится еще более безумным, если вы попытаетесь масштабировать размер субатомных частиц!
В центре атома находится воображаемая сфера, называемая ядром, которая содержит нейтроны и протоны, а снаружи — электроны. Если бы атом был увеличен до размеров футбольного поля, ядро было бы не больше, чем песчинка, находящаяся в самом центре этого поля — не мяч, а песчинка. По краям поля находятся электроны, а все остальное просто пустое пространство (нейтронным звездам есть куда сжиматься).
Теперь, когда мы освоились в микроскопическом мире атомов, как мы сможем наблюдать за такой крошечной вещью, не говоря уже о том, чтобы справиться с ней и взвесить ее даже на самых чувствительных весах?
Ньютон поможем нам в этом. Его второй закон движения, F = ma, где «а» — ускорение тела, имеющего массу «м», когда на него действует сила «F», — основная идея измерения атома. Инструмент, известный как масс-спектрометр, используется для проведения эксперимента.
Работа масс-спектрометра
Первым шагом делается ионизация газа, состоящего из атомов, путем запуска пучка частиц в газе, который либо добавляет электроны к атомам, либо сбивает несколько их электронов, в зависимости от типа используемого пучка частиц. Это дает атомам чистый отрицательный или положительный электрический заряд, и они образуют ионы.
Далее эти ионы пропускаются через трубку, в которой они подвергаются воздействию электрических и магнитных полей. Оба эти поля оказывают силы на ионы. Электрическая сила изменяет скорость ионов, в то время как магнитная сила изгибает их путь.
Затем ионы собираются с помощью чашек Фарадея (металлическая чаша, предназначенная для улавливания заряженных частиц в вакууме) на конце трубки, генерируя ток в проводах, прикрепленных к чашкам. Измеряя, когда и где поток ионов попадает в чашки Фарадея, физики могут определить ускорение и направление ионов под воздействием электрического и магнитного полей.
Наконец, с помощью второго закона движения Ньютона, F = ma, переставленного как m = F / a, вы делите общую силу, действующую на ионы, на их результирующее ускорение, чтобы определить массу ионов. Аналогично мы определяем массу электронов с помощью масс-спектрометра.
Используя масс-спектрометр, физики определили, что масса атома водорода составляет 1,6737236 × 10 -27 кг, причем более чем 99,99 % массы сконцентрировано в ядре.
Старый метод
До появления «масс-спектрометра» исследования по физике частиц тоже проводились, но идея атома была очень размытой. В те дни вес атомов, составляющих элемент, измерялся в единицах относительной массы, а не фактической массы.
Итальянский ученый Амедео Авогадро понял, что объем любого газа (при данном давлении и температуре) пропорционален числу атомов или молекул, составляющих его; это был большой прорыв. Это позволило физикам сравнить относительные веса одинаковых объемов различных газов, чтобы определить относительные массы атомов, составляющих их.
Атомные массы измерялись в единицах атомной массы (а.е.м.), где 1 а.е.м. был равен одной двенадцатой массы атома углерода-12. Вскоре после этого появилась знаменитая константа, известная как число Авогадро (6.023 × 1023).
Это число содержит количество атомов или молекул в одном моль (количество вещества системы, содержащей столько же структурных элементов, сколько атомов в 0.012 кг углерода-12.) газа. Это помогло им получить приблизительные оценки массы одного атома путем взвешивания объема всего газа и деления на число Авогадро.