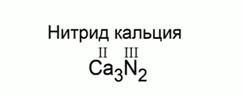Одной из самых главных задач в химии является правильное составление химических формул. Химическая формула – это письменное представление состава химического вещества с помощью латинского обозначения элемента и индексов. Для правильного составления формулы нам обязательно понадобится таблица Менделеева и знание простых правил. Они достаточно простые и запомнить их смогут даже дети.
Как составлять химические формулы
Основным понятием при составлении химических формул является “валентность“. Валентность – это свойство одного элемента удерживать определенное число атомов в соединении. Валентность химического элемента можно посмотреть в таблице Менделеева, а также нужно помнить и уметь применять простые общие правила.
- Валентность металла всегда равна номеру группы, при условии, что он находится в главной подгруппе. Например, калий имеет валентность 1, а кальций – 2.
- С неметаллами немного сложнее. Неметалл может иметь высшую и низшую валентности. Высшая валентность равна номеру группы. Низшую валентность можно определить вычтя номер группы элемента из восьми. При соединении с металлами неметаллы всегда имеют низшую валентность. Кислород всегда имеет валентность 2.
- В соединении двух неметаллов низшую валентность имеет тот химический элемент, который находится в таблице Менделеева правее и выше. Однако, фтор всегда имеет валентность 1.
- И еще одно важное правило при расстановке коэффициентов! Общее число валентностей одного элемента всегда должно быть равно общему количеству валентностей другого элемента!
Закрепим полученные знания на примере соединения лития и азота. Металл литий имеет валентность, равную 1. Неметалл азот располагается в 5 группе и имеет высшую валентность 5 и низшую – 3. Как мы уже знаем, в соединениях с металлами неметаллы всегда имеют низшую валентность, поэтому азот в данном случае будет иметь валентность равную трем. Расставляем коэффициенты и получаем искомую формулу: Li3N.
Вот так, достаточно просто, мы научились составлять химические формулы! А для лучшего запоминания алгоритма составления формул мы подготовили его графическое представление.
Составление химических формул: алгоритм
Описание презентации по отдельным слайдам:
-
1 слайд
Правила работы с презентацией:
Просмотри все слайды
Запиши основные правила в тетрадь, если у тебя их нет (по причине отсутствия)
Начиная «7» слайда идёт повторение темы «Составление формул по валентности
Все примеры обязательно записываются в рабочую тетрадь
Новая тема с «10» слайда -
2 слайд
25/08/21
Составление формул бинарных соединений
Правило нахождения валентности по П.С.:
2). У элемента, стоящего в формуле первым, валентность равна номеру группы.
1). На первое место в формуле ставится элемент, у которого номер группы меньше
3). У элемента, стоящего на втором месте в формуле, валентность равна 8 ─ № группы
Бинарными называют соединения, состоящие из двух элементов -
3 слайд
25/08/21
Составление формул по валентности:
Дано: кислород и натрий
Na O
Пример:
Порядок действий:
4. Находим индексы.
I
2
2. Находим валентность химических элементов.
3. Находим наименьшее общее кратное.
II
1. Определяем по ПСХЭ какой элемент писать первым.
2:I = 2
2
2:II = 1
1 -
4 слайд
25/08/21
Составление формул по валентности:
Дано: сера и алюминий
Al S
Пример:
Порядок действий:
4. Находим индексы.
III
6
2. Находим валентность химических элементов.
3. Находим наименьшее общее кратное.
II
1. Определяем по ПСХЭ какой элемент писать первым.
6:III = 2
2
6:II = 3
3 -
5 слайд
25/08/21
Составление формул по валентности:
Дано: цинк и фтор
Zn F
Пример:
Порядок действий:
4. Находим индексы.
II
2
2. Находим валентность химических элементов.
3. Находим наименьшее общее кратное.
I
1. Определяем по ПСХЭ какой элемент писать первым.
2:II = 1
1
2:I = 2
2 -
6 слайд
25/08/21
Составление формул по валентности:
Дано: фосфор и кислород
P O
Пример:
Порядок действий:
4. Находим индексы.
V
10
2. Находим валентность химических элементов.
3. Находим наименьшее общее кратное.
II
1. Определяем по ПСХЭ какой элемент писать первым.
10:V = 2
2
10:II = 5
5 -
7 слайд
25/08/21
Составить формулы по валентности:
Азот и барий:
Ba N
II III
3
2
фтор и фосфор:
PF
V I
5
Цинк и кислород:
ZnО
II II
6
5
2 -
8 слайд
25/08/21
Составить формулы по валентности:
фосфор и кальций:
Сa Р
II III
3
2
хлор и углерод:
CCl
IV I
4
Сера и углерод:
C S
IV II
6
4
4
2 -
9 слайд
25/08/21
Закрепление:
водород и натрий:
NaH
I I
фтор и магний:
Mg F
II I
2
Кремний и бром:
Si Br
IV I
1
2
4
4 -
10 слайд
Номенклатура бинарных соединений
Слово «Номенклатура»
обозначает «название» -
11 слайд
25/08/21
Правило составления названия вещества:
2). К его латинскому названию добавляют суффикс «ид»
1). Называют вещество по второму элементу
3). Затем добавляют русское название первого элемента
Этот значок, напоминает, что конспект необходимо записать в тетрадь -
12 слайд
25/08/21
S – сульфид
O – оксид
F – фторид
Cl – хлорид
I – иодид
Br — бромид
P – фосфид
N – нитрид
C – карбид
Si – силицид
H – гидридОбязательно списать таблицу в тетрадь!!!
-
13 слайд
Как эти правила работают:
Назвать вещество Li3N
Второй элемент в формуле по таблице (смотри предыдущий слайд)
Называется: «нитрид»
Первый элемент в формуле называем по-русски: «литий», в нужном падеже
Итак, вещество …. называется
Li3N – нитрид лития -
14 слайд
Как эти правила работают:
Назвать вещество BaS
Второй элемент в формуле по таблице (смотри таблицу)
Называется: «cульфид»
Первый элемент в формуле называем по-русски: «барий», в нужном падеже
Итак, вещество …. называется
BaS – сульфид бария -
15 слайд
Как эти правила работают:
Назвать вещество Na3P
Второй элемент в формуле по таблице (смотри таблицу)
Называется: «фосфид»
Первый элемент в формуле называем по-русски: «натрий», в нужном падеже
Итак, вещество …. называется
Na3P – фосфид натрия -
16 слайд
Как эти правила работают:
Назвать вещество Al4C3
Второй элемент в формуле по таблице (смотри таблицу)
Называется: «карбид»
Первый элемент в формуле называем по-русски: «алюминий», в нужном падеже
Итак, вещество …. называется
Al4C3 – карбид алюминия -
17 слайд
Назовите следующие вещества
MgO
ZnCl2
Al2S3
Li3P
Ag2O
H4C
Na4SiЗакрепление!
Опрос по новой теме будет проводиться по видеозвонку, начиная с понедельника
До встречи!
В процессе развития химии веществам давали произвольные исторически сложившиеся названия. Так, вещество с формулой NaCl получило название поваренная соль, H2SO4 – купоросное масло (так как представляет собой маслянистую жидкость). Некоторые из таких названий используются и сейчас, многие просто устарели. У каждого вещества есть научное название. Рассмотрим правила составления названий бинарных веществ (веществ, состоящих из атомов двух химических элементов).
Названия бинарных веществ состоят из двух слов. Первое слово обязательно имеет окончание –ид (Рис. 1).
Рис. 1. Названия некоторых бинарных веществ
Второе слово в названии – название элемента, образующего бинарное вещество (например, оксид кальция, хлорид магния).
Если элемент, стоящий в химической формуле на первом месте, имеет переменную валентность, то она указывается в скобках.
Пример. Составим название вещества с химической формулой Fe2S3.
На втором месте в формуле записана сера, следовательно, это сульфид. Элемент, стоящий на первом месте, — это железо. Железо имеет переменную валентность, в данном случае она равна III:
Рис. 2. Формула сульфида железа
2. Составление химической формулы вещества по его названию
Чтобы составить химическую формулу вещества по названию, необходимо знать валентности химических элементов. Нужно запомнить, что валентность серы в сульфидах равна II, хлора в хлоридах – I, брома в бромидах – I, йода в иодидах – I, фтора во фторидах – I, азота в нитридах – III, фосфора в фосфидах – III, кремния в силицидах – IV.
Пример. Составим формулу нитрида кальция.
На первом месте запишем символ химического элемента кальция, на втором – азота. Сверху над символами элементов запишем значения их валентности. Кальций имеет постоянное значение валентности, равное II, а азот в нитридах трехвалентен. НОК чисел 2 и 3 равно шести. Разделим это число на значение валентности каждого элемента и запишем индексы в формуле:
Рис. 3. Формула нитрида кальция
Алгоритм составления химических формул
Формулы составляются по валентности. Валентность определяется по электронной конфигурации. Чтобы сократить процесс и сэкономить время, используют данные таблицы растворимости.
1. Формула состоит из 2 частей. «+» ионы всегда на первом месте (тот, у кого забирают электроны), «–» ионы – всегда на втором (тот, кто отбирает). В таблице растворимости «+» ионы сверху, а «–» ионы – сбоку слева. Отделяем «+» от «–» вертикальной черточкой.
|
Na+ |
S2– |
|
1 |
2 |
Атом Na потерял электрон.
Атом S присоединил два электрона.
2. Валентность – степень окисления без знака. Она ставится над знаком атома химического элемента римской цифрой.
|
I |
II |
|
Na |
S |
3. Если атома нет в таблице, и он стоит на первом месте, то ставим валентность, указанную в скобке или анализируем электронную конфигурацию.
|
V |
|
|
P |
O (V) |
4. Если атома нет в таблице, и он стоит на втором месте, то вычисляем её по формуле: 8 – № группы атома химического элемента.
|
V |
II |
|
|
P |
O |
8–6=2 значит валентности кислорода II |
5. Находим наименьшее общее кратное между значениями валентности и ставим арабской цифрой над черточкой.
|
10 |
|
|
V |
II |
|
P |
O |
6. Делим НОК на каждую валентность и получаем индекс, который ставится справа снизу от знака атома химического элемента.
|
10 |
|
|
V |
II |
|
P2 |
O5 |
7. Ион, состоящий из одинаковых атомов, называется простым. Индекс ставится справа снизу от иона (__________________________________)
8. Ион, состоящий из разных атомов, называется сложным. При постановке индекса его берут в скобки (___________________________).
|
2 |
|
|
II |
I |
|
Ca |
(OH)2 |
9. Формулу всегда называют с «богатого» в именительном падеже, а затем называют «бедного» в родительном падеже.
CaCl2 (что?) хлорид (чего?) кальция
Алгоритм составления химических формул
Формулы составляются по валентности. Валентность определяется по электронной конфигурации. Чтобы сократить процесс и сэкономить время, используют данные таблицы растворимости.
1. Формула состоит из 2 частей. «+» ионы всегда на первом месте (тот, у кого забирают электроны), «–» ионы – всегда на втором (тот, кто отбирает). В таблице растворимости «+» ионы сверху, а «–» ионы – сбоку слева. Отделяем «+» от «–» вертикальной черточкой.
|
Na+ |
S2– |
|
1 |
2 |
Атом Na потерял электрон.
Атом S присоединил два электрона.
2. Валентность – степень окисления без знака. Она ставится над знаком атома химического элемента римской цифрой.
|
I |
II |
|
Na |
S |
3. Если атома нет в таблице, и он стоит на первом месте, то ставим валентность, указанную в скобке или анализируем электронную конфигурацию.
|
V |
|
|
P |
O (V) |
4. Если атома нет в таблице, и он стоит на втором месте, то вычисляем её по формуле: 8 – № группы атома химического элемента.
|
V |
II |
|
|
P |
O |
8–6=2 значит валентности кислорода II |
5. Находим наименьшее общее кратное между значениями валентности и ставим арабской цифрой над черточкой.
|
10 |
|
|
V |
II |
|
P |
O |
6. Делим НОК на каждую валентность и получаем индекс, который ставится справа снизу от знака атома химического элемента.
|
10 |
|
|
V |
II |
|
P2 |
O5 |
7. Ион, состоящий из одинаковых атомов, называется простым. Индекс ставится справа снизу от иона (__________________________________)
8. Ион, состоящий из разных атомов, называется сложным. При постановке индекса его берут в скобки (___________________________).
|
2 |
|
|
II |
I |
|
Ca |
(OH)2 |
9. Формулу всегда называют с «богатого» в именительном падеже, а затем называют «бедного» в родительном падеже.
CaCl2 (что?) хлорид (чего?) кальция
Составление формул бинарных соединений
Запомнить!
|
Формула бинарного соединения |
Название |
|
ЭxHy |
гидриды |
|
ЭxOy |
оксиды |
|
ЭxSy |
сульфиды |
|
ЭxCly |
хлориды |
|
ЭxBry |
бромиды |
|
ЭxFy |
фториды |
|
ЭxPy |
фосфиды |
|
ЭxNy |
нитриды |
|
ЭxIy |
йодиды |
|
ЭxCy |
карбиды |
|
ЭxSiy |
силициды |
На первом месте в формуле бинарного соединения элемент с положительной степенью окисления.
На втором месте в формуле бинарного соединения элемент с отрицательной степенью окисления.
Отрицательная степень окисления определяется по формуле – (8 — № группы)
|
ЭxHy-1 |
|
ЭxCly-1 |
|
ЭxBry-1 |
|
ЭxFy-1 |
|
ЭxIy-1 |
|
ЭxOy -2 |
|
ЭxSy-2 |
|
ЭxPy-3 |
|
ЭxNy-3 |
|
ЭxCy-4 |
|
ЭxSiy-4 |
Алгоритм составления формулы бинарного соединения.
|
Последовательность действий |
Составление формулы ОКСИДА БОРА |
|
1. Написать символы элементов |
В О |
|
2. Определить степени окисления элементов (у первого элемента- по номеру группы, у второго элемента –(8-№группы )) |
+3 -2 |
|
3. Найти наименьшее общее кратное численных значений степеней окисления |
3•2 = 6 |
|
4. Найти соотношения между атомами элементов путем деления найденного наименьшего кратного на соответствующие степени элементов |
6 : 3 = 2, 6 : 2 = 3; |
|
5. Записать индексы при символах элементов |
В2 О3 |
|
6. Формула соединения (оксида бора ) |
В2О3 |
Алгоритм составления формулы бинарного соединения.
|
Последовательность действий |
Составление формулы ФТОРИДА ХРОМА (III) |
|
1. Написать символы элементов |
CrF |
|
2. Определить степени окисления элементов (у первого элемента- число из скобок в названии, у второго элемента – (8-№группы )) |
+3 -1 |
|
3. Найти наименьшее общее кратное численных значений степеней окисления |
3•1 = 3 |
|
4. Найти соотношения между атомами элементов путем деления найденного наименьшего кратного на соответствующие степени элементов |
3 : 3 = 1, 3 : 1 = 3; |
|
5. Записать индексы при символах элементов. (Индекс 1 не записываем) |
CrF 3 |
|
6. Формула соединения (оксида бора ) |
CrF 3 |
Составьте формулы бинарных соединений.
|
Силицид магния |
Mg2+2Si-4 |
Mg2Si |
|
Сульфид серебра(I) |
Ag2+1S-2 |
Ag2S |
|
Бромид бария |
Ba+2Br2-1 |
BaBr2 |
|
Оксид азота (I) |
N2+1O-2 |
N2O |
|
Фосфид магния |
||
|
Фторид кремния (IV) |
||
|
Оксид стронция |
||
|
Фосфид натрия |
||
|
Оксид азота (III) |
||
|
Хлорид бора |
||
|
Сульфид железа (II) |
||
|
Хлорид ртути(II) |
||
|
Сульфид натрия |
||
|
Оксид хрома (VI) |
||
|
Бромид фосфора (V) |
||
|
Оксид марганца(VII) |
||
|
Гидрид калия |
||
|
Бромид меди (II) |
||
|
Фосфид кальция |
||
|
Нитрид алюминия |