Задать вопрос
Задать вопрос
Ваш вопрос
Вопрос должен состоять из 4 и более символов (не считая знаков препинания)
Подробное описание
Можно ввести 4000 cимволов
Темы
Темы обязательны для заполнения
отправить
дежурный
Нажимая кнопку «отправить», вы принимаете условия пользовательского соглашения
Выберите причину жалобы и оставьте комментарий
Содержит грамматические или орфографические ошибкиСпамНе соответствует тематике сайтаНарушает закон РФМожет показаться обиднымНеверно указана темаПлохо сформулированДругое
Опишите, пожалуйста, подробно причину для более быстрой
обработки вашей жалобы:
Можно ввести 4000 cимволов
E-mail для обратной связи
Отправить
Нажимая кнопку «Отправить», вы принимаете условия пользовательского соглашения
Спасибо
Ваша заявка будет рассмотрена в течение 5 рабочих дней.
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые (
Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Как получить этиловый эфир аминопропионовой кислоты составьте уравнение реакцииFOR-DLE.ru — Всё для твоего DLE На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх. |
Задание 1
Какие органические вещества называют аминокислотами?
Органические вещества, содержащие в молекуле карбоксильную группу ―COOH и аминогруппу ― NH2.
Приведите примеры формул и названий таких соединений.
H2N ― CH2 ― COOH аминоуксусная кислота.
CH3 ― CH(NH2) ― COOH 2-аминопропионовая кислота.
C2H5 ― CH(NH2) ― COOH 2-аминобутановая кислота.
Почему их относят к амфотерным органическим соединениям? Аминокислоты могут проявлять кислотные свойства, которые определяет карбоксильная группа ― COOH, и основные свойства, которые определяет аминогруппа –NH2 , которая способна присоединять к себе катион водорода по донорно-акцепторному механизму за счёт наличия свободной электронной пары в атома азота.
Аминокислоты взаимодействуют с кислотами и щелочами:
H2N ― CH2 ― COOH + NaOH ⟶ H2N ― CH2 ― COONa + H2O
H2N ― CH2 ― COOH + HCl ⟶ [H3N ― CH2 ― COOH]Cl
Задание 2
Какие природные биополимеры называют белками?
Белки ― это природные полимеры, образованные остатками аминокислот, связанными между собой пептидными связями.
Задание 3
Опишите качественные реакции на белки.
1. Качественной реакцией на пептидные группы в молекулах органических соединений, является биуретовая реакция . При взаимодействии белков с раствором соли меди (II) в щелочной среде возникает фиолетовая окраска.
2. К ачественной реакцией на белок, содержащий фрагменты молекул ароматических аминокислот, является ксантопротеиновая реакция . Если белки или их растворы нагревать с концентрированной азотной кислотой, то имеющиеся в белках фрагменты молекул ароматических аминокислот взаимодействуют с этой кислотой с образованием азотсодержащих соединений желтого цвета.
Задание 4
Что называют денатурацией белка? Денатурация ― нарушение структуры белка.
Во время денатурации сохраняется только первичная структура белка, а остальные (вторичная, третичная и четвертичная) необратимо разрушаются.
Какие факторы могут её вызвать? Температура, механическое воздействие, действия химических реагентов.
Задание 5 Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
глюкоза ⟶ этиловый спирт ⟶ уксусный альдегид ⟶ уксусная кислота ⟶ хлоруксусная кислота ⟶ аминоуксусная кислота ⟶ дипептид аминоуксусной кислоты.
C6H12O6дрожжи ⟶ 2C2H5OH + 2CO2↑
2C2H5OH + O2 ⟶ 2CH3CHO + 2H2O (t 0 , кат.)
2CH3CHO + O2 ⟶ 2CH3COOH (t 0 , кат.)
CH3COOH + Cl2 ⟶ CH2ClCOOH + HCl (кат.)
CH2ClCOOH + 2NH3 ⟶ H2N ― CH2 ― COOH + NH4Cl 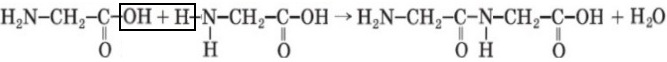
или так записать:
H2N ― CH2 ― COOH + H2N ― CH2 ― COOH ⟶ H2N ― CH2 ― CO ― NH ― CH2 ― COOH + H2O
Задание 6
В медицине для улучшения обменных процессов в центральной нервной системе применяют глицин в таблетках. Рассчитайте количество вещества глицина, содержащегося в одной таблетке массой 0,15 г, если известно, что в качестве вспомогательных веществ каждая таблетка содержит также 1% стеарата магния и 1% метилцеллюлозы.
Дано: m(таблетки)=0,15г, ω(стеарата магния)=1%, ω(метилцеллюлозы)=1%
Найти: n(NH2CH2COOH)-?
Решение
1. Рассчитываем массовую долю глицина в таблетке.
ω(NH2CH2COOH)=100%−ω(стеарата магния)−ω(метилцеллюлозы)=100%-1%-1%=98%
2. Вычисляем массу глицина в таблетке.
m(NH2CH2COOH)=ω(NH2CH2COOH) • m(таблетки):100%=98% •0,15 г:100%=0,147 г
3. Вычисляем ко личество вещества глицина массой 0,147 г по формуле: n =m/M, где M ― молярная масса.
M (NH2CH2COOH )=75 г/моль
n( NH2CH2COOH )=m( NH2CH2COOH )/M( NH2CH2COOH )=0,147 г : 75 г/моль=0,00196 моль=1,96 ммоль
Ответ: в таблетке содержится 1,96 ммоль глицина.
Задание 7
В двух пробирках находятся растворы глюкозы и белка. Как с помощью одного и того же реактива различить их?
Различить растворы глюкозы и белка можно с помощью свежеприготовленного осадка гидроксида меди (II). Под его действием белки (в щелочной среде) дают фиолетовое окрашивание (биуретовая реакция) , а глюкоза (как многоатомный спирт) образовывает с ним растворимое соединение ярко-синего цвета.
Задание 8
Какую биологическую роль играют белки в организме? При ответе используйте не только материал параграфа, но и знания, полученные на уроках биологии.
Белки ― строительный материал любого живого организма. В процессе пищеварения белки гидролизуются до аминокислот, из которых организм синтезирует необходимые для него белки.
Белки очень важны для организма:
― глицин и глутамин ― нейромедиаторы (участвуют в передаче нервных импульсов) ;
― с тирозина образуется йодтироксин (гормон щитовидной железы) ;
― белки-ферменты ускоряют реакции;
― гемоглобин в составе эритроцитов переносит кислород к тканям и углекислый газ от них;
― миоглобин запасает кислород в мышцах;
― белок коллаген, есть в составе кожи и костей, сохраняет определенную их форму и упругость;
― родопсин ― это белок-рецептор, воспринимает свет на сетчатке глаза и т.д.
Как получить этиловый эфир аминопропионовой кислоты составьте уравнение реакции
Содержание
Нашли о и ш бку?
Выделите её мышкой и нажмите CTRL + ENTER
Большое спасибо всем, кто помогает делать сайт лучше! =)
как получить этиловый спирт аминопропионовой кислоты? составьте уравнение реакции
Попроси больше объяснений
Ответ(ы) на вопрос:
Гость:
СН3-СН-СООН + OHC2H5 = CH2NH2COOC2H5 + H2O | NH2 (не очень уверена)
(44),
на голосовании
Голосование за лучший ответ
Надежный Как Аватор
Мастер
(1181)
10 лет назад
Ну неужели сложно поискать… .
CH3-CH(-NH3)-C(=O)-Cl + Na-O-CH2-CH3 = CH3-CH(-NH3)-C(=O)-O-CH2-CH3 + NaCl
Держи.
Похожие вопросы
- Вопросы и Ответы
- Химия
- Как получить этиловый эфир альфа-аминомасляной кислоты? уравнение реакции
Как получить этиловый эфир альфа-аминомасляной кислоты? уравнение реакции
- получить
- альфа
- кислоты
- уравнение
- реакции
- 1 — 4 классы
- химия
1 Ответ
Эфир получают реакцией этерификации. Т.е. Берем аминомасляную кислоту и этиловый спирт= то что ты спрашиваешь
Здравствуйте! На сайте Otvet-Master.ru собраны ответы и решения на все виды школьных задач и университетских заданий. Воспользуйтесь поиском решений на сайте или задайте свой вопрос онлайн и абсолютно бесплатно.
Напишите уравнения реакций синтеза этилового эфира пропионовой кислоты.
На странице вопроса Напишите уравнения реакций синтеза этилового эфира пропионовой кислоты? из категории Химия вы найдете
ответ для уровня учащихся 10 — 11 классов. Если полученный ответ не
устраивает и нужно расшить круг поиска, используйте удобную поисковую
систему сайта. Можно также ознакомиться с похожими вопросами и ответами
других пользователей в этой же категории или создать новый вопрос. Возможно,
вам будет полезной информация, оставленная пользователями в комментариях, где
можно обсудить тему с помощью обратной связи.
http://gdz.cool/h10_gos_2019/832-h10_gos_2019_19.html
http://expert-domru.ru/kak-poluchit-etilovyj-efir-aminopropionovoj-kisloty-sostavte-uravnenie-reakczii/
1
H
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
232,04
f-элемент
Серый мягкий металл
91
Pa
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Напишите уравнение реакции получения этилового эфира а-аминопропионовой кислоты (а-аланина). [c.90]
Этиловый эфир -аминопропионовой кислоты, получение см. [3]. [c.109]
Напишите схемы реакций, при которых образуются а ) метиловый эфир (З-аминопропионовой кислоты б) этиловый эфир аланина в) изопропиловый эфир у-аминовалериановой кислоты г) полный метиловый эфир глутаминовой кислоты. [c.79]
Нами предложен метод получения этилового эфира й)-аминоэнантовой кислоты действием гидрата окиси свинца на его гидрохлорид по аналогии с получением этилового эфира -аминопропионовой кислоты [5], так как этот метод прост в выполнении и дает лучший выход. [c.231]
ЭТИЛОВЫЙ ЭФИР 3 АМИНОПРОПИОНОВОЙ кислоты [c.229]
По литературным данным [3], т. кип. этилового эфира -аминопропионовой кислоты 54°/12 мм 58714 мм. [c.230]
Большее потери н соответственно низкий выход имеют место за счег разложения этилового эфира -аминопропионовой кислоты и быстрой полимеризации продуктов разложения. [c.230]
В трехгорлую колбу, снабженную обратным холодильником, мешалкой и трубкой для подачи газа, помещают 200 г -аланина, добавляют 500 мл этилового спирта и при интенсивном перемешивании пропускают через смесь ток хлористого водорода. Через 2—3 часа образуется прозрачный раствор. Спирт отгоняют в вакууме (20—30 мм), после чего образовавшийся гидрохлорид эфира -аминопропионовой кислоты переносят в эксикатор над серной кислотой и выдерживают в вакууме до постоянного веса. [c.230]
Получение ионита с группами -аминопропионовой кислоты проводят аналогично. Смесь 4 г хлорметилированиого сополимера в 15 мл диметилформамида и 14,5 г этилового эфира -амиНопропионовой кислоты выдерживают 6 часов при 80° и постоянном перемешивании. После гидролиза 0,5 н. раствором едкого натра (300 мл) и обработки 6%-ным раствором соляной кислоты (300 мл) получают ионит с амино-пропиоиовыми группировками. [c.110]
Этиловый эфир (5-аминопропионовой кислоты. [c.5]
СХЕМА СИНТЕЗА ЭТИЛОВОГО ЭФИРА Р АМИНОПРОПИОНОВОЙ КИСЛОТЫ [c.229]
Этиловый эфир З-фенил-З-аминопропионовой кислоты Г7, VI, 878. [c.204]
Напишите структурные формулы следующих соединений Р-аминомасляной кислоты, хлоргидрата этилового эфира 7-амино-валериановой кислоты, амида а-аминопропионовой кислоты. [c.86]
Этиловый эфир — (п X л о р ф е н и л I — а м и н о п р о п и о н о в о й кислоты—из 1.5 г хлоргидрата иминоэфира Р-( -хлорфенил)-аминопропионовой кислоты. Выход 1.0 г (88.5%1. т. кип. 165° (4 мм). [c.1089]
Этиловый эфир К-бензоил- (3,4-ди-хлорфенил) -2-аминопропионовой кислоты (суффикс) > 1.0 [c.66]
Выход продукта равен 8—9 г, что составляет 50—60% от теорети1 ского, считая на гидрохлорид этилового эфира -аминопропионовой кислоты. [c.230]
Какое строение будет иметь дипептид, синтезированный из хлоргидрата хлорангидрида а-аминопропионовой кислоты и этилового эфира аминоуксусной кислоты Составьте схему синтеза. [c.138]
Мы выделили этиловые эфиры р-фенил- и р-(я-хлорфенил)-амино-пропионовой кислоты в результате разложения соответственных хлоргидратов иминоэфиров при обработке раствором щелочи. Следует отметить, что этиловый эфир 3-( -хлорфенил)-аминопропионовой кислоты ранее был получен Эльдерфильдом и Маггиало ] присоединением этилового эфира акриловой кислоты к л-хлоранилину. [c.1087]
Этиловый эфир -фениламинопропионовой кислоты — из 11 г хлоргидрата этилового иминоэфира -фенил-аминопропионовой кислоты. Выход 6.5 г <81%), т. кип. 145° (4 мм). [c.1089]
Для сдвига равновесия реакции в сторону образования 3-аланина следует обеспечить большой избыток аммиака и высокую температуру [44, 66]. По данным Е. Жданович [50], требуется температура реакции 154— 158° С (избыточное давление 26—32 кгс/см ), соотношение 10%-ного раствора аммиака к акрилонитрилу 18,5 1 и углекислого аммония к акрилонитрилу 3,7 1. На основании этих данных технологический процесс заключается в следующем в горизонтальный автоклав 1 (рис. 18) с вращающейся мешалкой и паровой рубашкой загружают из мерника 2 водный раствор (10—15%) аммиака и из сборника 3 двууглекислого аммония и из мерника 4 акрилонитрил. Нагревают реакционную массу до 154—158° С, при этом избыточное давление повышается до 30—40 кгс1см . Не допускается загрузка более 0,4 объема автоклава. Из автоклава реакционную массу выгружают в перегонный аппарат 5, где отгоняют водный раствор аммиака. Кубовый остаток сливают в реактор 6, разбавляют водой и очищают активированным углем при температуре 40—50° С уголь отфильтровывают на нутч-фильтре 7, фильтрат направляют в сборник 8, а затем в вакуум-аппарат 9 для сгущения. Сгущенный раствор сливают в кристаллизатор 10, где выделяют -аланин добавлением из мерника // этилового абсолютированного спирта при температуре 0-1-5° С. Затем осадок фугуют в центрифуге 2. Кристаллы сушат в вакуум-сушилке 13 и направляют в сборник 14. Маточный раствор поступает в сборник 15, откуда засасывают в вакуум-аппарат 16, сгущают, сливают в кристаллизатор 17, где спиртом выделяют дополнительное количество -аланина, который отфуговывают в центрифуге 18. Кристаллы -аланина II для переосаждения направляют в реактор-кристаллизатор 10. Маточный раствор II из центрифуги 18 собирают в приемнике 19, он является либо отходом производства, либо его направляют на переработку в -аланин. Выход -аланина — прямой 40—50%, а при регенерации -аланина из вторичного и третичного аминов выход может быть увеличен до 65—70 %. -Аланин ( -аминопропионовая кислота) aHjOaN представляет собой бесцветные кристаллы с температурой 199— 200° С [52], молекулярная масса 89,09, хорошо растворим в воде, труднее в метиловом, этиловом и изопропиловом спиртах нерастворим в эфире и ацетоне. [c.144]
Этилендиаминтетрауксусной кислоты динатриевая соль (Трилон Б) Этиленхлоргидрин (1-хлорэтан6л-2) Этилксантогенат калия Этилмеркурхлорид Этиловый эфир К-бензоил-Н- (3,4-ди-хлорфенил) -2-аминопропионовой кислоты (Суффикс) [c.440]
Какие структурные формулы имеют следующие аминокислоты и их производные а) а-аминомасляная, б) 7-аминомасля-ная, в) р-аминовалериановая, г) у-аминовалериановая, д) ос-амино-изовалериановая, е) р-аминоглутаровая, ж) у-аминокапроновая, з) р-окси-а-аминопропионовая, и) а-аминоадипиновая, к) а-амино-Р,7,б-триметилкапроновая,, л) а,6-диаминовалериановая, м) а-аминоизокапроновая (лейцин), н) моноамид а-аминоянтар-ной кислоты (аспарагин), о) этиловый эфир гликоколя, п) нитрил 7-аминомасляной кислоты, р) а,е-диаминокапроновая кислота (лизин). [c.221]
Ответ:
1. 3KOH+ AL(NO3)3=>Al(OH)3(осад.) +3KNO3
m(KOH)=mра-раf*массов.долю= 56*0,06=3,36
n(KОH)=3,36/56=0,06
т.к.избыток расствора нитрата алюминия то считаем по KOH
n(Al(OH)3) = 13n(KOH)=0,02
m(AlOH)3)=n*M=0,02*78=1,56-ответ
2. CuCl2+2AgNO3=Cu(NO3)2+2AgCl(осадок)
Решение:
m(CuCl2)=134·0,02=2,68 г
n(СuCl2)=2,68:135=0,019 моль
n(AgCl)=0,019·2=0,038 моль
m(AgCl)=0,038·143,5=5,453 г-ответ
3. Na3PO4+Ba(NO3)2=Ba3(PO4)2+3NANO3
m(Na3PO4)=205*0,08=16.4 г
n(Na3PO4)=16.4/164=0.1моль
n(Na3PO4)=n(Ba3(PO4)2)=0.1 моль
m(Ba3(PO4)2)=0.1*601=60.1г-ответ
Объяснение:


