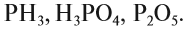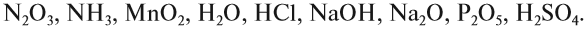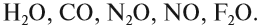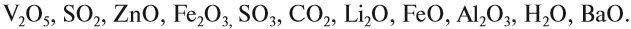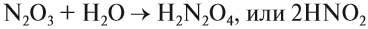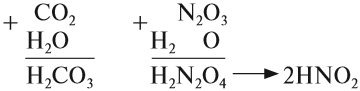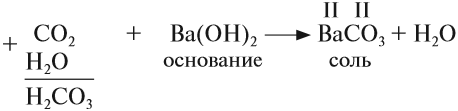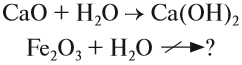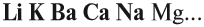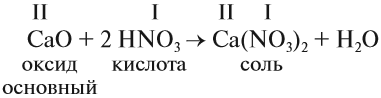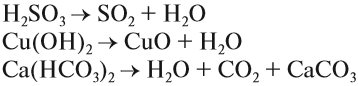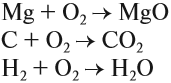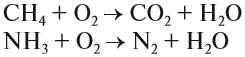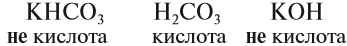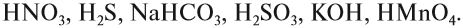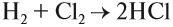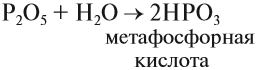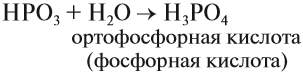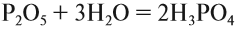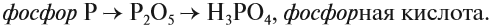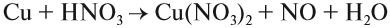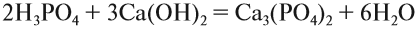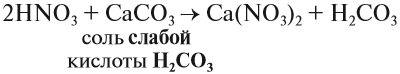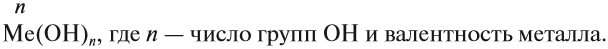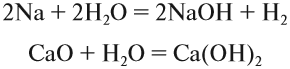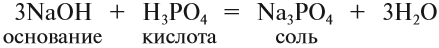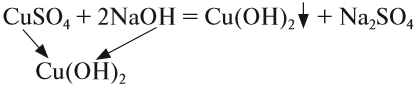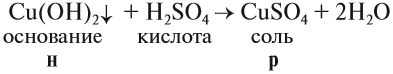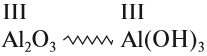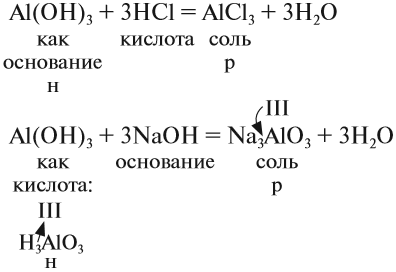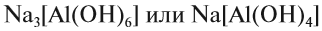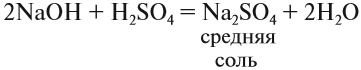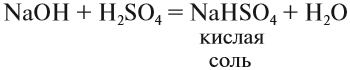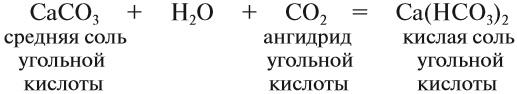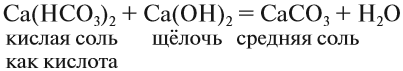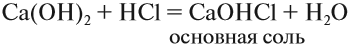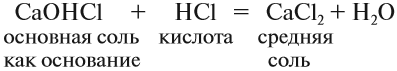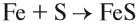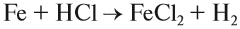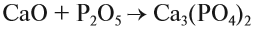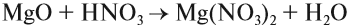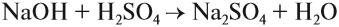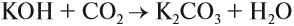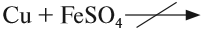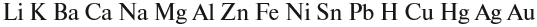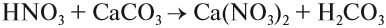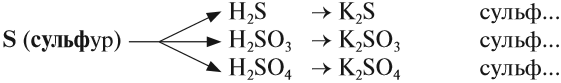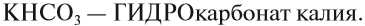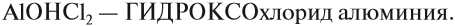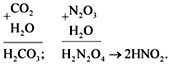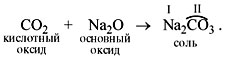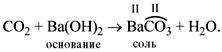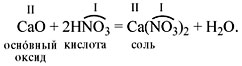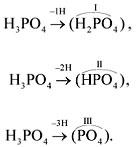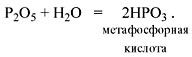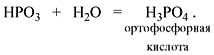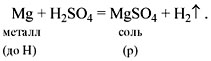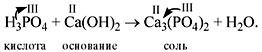|
§ 17 |
Валентность. Составление формул оксидов |
Вы, наверное, обратили внимание на то, что оксиды различных химических элементов по составу отличаются друг от друга. Например, на один атом кислорода в воде H2O приходятся два атома водорода, а в оксиде магния MgO — один атом магния. Как это можно объяснить?
В XIX в. учёные предположили, что атомы разных элементов обладают различной способностью присоединять к себе другие атомы. Так, атом водорода может присоединить лишь один атом другого химического элемента, кислород — два атома, азот — три. В настоящее время известно, что атомы, входящие в состав молекул, соединены между собой химическими связями в определённой последовательности. Чтобы показать это, используют структурные формулы, выражающие не только число атомов, но и последовательность их соединения. Химические связи между атомами в молекулах принято обозначать чёрточками.
Число связей, которые данный атом образует с другими атомами, называют валентностью.
Слово «валентность» в переводе с латинского означает «сила, способность».
Изобразим структурную формулу воды:
Обратите внимание на то, что атомы водорода в молекуле воды не связаны друг с другом, а соединены только с атомом кислорода. Каждый атом водорода образует одну химическую связь (от символа H отходит одна чёрточка) — он одновалентен. Атом кислорода образует две связи — он двухвалентен. Число чёрточек, отходящих от символа химического элемента в структурной формуле, и есть валентность данного атома.
Установлено, что и в других соединениях водород всегда одновалентен, т. е. атомы водорода образуют лишь одну связь. Валентность кислорода всегда равна двум.
В молекуле углекислого газа CO2 атом углерода образует с каждым атомом кислорода две двойные связи, которые равноценны четырём одинарным (четыре чёрточки в структурной формуле), следовательно, углерод в этом веществе четырёхвалентен:
O

Зная валентность одного химического элемента в соединении, можно определить валентность другого. Так, хлор в хлороводороде HCl одновалентен, азот в аммиаке NH3 трёхвалентен, а валентность углерода в метане CH4 равна четырём:
Для обозначения валентности обычно используют римские цифры, которые ставят в формуле над символом химического элемента:
Чтобы подсчитать валентность, нет необходимости каждый раз рисовать структурные формулы. Легко заметить, что в соединении общее число единиц валентности всех атомов одного элемента всегда равно общему числу единиц валентности всех атомов другого элемента. Иными словами, произведение числа атомов одного элемента на его валентность равно произведению числа атомов второго элемента на его валентность.
Таблица 4
|
Последовательность действий |
Составление формулы |
|
|
Указать валентность кислорода |
|
|
|
Умножить число атомов кислорода на численное значение его валентности (II) |
3•2 = 6 |
2•2 = 4 |
|
Разделить полученное значение на индекс, показывающий число атомов другого элемента |
6 : 2 = 3 |
4 : 1 = 4 |
|
Записать значение валентности над символом этого элемента |
|
|
Например:

Для углерода (число атомов равно 1): IV•1 = 4;
для кислорода (число атомов равно 2): II•2 = 4.
Чтобы определить валентность элемента в оксиде по формуле, необходимо провести следующие математические вычисления (табл. 4).
Некоторые химические элементы проявляют в соединениях постоянную валентность (табл. 5), её надо запомнить, другие — переменную.
Химические элементы с постоянной валентностьюТаблица 5
|
Валентность |
Химические элементы |
|
I |
H, Na, K, Ag |
|
II |
O, Mg, Ca, Ba, Zn |
|
III |
Al |
Таблица 6
|
Последовательность действий |
Составление формулы |
|
|
Записываем символы химических элементов (кислород на втором месте) и указываем их валентность (кислород двухвалентен, валентность второго элемента либо дана в названии, либо постоянна и приведена в таблице 5) |
Оксид алюминия |
Оксид углерода(IV) |
|
Находим наименьшее общее кратное двух числовых значений валентности |
III и II ⇒ 6 |
IV и II ⇒ 4 |
|
Находим индексы, поделив наименьшее общее кратное на численные значения валентности данного элемента |
6 : 3 = 2 (Al) 6 : 2 = 3 (O) |
4 : 4 = 1 (C) 4 : 2 = 2 (O) |
|
Записываем индексы после знаков химических элементов |
Al2O3 |
CO2 |
Обратите внимание, что значения валентности многих металлов совпадают с номерами групп Периодической системы химических элементов Д. И. Менделеева, в которых они находятся.
Значение переменной валентности принято указывать в скобках в названии соединения, например: 

Рассмотрим, как можно составить формулу оксида по его названию (табл. 6).
Понятие о валентности возникло на заре современной химии, поэтому его использование в настоящее время вызывает много вопросов. Как, например, определить валентность атомов в простых веществах? В железе при комнатной температуре у каждого атома 8 ближайших соседей (см. рис. 23, а). Означает ли это, что железо восьмивалентно? Как быть с другими веществами немолекулярного строения? Так, оксиды металлов, как правило, не образуют молекул. Строение того же оксида алюминия Al2O3 лишь формально можно изобразить структурной формулой O



1.Дайте определение понятия «валентность».
2.Зная, что водород одновалентен, определите валентность химических элементов по формулам соединений: NaH, CaH2, AlH3, CH4, PH3, H2S, HF.
3.Определите валентность элементов по формулам оксидов и назовите вещества: P2O5, SO2, SO3, NO, Na2O, CaO, Mn2O7, SnO2, I2O5, H2O.
4.Напишите формулы следующих оксидов: оксида магния, оксида фосфора(III), оксида калия, оксида хлора(IV), оксида железа(III), оксида меди(II), оксида кремния(IV), оксида хлора(VII), оксида цинка, оксида алюминия, оксида водорода, оксида золота(III).
5.В соединениях с кислородом марганец проявляет валентности II, III, IV, VII. Составьте формулы этих оксидов и назовите их.
6.Хлор образует четыре оксида, в которых он проявляет валентности I, III, V и VII. Составьте формулы этих соединений и назовите их.
7.При горении магния, цинка и алюминия в кислороде образуются их оксиды. Составьте формулы этих соединений, напишите уравнения реакций.
Содержание
- Оксиды
- Свойства кислотных оксидов
- Свойства основных оксидов
- Свойства амфотерных оксидов
- Способы получения оксидов
- Выводы
- Кислоты
- Свойства кислот
- Выводы
- Основания
- Свойства и способы получения щелочей
- Свойства и способы получения нерастворимых в воде оснований
- Свойства амфотерных гидроксидов
- Выводы
- Соли
- Способы получения солей
- Названия солей
- Выводы
Оксиды
Оксиды — сложные вещества, молекулы которых состоят из атомов двух химических элементов, один из которых — кислород. Атом кислорода в оксидах всегда имеет степень окисления –2.
Определите, какое из следующих соединений — оксид:
Оксидом является последнее соединение — P2O5 (в состав РН3 не входит атом кислорода, а в состав H3PO4 входят атомы трёх химических элементов: H, Р, O).
Оксиды называют по схеме:
оксид чего? (название элемента).
Например: СаО — оксид кальция.
Если оксид образован химическим элементом с переменной валентностью, то после названия элемента, нужно указать его валентность.
Например: Fe2О3 — оксид железа III, FеО — оксид железа II.
Задание 2.1. Среди следующих соединений найдите оксиды и назовите их:
Задание 2.2. Составьте формулы следующих оксидов: оксид хрома III, оксид углерода IV, оксид магния, оксид серы VI, оксид азота V, оксид калия, оксид марганца VI.
Многие оксиды могут реагировать с кислотами или основаниями. Продуктами таких реакций являются соли. Поэтому такие оксиды называются солеобразующими.
Однако существует небольшая группа оксидов, которые к таким реакциям не способны. Такие оксиды называются несолеобразующими:
Задание 2.3. Назовите эти несолеобразующие оксиды.
Некоторые оксиды имеют особые (тривиальные) названия:
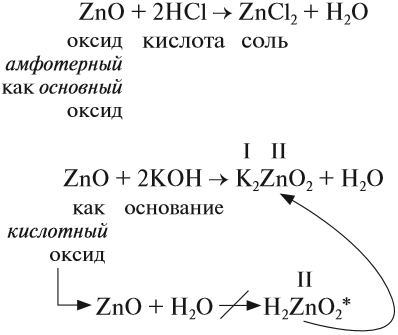
Солеобразующие оксиды делятся на три группы: основные, кислотные, амфотерные.
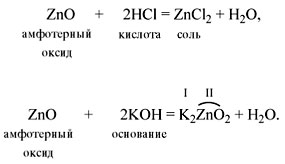
Точно установить характер оксида можно, только изучая его химические свойства. Например, кислотные оксиды реагируют с основаниями и не реагируют с кислотами. Основные оксиды реагируют с кислотами и не реагируют с основаниями. Амфотерные оксиды могут реагировать и с кислотами, и с основаниями, причём, реагируя с кислотами, они проявляют свойства основных оксидов, а реагируя с основаниями, — кислотных.
Отсюда вывод: в химических реакциях участвуют вещества с противоположными свойствами:
- основание и кислота;
- металл и неметалл;
- окислитель и восстановитель.
Впрочем, последние два случая мы рассмотрим позднее (см. уроки 2.4 и 7).
Поэтому, если определить по формуле оксида, какими свойствами он обладает, — можно предсказать, возможна ли эта реакция или нет! Но КАК это сделать? Вот некоторые правила:
- неметаллы образуют только кислотные оксиды*;
- металлы могут образовывать разные оксиды — основные, амфотерные, кислотные — в зависимости от валентности металла.
* Обратите внимание, что и безразличные оксиды образуются только неметаллами.
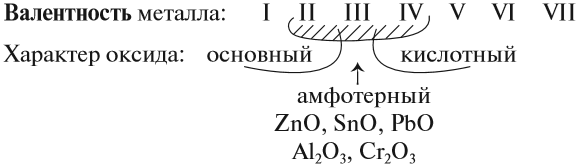
Предсказать свойства оксида металла может помочь эта схема.
Итак, основные оксиды металлов от кислотных оксидов металлов отличить легко: малая валентность металла — основный оксид; большая — кислотный. Но как быть с амфотерными оксидами? «Любимая» валентность металлов в этих оксидах — III. Но есть и исключения. Поэтому желательно запомнить формулы наиболее часто встречающихся амфотерных оксидов:
Задание 2.4. Назовите эти амфотерные оксиды.
Задание 2.5. Классифицируйте нижеприведённые оксиды:
Упражнение рекомендуется выполнить по схеме:
1. Определить, не является ли данный оксид несолеобразующим;
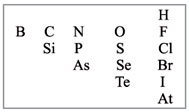
2. Определить, какой элемент входит в состав оксида: металл или неметалл, для чего выписать из таблицы Менделеева символы элементов – неметаллов: они расположены в главных подгруппах выше линии БОР — АСТАТ и на этой линии. Это:
3. Если в состав оксида входит атом неметалла — то оксид кислотный;
4. Для атома металла определить валентность, и по схеме определить характер оксида: основный, амфотерный или кислотный.
Например:
- Сr2О3 — амфотерный, так как хром — металл с низкой валентностью III;
- N2O3 — кислотный оксид, так как азот — неметалл;
- СrO3 — кислотный оксид, так как хром — металл с высокой валентностью VI.
Зная характер оксида, можно описать его свойства.
Свойства кислотных оксидов
1. Кислотные оксиды, кроме SiО2, реагируют c водой, образуя кислоту:
Чтобы составить формулу кислоты, нужно «сложить» все атомы исходных веществ, записывая на первом месте символ водорода, на втором — символ элемента, образующего оксид, и на последнем — символ кислорода. Если индексы получились чётными, их можно сократить:
Эти же реакции можно записать в виде «арифметического примера»:
Задание 2.6. Составьте уравнения реакций с водой для кислотных оксидов из задания 2.5, зная, что реакции идут по схеме:
кислотный оксид + вода → кислота
2. Кислотные оксиды реагируют с основными оксидами, образуя соль соответствующей кислоты, т. е. кислоты, которая образуется при взаимодействии этого оксида с водой (см. выше):
Для того чтобы составить такое уравнение, нужно:
- составить формулу кислоты («прибавив» к молекуле оксида молекулу воды);
- определить валентность кислотного остатка (это часть молекулы кислоты без атомов водорода). В данном случае кислотный остаток имеет состав СО3, его валентность равна числу атомов водорода в кислоте, т. е. II;
- составить формулу соли, записав вместо атомов водорода атом металла из основного оксида с его валентностью (в данном случае — натрий);
- составить формулу соли по валентности металла и кислотного остатка.
Задание 2.7. Составьте уравнения реакций с оксидом кальция кислотных оксидов из задания 2.5, зная, что реакции идут по схеме:
кислотный оксид + основный оксид → соль
3. Кислотные оксиды реагируют с основаниями, образуя соль соответствующей кислоты и воду:
Принципы составления уравнения те же, что и для реакций с основными оксидами (см. пункт 2).
Задание 2.8. Составьте уравнения реакций с гидроксидом натрия NаОН кислотных оксидов из задания 2.5, зная, что реакции идут по схеме:
кислотный оксид + основание → соль + вода
ЗАПОМНИТЕ! Кислотные оксиды и с кислотами и кислотными оксидами НЕ РЕАГИРУЮТ!
Свойства основных оксидов
1. Основные оксиды реагируют с водой, образуя основание. Реакция происходит, если получающееся основание растворимо в воде.
Общая формула оснований Ме(ОН)х, где х — валентность металла, равная числу ОН групп.
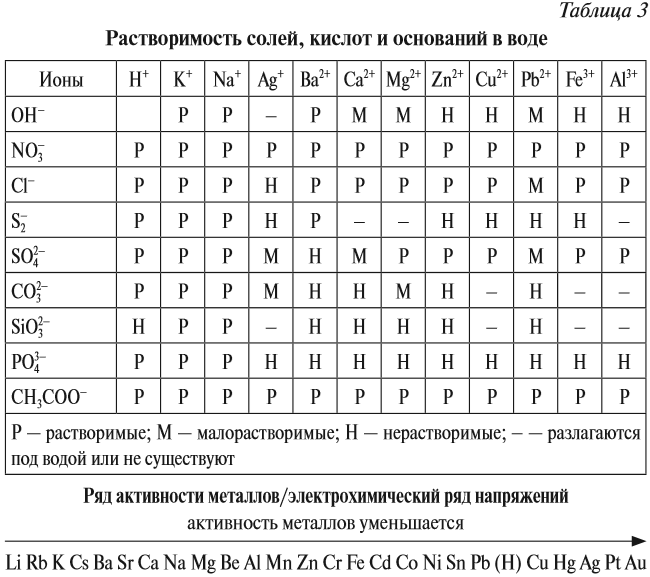
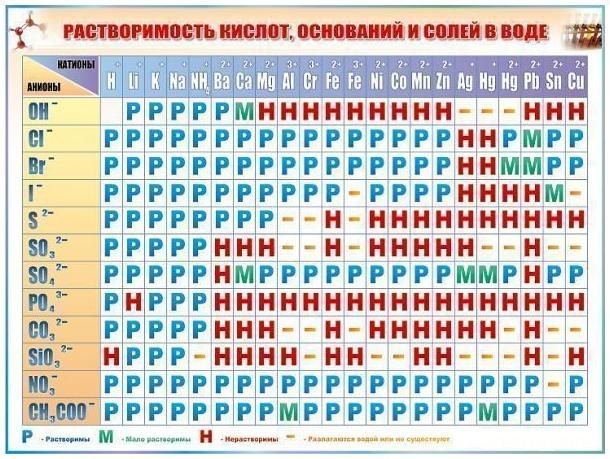
Последняя реакция не идет, так как основание Fe(ОН)3 нерастворимо в воде. Растворимость веществ в воде можно определить по таблице растворимости (рис. 2).
При определении возможности протекания данной реакции можно использовать и другое правило.
Основный оксид реагирует с водой, если он образован активным металлом. Такие металлы стоят в ряду напряжений до магния (см. табл. 3).
Задание 2.9. Составьте уравнения реакций с водой для основных оксидов из задания 2.5, зная, что реакции идут по схеме:
основный оксид + вода → основание
2. Основные оксиды реагируют с кислотами, образуя соль и воду:
Обратите внимание: при составлении формулы соли нужно вместо атомов водорода в формуле кислоты написать символ металла, а затем составить полученную формулу по валентности.
Задание 2.10. Составьте уравнения реакций с Н2SО4 для основных оксидов из задания 2.5, зная, что реакции идут по схеме:
основный оксид + кислота → соль + вода
3. Основные оксиды реагируют с кислотными оксидами, образуя соль (см. задание 2.7).
4. Некоторые основные оксиды реагируют при нагревании с водородом, при этом образуется металл и вода:
ЗАПОМНИТЕ! Основные оксиды с основаниями и основными оксидами НЕ РЕАГИРУЮТ!
ВЫВОД. В реакцию легче всего вступают вещества с противоположными свойствами, и не вступают в реакцию вещества со сходными свойствами.
Свойства амфотерных оксидов
Амфотерные оксиды (от греч. amphi — двойной) проявляют двойственные свойства: они могут реагировать и с кислотами, и с основаниями (точнее, со щелочами). При этом образуются соль и вода.
Например,
* Такая реакция не происходит, но эта схема позволяет определить состав «кислотного остатка» и его валентность, а затем составить химическую формулу соли.
Задание 2.11. Составьте уравнения реакций с КОН и с НNО3 для амфотерных оксидов из задания 2.5.
Задание 2.12. С какими веществами (Н2О, NаОН, НСl) могут реагировать оксиды: Cr2O3, CrO, SO3, V2O5?
Составьте уравнения необходимых реакций. При составлении уравнений реакций помните:
- реагируют вещества с противоположными свойствами;
- сначала определите, какой это оксид (см. задание 2.5);
- затем, исходя из свойств этого оксида, составьте уравнения, пользуясь схемами заданий 2.6–2.10 и вышеприведенными уравнениями реакций для амфотерных оксидов.
Способы получения оксидов
Оксиды могут быть получены при разложении некоторых кислот, оснований, солей:
Оксиды обычно получают при сгорании в кислороде простых и сложных веществ:
Обратите внимание! При сгорании сложных веществ образуются оксиды элементов, которые входят в его состав. Исключение составляют только азот и галогены (F, Cl, Br, I), которые выделяются в виде простых веществ. Например:
Выводы
Молекулы оксидов состоят из атомов двух элементов. Один из этих элементов — кислород. Оксиды, образующие соли, бывают кислотные, амфотерные и основные. Оксиды реагируют с веществами, которые проявляют противоположные свойства.
- Основные оксиды — с кислотными оксидами или кислотами.
- Кислотные оксиды — с основными оксидами или основаниями.
- Амфотерные — и с кислотами, и с основаниями (щелочами).
В каждой из таких реакций образуется соль и вода.
Кислоты
Кислоты — это сложные вещества, в состав молекул которых входит активный атом водорода и кислотный остаток. Этот активный атом водорода в химических реакциях способен замещаться на атом металла, в результате чего всегда получается соль.
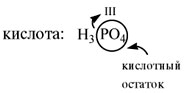
В формулах неорганических кислот этот атом водорода записывается на первом месте*:
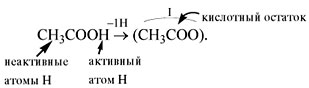
* В химических формулах органических кислот атом водорода стоит в конце, например, CH3–COOH уксусная кислота
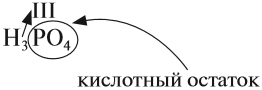
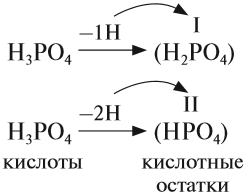
В состав любой кислоты кроме атомов водорода входит кислотный остаток. Кислотный остаток — это часть молекулы кислоты без атомов водорода (которые могут быть замещены на атом металла). Валентность кислотного остатка равна числу таких атомов водорода:
При определении валентности кислотного остатка учитываются те атомы водорода, которые участвовали в реакции или могут участвовать в ней. Так, фосфорной кислоте Н3РО4, в зависимости от условий, могут соответствовать кислотные остатки иного состава:
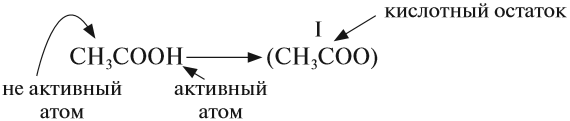
У органических кислот не все атомы водорода в молекуле способны замещаться на атом металла:
Задание 2.13. Определите состав и валентность кислотных остатков для кислот, учитывая, что все атомы водорода кислот участвуют в реакции:
По числу атомов водорода кислоты делят на одноосновные и многоосновные:
- НСl — одноосновная, так как один атом водорода;
- Н2СО3 — двухосновная, так как два атома водорода.
По составу кислоты делят на:
- бескислородные: НСl, Н2S;
- кислородсодержащие: НСlO, Н2SO4.
Бескислородные кислоты представляют собой растворы некоторых газов в воде, при этом и растворённому газу, и полученному раствору приписывают одинаковые свойства, хотя это не так. Например, из простых веществ водорода и хлора получается газ хлороводород:
Этот газ не проявляет кислотных свойств, если он сухой: его можно перевозить в металлических ёмкостях, и никакой реакции не происходит. Но при растворении хлороводорода в воде получается раствор, который проявляет свойства сильной кислоты, её перевозить в металлических ёмкостях нельзя! Этот раствор называется «соляная кислота».
Названия бескислородных кислот составляют по принципу:
«ЭЛЕМЕНТ» + «ВОДОРОД»ная кислота
- H2S — сероводородная кислота (это раствор газа сероводорода в воде);
- НСl — хлороводородная (соляная) кислота (это раствор газа хлороводорода в воде);
- НF — фтороводородная (плавиковая) кислота (это раствор газа фтороводорода в воде).
Кислородсодержащие кислоты могут быть получены при действии воды на кислотные оксиды (см. задание 2.6). Исходные кислотные оксиды называются «АНГИДРИДЫ кислот»:
Метафосфорная кислота неустойчива и, присоединяя воду, превращается в более устойчивую кислоту:
или в суммарном виде:
Таким образом, Р2O5 — ангидрид фосфорной кислоты, а также некоторых других, менее устойчивых кислот.
Обратите внимание! Название кислородосодержащей кислоты содержит в виде корня название элемента, входящего в состав ангидрида:
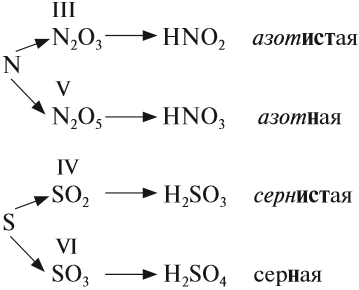
Если элементу соответствуют несколько кислот, то для кислоты с большей валентностью элемента, входящего в состав ангидрида, в названии употребляют суффикс «Н» или «В». Для кислот с меньшей валентностью элемента в названиях добавляют еще один суффикс «ИСТ».
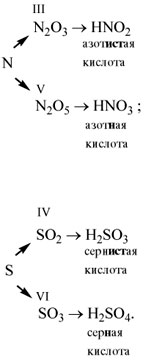
Валентность элемента проще всего определять по формуле ангидрида:
Обратим внимание, что в названии сернистой кислоты основной суффикс -ИСТ-, а суффикс -Н- введён дополнительно для благозвучия.
Сведём всё известное о названиях кислот в таблицу 4.
Задание 2.14. Заполнить табл. 4, заменив знаки вопросов формулами и названиями соответствующих кислот.
Задание 2.15. Напишите НА ПАМЯТЬ формулы кислот: кремниевой, сернистой, серной, сероводородной, азотистой, азотной, соляной, фосфорной, угольной. Укажите ангидриды этих кислот (там, где они существуют).
Свойства кислот
Главным свойством всех кислот является их способность образовывать соли. Соли образуются в любой реакции, в которой участвует кислота, при этом замещаются активные атомы водорода (один, все или несколько).
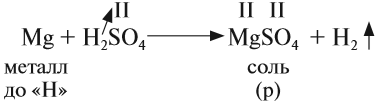
1. Кислоты реагируют с металлами, при этом атом водорода кислоты замещается на атом металла — в результате образуется растворимая соль* и водород:
* Если образуется нерастворимая соль, то эта соль закрывает поверхность металла и реакция останавливается.
Не все металлы способны вытеснять водород из растворов кислот: этот процесс возможен только для тех металлов, которые стоят в ряду напряжений ДО водорода (рис. 3 или таблица 3).
Задание 2.16. Составьте уравнения возможных реакций:
- серная кислота + алюминий →
- соляная кислота + серебро →
- бромоводородная кислота + цинк →
При составлении уравнений пользуйтесь рядом напряжений и схемой реакции:
кислота + металл (до водорода) → соль + водород
Не забывайте, составляя формулы солей, учитывать валентность металла и кислотного остатка.
Некоторые кислоты могут растворять металлы, которые стоят в ряду напряжения после водорода, но водород при этом не выделяется:
2. Кислоты реагируют с основаниями, образуя соль и воду*. Это реакция обмена, и поэтому валентность составных частей в результате реакции не меняется:
* Реакция между кислотой и основанием называется реакцией нейтрализации.
Расставим коэффициенты:
Задание 2.17. Составьте аналогичные уравнения реакций по схеме:
кислота + основание → соль + вода
для:
- серной кислоты и Fe(ОН)3;
- соляной кислоты и Ва(ОН)2;
- сернистой кислоты и NаОН.
Не забудьте:
- составить формулу соли по валентности металла и кислотного остатка;
- расставить коэффициенты.
3. Кислоты могут реагировать с солями. При этом сильная кислота вытесняет более слабую из её соли.
- К сильным кислотам относятся: серная, азотная, соляная и др.
- К слабым кислотам относятся: угольная, кремниевая, сероводородная, азотистая.
Происходит реакция обмена: образуется новая соль и новая кислота.
Более подробно о подобных реакциях см. в уроке 6.
Задание 2.18. Составьте НА ПАМЯТЬ формулы: а) сильных, б) слабых кислот.
Задание 2.19. Составьте уравнения реакций по схеме:
(более сильная) кислота + соль → соль + кислота (более слабая):
- соляная кислота + FeS →
- азотная кислота + Na2SiO3 →
- серная кислота + K2CO3 →
4. И, наконец, выяснив свойства кислот, зададим себе вопрос: а можно ли обнаружить кислоту в растворе? Например, в одном стакане налита вода, а в другом — раствор кислоты. Как определить, где кислота? Хотя многие кислоты кислые на вкус, пробовать их НЕЛЬЗЯ — это опасно! Выручают особые вещества — ИНДИКАТОРЫ. Это соединения, которые изменяют цвет в присутствии кислот:
- синий ЛАКМУС становится красным;
- оранжевый МЕТИЛОРАНЖ тоже становится красным.
Выводы
Кислоты классифицируются:
- по числу атомов водорода на одноосновные, двухосновные и т. д.,
- по наличию атома кислорода в составе молекулы на бескислородные и кислородсодержащие,
- по силе на сильные и слабые,
- по устойчивости на устойчивые и неустойчивые.
Кислоты реагируют:
- с активными металлами (до «Н»),
- с основаниями,
- с основными и амфотерными оксидами,
- с солями более слабых кислот.
Кислоты обнаруживаются индикаторами в кислой («красной») области.
Основания
Основания — это сложные соединения, в состав молекул которых входит атом металла и гидроксогруппа ОН:
Валентность ОН-группы равна I.
Основания называют по схеме:
гидроксид (чего?) металла (n),
где n — переменная валентность металла.
Например:
- Са(ОН)2 — гидроксид кальция,
- Fе(OH)3 — гидроксид железа (III),
- NH4OH — гидроксид аммония.
Обратите внимание. В состав последнего основания не входит атом металла. Это исключение. Валентность группы NН4 (аммоний) равна I.
Основания бывают растворимые в воде и нерастворимые в воде. Это легко определить по таблице растворимости.
Растворимые в воде основания называются ЩЕЛОЧАМИ. В состав щелочей входят атомы активных металлов (они находятся в начале ряда напряжений, до магния). Гидроксид аммония тоже относится к щелочам, так как существует только в растворах.
Задание 2.20. Составьте, пользуясь таблицей растворимости или рядом напряжений, химические формулы 2–3 щелочей.
Свойства и способы получения щелочей
Щёлочи можно получить действием активного металла (К, Nа, Cа, Ва) или его оксида на воду:
1. Растворы щелочей реагируют с кислотными и амфотерными оксидами (см. урок 2.1) и с кислотами (см. урок 2.2). Последняя реакция называется реакцией НЕЙТРАЛИЗАЦИИ:
Реакция нейтрализации характерна для всех кислот!
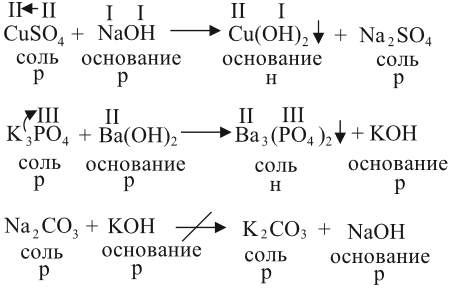
2. Растворы щелочей реагируют с растворами солей. Реакция происходит, если образуется хотя бы одно нерастворимое соединение. Эта реакция относится к реакциям обмена, т. е. в результате получается новая соль и новое основание:
- Последняя реакция не происходит, так как оба полученных вещества растворимы в воде.
- Валентности составных частей исходных молекул определяйте по кислотному остатку или по числу групп ОН.
- Полученные значения валентностей используйте при составлении формул полученных веществ.
- Растворимость получаемых веществ определяйте по таблице растворимости.
Задание 2.21. Расставьте коэффициенты в вышеприведённых уравнениях реакций.
Задание 2.22. Составьте уравнения реакций обмена:
- Fe(NO3)3 + гидроксид калия →
- Na2SO3 + гидроксид кальция →
- K3PO4 + гидроксид аммония →
Определите, какая из реакций не происходит и почему.
3. Растворы щелочей, как и растворы кислот, способны изменять окраску индикаторов:
- фиолетовый лакмус синеет,
- оранжевый метилоранж желтеет,
- бесцветный фенолфталеин краснеет.
Все изменения окрасок индикаторов можно свести в таблицу 5.
Обратите внимание: если к воде добавить кислоты, то в растворе будет кислая среда; если добавить щелочь — щелочная; в чистой воде среда нейтральная.
Вопрос 1. Можно ли при помощи фенолфталеина узнать, что налито в стакане: вода? НCl? КОН? А при помощи лакмуса?
Вопрос 2. Почему реакция между кислотой и щелочью названа реакцией нейтрализации?
Свойства и способы получения нерастворимых в воде оснований
Среди нерастворимых в воде оснований следует выделить особую группу веществ — амфотерные гидроксиды. Их свойства будут рассмотрены ниже. Способы получения их такие же, как и для нерастворимых оснований.
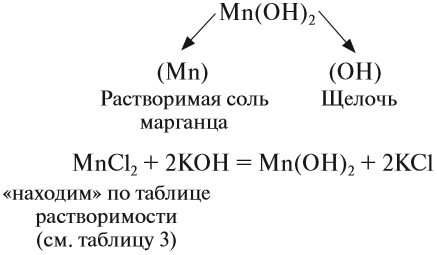
Нерастворимые основания получают, действуя на раствор соли, в состав которой входит нужный атом металла, раствором щёлочи:
Попробуем определить, какие вещества нужно взять для того, чтобы получить гидроксид марганца (II):
Задание 2.23. Напишите уравнения реакций, при помощи которых можно получить: а) гидроксид железа (III), б) гидроксид железа (II).
Свойства нерастворимых в воде оснований во многом отличаются от свойств щелочей: нерастворимые в воде основания не могут реагировать с растворами солей, а также с амфотерными и некоторыми кислотными оксидами. Они не изменяют окраску индикатора.
1. Нерастворимые основания могут реагировать с кислотами, если при этом происходит растворение исходного нерастворимого вещества (осадка):
Таким образом, эта реакция возможна, если образуется растворимая соль (см. таблицу 3).
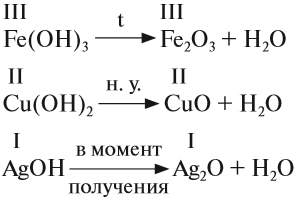
2. Нерастворимые основания разлагаются при нагревании. При этом, чем меньше активность металла (см. ряд напряжений), тем легче разлагается основание на оксид и воду:
Свойства амфотерных гидроксидов
Амфотерные гидроксиды соответствуют амфотерным оксидам. Это означает, что в состав амфотерного гидроксида входит тот же атом металла и с той же валентностью, что и в состав амфотерного оксида:
Как вы думаете, почему эти вещества называются амфотерными? (Если ответить не можете — загляните в урок 2.1.)
Ответ простой — амфотерные соединения проявляют двойственные свойства, т. е. реагируют) и с кислотами, и со щелочами (и растворяются при этом):
Если эта реакция происходит с растворами щелочей, то вместо вещества состава Na3AlO3 (или NaAlO2)* образуется сложное комплексное соединение:
* Ортоалюминиевая кислота H3AlO3 теряет молекулу H2O, и образуется метаалюминиевая кислота HAlO2, в которой кислотный остаток AlO2 имеет валентность I.
Задание 2.24. Составьте уравнения реакций с кислотой и со щёлочью для амфотерных гидроксидов: а) гидроксида цинка; б) гидроксида хрома (III).
Выводы
Молекулы неорганических оснований содержат гидроксогруппу ОН. Все неорганические основания, кроме NH4OH, содержат атом металла. Основания делят на растворимые в воде (щёлочи) и нерастворимые в воде.
Растворы щёлочей реагируют:
- с кислотами (реакция нейтрализации),
- с кислотными и амфотерными оксидами,
- с растворами солей.
Щёлочи обнаруживаются индикаторами в щелочной («синей») области. Нерастворимые в воде основания не изменяют окраску индикатора, могут реагировать с некоторыми кислотами и кислотными оксидами, а также термически неустойчивы.
Соли
Соли — это продукт реакции между кислотой и основанием, например реакции нейтрализации. Даже если такая реакция невозможна, ЛЮБОЙ соли можно поставить в соответствие основание и кислоту. Поэтому в состав любой соли входит остаток основания (обычно атом металла или группа NH4) и остаток кислоты (кислотный остаток).
Задание 2.25. Попробуйте определить для каждой из этих солей
где в её молекуле остаток кислоты, а где — остаток основания. Определите валентности составных частей.
Обратите внимание, что в состав некоторых солей входят атомы водорода или группы ОН. Такое различие подсказывает, что соли могут быть разных типов. Рассмотрим три вида солей.
Средние соли. Такие соли получаются, если кислота и основание полностью прореагировали:
Кислые соли. Такие соли получаются, если не все атомы водорода кислоты были замещены на атом металла:
Кислотные остатки таких солей содержат атом водорода. Кислые соли образуются в результате гидролиза некоторых солей, а также при взаимодействии средней соли с ангидридом «своей» кислоты:
Кислые соли могут проявлять некоторые свойства кислот, например они могут реагировать с щелочами:
Основные соли. Такие соли образуются, если не все группы ОН основания замещены на кислотный остаток:
Такие соли содержат гидроксогруппу ОН. Основные соли образуются в результате гидролиза некоторых солей. Основные соли могут проявлять некоторые свойства оснований. Например, они могут реагировать с кислотами:
Способы получения солей
Вспомните, во многих примерах, которые иллюстрировали свойства оксидов, кислот, оснований, — продуктом реакции была соль. Попробуем обобщить эти сведения и выяснить, в результате каких процессов можно получить СОЛЬ заданного состава. Прежде всего, отметим, что способы получения солей можно условно разбить на 2 группы:
- I — получение солей из веществ, которые не являются солями;
- II — получение солей из других солей.
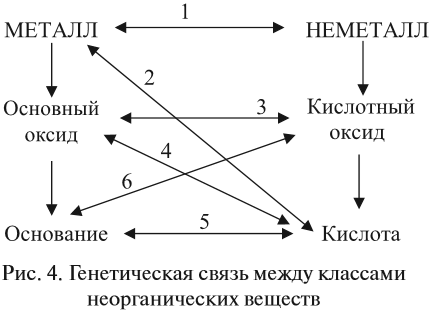
Реакции I группы основаны на том, что в реакцию вступают противоположные по свойствам вещества (рис. 4).
Приведём конкретные примеры:
1. Металл + неметалл (галоген или сера):
2. Металл + кислота:
3. Основный оксид + кислотный оксид:
4. Основный оксид + кислота:
5. Основание + кислота:
6. Основание + кислотный оксид:
Задание 2.26. Расставьте коэффициенты в этих уравнениях. Приведите свои примеры каждого типа.
Реакции II группы являются реакциями обмена или замещения. В каждой из таких реакций участвует соль, и поэтому способы получения солей по группе II фактически являются химическими свойствами солей:
7. Более активный металл вытесняет менее активный из растворов его солей:
обратный процесс не идёт:
Активность металлов можно определять по ряду напряжений:
В этом ряду любой металл активнее всех металлов, стоящих после него (правее него).
8. Сильная кислота вытесняет более слабую кислоту из её соли:
9. Щёлочь, реагируя с солью, образует новое основание и новую соль
Эта реакция происходит, если оба исходных вещества растворимы, а хотя бы одно из полученных веществ — нерастворимо.
10. Соль, вступая в реакцию обмена с другой солью, образует две новые соли
Эта реакция также происходит, если оба исходных вещества растворимы, а хотя бы одно из полученных веществ — нерастворимо.
Например, эта реакция:
невозможна, так как обе полученные соли растворимы. А этот процесс:
невозможен потому, что СаСО3 (мел) нерастворим в воде.
Названия солей
Названия солей происходят от латинского названия химического элемента, который входит в состав кислотного остатка (исключая кислород):
- S — сульфур;
- N — нитрогениум;
- С — карбонеум;
- Si — силициум.
Например:
Очевидно, что для солей разного состава должны быть разные названия. Это достигается введением суффиксов:
- для солей бескислородных кислот -ИД-;
- для солей кислородсодержащих кислот -ИТ- (меньшая валентность элемента), АТ- (бОльшая валентность элемента).
Задание 2.27. Составьте названия вышеприведённых солей серусодержащих кислот.
При правильной работе должно получиться:
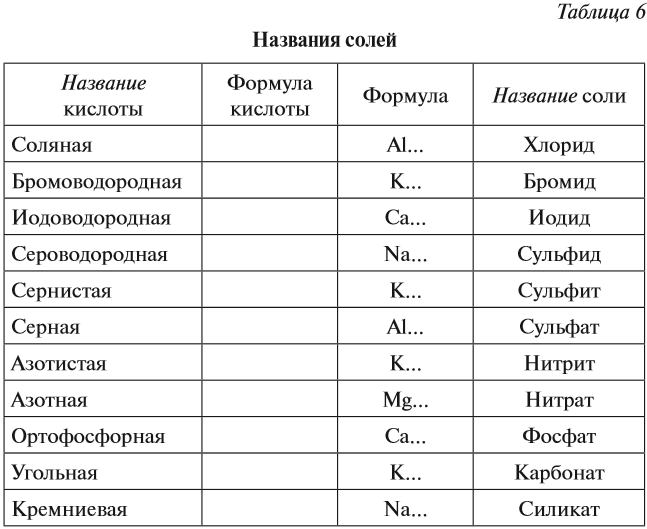
Аналогично составляют названия остальных солей (табл. 6).
Задание 2.28. Дополните таблицу 6, составив химические формулы солей тех металлов, которые указаны в таблице.
При составлении названий кислых солей используют частицу «гидро»:
При составлении названий основных солей используют частицу «гидроксо»:
Задание 2.29. Назовите все соли, которые встречаются в тексте и уравнениях реакций этого раздела.
Задание 2.30. Составьте по 3–4 уравнения реакций получения:
- бромида магния;
- сульфата цинка.
Выводы
Соли состоят из остатков веществ, которые проявляют противоположные свойства: кислоты и основания.
Е.Н.ФРЕНКЕЛЬ
Самоучитель по химии
Пособие для тех, кто не знает, но хочет
узнать и понять химию
Продолжение. Начало см. в № 13/2007
Глава 2. Важнейшие классы
неорганических соединений
2.1. Оксиды
Оксиды – сложные вещества, которые состоят из
атомов двух химических элементов, один из
которых кислород.
Определим, какое из следующих соединений оксид:
PH3, H3PO4, P2O5.
К оксидам относят соединение P2O5.
Два других вещества – не оксиды: в состав РН3
не входит атом кислорода, а в состав H3PO4 входят
атомы трех химических элементов – H, Р, O.
Названия оксидов складываются из двух слов:
первое слово – «оксид», второе слово – название
химического элемента, образующего данный оксид,
в родительном падеже. Например: СаО – оксид
кальция.
Если оксид образован химическим элементом с
переменной валентностью, то после названия
элемента нужно указать его валентность.
Например: Fe2О3 – оксид железа(III), FеО –
оксид железа(II).
Задание 2.1. Среди следующих соединений
найдите оксиды и назовите их:
N2O3, NH3, MnO2, H2O,
HCl, NaOH, Na2O, P2O5, H2SO4.
Задание 2.2. Составьте формулы следующих
оксидов:
оксид хрома(III), оксид углерода(IV), оксид магния,
оксид серы(VI), оксид азота(V), оксид калия, оксид
марганца(VI).
Многие оксиды могут реагировать с кислотами
или основаниями. В таких реакциях получаются
соли. Поэтому такие оксиды называются солеобразующими.
Однако существует небольшая группа оксидов,
которые к таким реакциям не способны. Такие
оксиды называют несолеобразующими.
Задание 2.3. Назовите несолеобразующие оксиды:
H2O, CO, N2O, NO, F2O.
Некоторые оксиды имеют особые (тривиальные)
названия: Н2О – вода, СО – угарный газ, СО2
– углекислый газ и др.
Солеобразующие оксиды подразделяют на три
группы: основные, кислотные, амфотерные.
Точно установить характер оксида можно, только
изучая его химические свойства. Например,
кислотные оксиды реагируют с основаниями и не
реагируют с кислотами. Основные оксиды реагируют
с кислотами и не реагируют с основаниями.
Амфотерные оксиды могут реагировать и с
кислотами, и с основаниями.
По формуле оксида можно определить, какими
свойствами он обладает. Правда, иногда эта оценка
будет приблизительной.
• Неметаллы образуют только кислотные и
безразличные оксиды.
• Металлы в зависимости от валентности могут
образовывать разные оксиды – основные, амфотерные
и кислотные.
Предсказать свойства оксида металла может
помочь эта схема:
Основные оксиды металлов от кислотных оксидов
металлов отличить легко: малая валентность
металла – основный оксид, большая – кислотный.
Как быть с амфотерными оксидами? «Любимая»
валентность металлов в этих оксидах III, но есть и
исключения. Поэтому желательно запомнить
формулы наиболее часто встречающихся амфотерных
оксидов: ZnO, Al2O3, SnO, PbO, Cr2O3.
Задание 2.4. Назовите амфотерные оксиды:
ZnO, SnO, PbO, Al2O3, Cr2O3.
Задание 2.5. Классифицируйте приведенные
ниже оксиды:
V2O5, SO2, ZnO, Fe2O3,
SO3, CO2, Li2O, FeO, Al2O3, H2O,
BaO.
Задание рекомендуется выполнить по следующей
схеме.
1) Определить, какой это оксид – солеобразующий
или несолеобразующий.
2) Определить, какой элемент входит в состав
солеобразующего оксида – металл или неметалл.
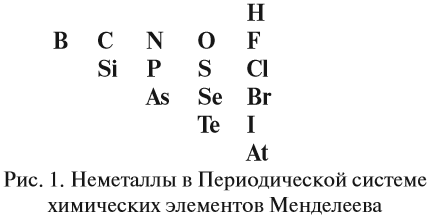
Для этого надо выписать из таблицы
Д.И.Менделеева символы элементов-неметаллов. Они
расположены в главных подгруппах на линии бор –
астат и выше этой линии (рис. 1).
|
|
Рис. 1. Элементы-неметаллы
|
3) Если в состав оксида входит атом
неметалла, то оксид кислотный.
4) Если в состав оксида входит атом металла, то
следует определить его валентность и по ней
выяснить характер оксида – основный, амфотерный
или кислотный.
Например: Cr2O3 – амфотерный, т.к. хром
– металл с валентностью III;
N2O3 – кислотный оксид, т.к. азот –
неметалл;
CrO3 – кислотный оксид, т.к. хром – металл с
высокой валентностью VI.
Зная характер оксида, можно описать его
свойства.
Свойства кислотных оксидов
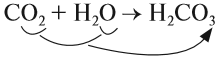
• Кислотные оксиды реагируют c водой, образуя
кислоты. Например:
CO2 + H2O = H2CO3.
Чтобы составить формулу кислоты, нужно сложить
все атомы исходных веществ, записывая на первом
месте атом водорода, на втором – элемент,
образующий оксид, и на последнем – кислород. Если
индексы получились четными, то их можно
сократить:
N2O3 + H2O = H2N2O4
(2HNO2).
Эти же реакции можно записать в виде
арифметического примера:
Задание 2.6. Составьте уравнения реакций
кислотных оксидов из задания 2.5 с водой.
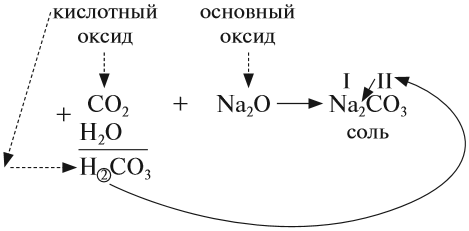
• Кислотные оксиды реагируют с осно?вными
оксидами, образуя соли соответствующей кислоты,
т.е. соль той кислоты, которая образуется при
взаимодействии этого оксида с водой. Например:
Чтобы составить такое уравнение, нужно
действовать по следующей схеме.
1) Составить формулу кислоты (прибавив к
молекуле оксида молекулу воды):
CO2 + H2O = H2CO3.
2) Определить валентность кислотного остатка
(это часть молекулы кислоты без атомов водорода).
В данном случае кислотный остаток имеет
состав СО3, его валентность равна числу
атомов водорода в кислоте, т.е. II.
3) Cоставить формулу соли, записав вместо атомов
водорода атом металла из основного оксида с его
валентностью (в данном случае натрий).
4) Составить формулу соли по валентности
металла и кислотного остатка: Na2CO3.
Задание 2.7. Составьте уравнения реакций
кислотных оксидов из задания 2.5 с оксидом
кальция.
• Кислотные оксиды реагируют с основаниями,
образуя соль соответствующей кислоты и воду.
Например:
Принципы составления уравнений реакций с
основаниями те же, что и для реакций с
осно?вными оксидами (см. выше).
Задание 2.8. Составьте уравнения реакций
кислотных оксидов из задания 2.5 с гидроксидом
натрия NаОН.
З а п о м н и т е! Кислотные оксиды ни с кислотами,
ни c кислотными оксидами не реагируют.
Свойства основных оксидов
• Основные оксиды реагируют с водой,
образуя основания. Реакция протекает, если
получающееся основание растворимо в воде.
Общая формула оснований – М(ОН)х, где х
– число ОН-групп, равное валентности металла М.
Например:
СаО + Н2О = Са(ОН)2,
Fe2O3 + Н2О нет реакции.
Последняя реакция не идет, т.к. основание Fe(ОН)3
нерастворимо в воде. Растворимость веществ в
воде можно определить по таблице растворимости
(рис. 2).
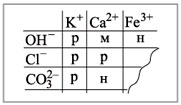 |
Рис. 2.
|
Условные обозначения: р – растворимо в воде, м
– малорастворимо в воде,
н – нерастворимо в воде.
При определении возможности протекания данной
реакции можно использовать и другое правило.
Основный оксид реагирует с водой, если он
образован активным металлом. Эти металлы стоят в
ряду напряжений до магния: Li, K, Ba, Ca, Na, Mg…
Задание 2.9. Составьте уравнения реакций основных
оксидов из задания 2.5 с водой.
• Основные оксиды реагируют с
кислотами, образуя соль и воду:
Обратите внимание: при составлении формулы
соли нужно вместо атомов водорода в формуле
кислоты написать символ металла, а затем
расставить индексы согласно валентности.
Задание 2.10. Составьте уравнения реакций
осно?вных оксидов из задания 2.5 с Н2SО4.
• Основные оксиды реагируют с
кислотными оксидами, образуя соли.
• Некоторые основные оксиды
реагируют при нагревании с водородом, при этом
образуются металл и вода:
CuO + H2 = Cu + H2O.
З а п о м н и т е! Основные оксиды с
основаниями и основными оксидами не
реагируют!
В ы в о д. В реакцию легче всего вступают
вещества с противоположными свойствами и не
вступают в реакцию вещества со сходными
свойствами.
Свойства амфотерных оксидов
Амфотерные оксиды (от греч. amphi – двойной)
проявляют двойственные свойства: они могут
реагировать и с кислотами, и с основаниями
(точнее, со щелочами). При этом образуются соль и
вода. Например:
Задание 2.11. Составьте уравнения реакций
амфотерных оксидов из задания 2.5 с КОН и НNО3.
Задание 2.12. С какими из веществ – Н2О,
NаОН, НСl – могут реагировать следующие оксиды:
Cr2O3, CrO, SO3, V2O5?
Составьте уравнения возможных реакций.
Способы получения оксидов
Оксиды могут быть получены при разложении
некоторых кислот, оснований, солей:
H2SO3 = SO2 + H2O,
Cu(OH)2 = CuO + H2O,
Са(НСО3)2 = Н2О + СО2
+ СаСО3.
Оксиды обычно получают сжиганием в кислороде
простых и сложных веществ:
2Mg + O2 = 2MgO,
C + O2 = CO2,
2H2 + O2 = 2H2O,
CH4 + 2O2 = CO2 + 2H2O.
Обратите внимание: при сгорании сложного
вещества образуются оксиды элементов, которые
входят в его состав. Исключение составляют
только азот и галогены, которые выделяются в виде
простых веществ.
В ы в о д ы по главе 2.1
Молекулы оксидов состоят из атомов двух
элементов. Один из этих элементов – кислород.
Оксиды, образующие соли, бывают кислотными,
амфотерными и основными.
Оксиды реагируют с веществами, которые
проявляют противоположные свойства.
Основные оксиды реагируют с
кислотными оксидами или кислотами, кислотные
оксиды – с основными оксидами или
основаниями, амфотерные оксиды – и с кислотами, и
с основаниями (щелочами).
2.2. Кислоты
Кислоты – это сложные вещества, в состав
молекул которых входят активные атомы водорода и
кислотные остатки. Активный атом водорода в
химических реакциях способен замещаться на атом
металла, в результате чего всегда получается
соль.
В формулах неорганических кислот атом водорода
записывается на первом месте*.
Например:
В состав молекулы любой кислоты кроме атомов
водорода входит кислотный остаток. Кислотный
остаток – это часть молекулы кислоты без атомов
водорода (которые могут быть замещены на атом
металла). Валентность кислотного остатка равна
числу таких атомов водорода:
При определении валентности кислотного
остатка учитываются те атомы водорода, которые
участвовали в реакции или могут участвовать в
ней. Так, фосфорной кислоте Н3РО4 в
зависимости от условий могут соответствовать
кислотные остатки разного состава:
У органических кислот не все атомы водорода в
молекуле способны замещаться на атом металла:
Задание 2.13. Определите состав и валентность
кислотных остатков для кислот, учитывая, что все
атомы водорода кислот активные:
HNO3, H2S, NaHCO3, H2SO3,
KOH, HMnO4.
По числу атомов водорода в молекулах кислоты
делят на одноосновные и многоосновные.
Например:
HCl – одноосновная кислота, т. к. в ее молекуле
один атом водорода;
Н2СО3 – двухосновная кислота, т. к. в
ее молекуле два атома водорода.
По составу кислоты делят на бескислородные
(НСl, Н2S) и кислородсодержащие (НСlO, Н2SO4).
Бескислородные кислоты представляют собой
растворы некоторых газов в воде, при этом и
растворенному газу, и полученному раствору
приписывают одинаковые свойства, хотя это не так.
Например, из простых веществ водорода и хлора
получается газ хлороводород:
H2 + Cl2 = 2HCl.
Этот газ не проявляет кислотных свойств, если
он сухой: его можно перевозить в металлических
емкостях, и никакой реакции не происходит.
Но при растворении хлороводорода в воде
получается раствор, который проявляет свойства
сильной кислоты. Такую кислоту перевозить в
металлических емкостях нельзя.
Названия бескислородных кислот составляют по
схеме:
элемент + водород + «ная» кислота.
Например: H2S – сероводородная кислота
(раствор газа сероводорода в воде).
Некоторые бескислородные кислоты имеют особые
(тривиальные) названия: НСl – соляная кислота
(раствор газа хлороводорода в воде), НF –
плавиковая кислота (раствор газа фтороводорода в
воде).
Задание 2.14. Дайте химические названия
соляной и плавиковой кислотам.
Кислородсодержащие кислоты могут быть
получены при действии воды на кислотные оксиды
(см. выше). Исходные кислотные оксиды называют
«ангидриды кислот»:
Метафосфорная кислота неустойчива и,
присоединяя воду, превращается в более
устойчивую ортофосфорную кислоту:
Или в суммарном виде:
Р2О5 + 3Н2О = 2Н3РО4
.
Таким образом, Р2O5 – ангидрид
фосфорной кислоты, а также некоторых других,
менее устойчивых кислот.
Обратите внимание: название
кислородсодержащей кислоты содержит в виде
корня название элемента, входящего в состав
ангидрида: фосфор Р
фосфорный ангидрид Р2О5 фосфорная кислота Н3РО4.
Если элементу соответствует несколько кислот,
то для кислоты с большей валентностью
элемента, входящего в состав ангидрида, в
названии употребляют суффиксы «н» или «в».
Для кислот с меньшей валентностью элемента в
название кислоты добавляют суффикс «ист».
Валентность элемента проще всего определять по
формуле ангидрида:
В названии сернистой кислоты основной суффикс
«ист», а суффикс «н» введен дополнительно для
благозвучия.
Сведения о названиях некоторых кислот обобщены
в табл. 3.
Таблица 3
Названия кислот
| Ангидрид | Кислота | Название |
| Нет | НС1 | Соляная, хлороводородная |
| CO2 | Н2СО3 | Угольная |
| SiO2 | …………… | Кремниевая |
| N2O3 | …………… | Азотистая |
| N2O5 | …………… | Азотная |
| SO2 | …………… | …………………….. |
| SO3 | …………… | …………………….. |
| P2O5 | …………… | …………………….. |
| CrO3 | …………… | Хромовая |
| Нет | H2S | Сероводородная |
Задание 2.15. Вместо пропусков в табл.
3 напишите формулы и названия соответствующих
кислот.
Задание 2.16. Напишите на память (никуда не
заглядывая) формулы кислот: кремниевой,
сернистой, серной, сероводородной, азотистой,
азотной, соляной, фосфорной, угольной. Укажите
ангидриды этих кислот (там, где они существуют).
Свойства кислот
Главным свойством всех кислот является их
способность образовывать соли. Соль образуется в
любой реакции, в которой участвует кислота, при
этом замещаются активные атомы водорода (один
или несколько).
• Кислоты реагируют с металлами. При этом атомы
водорода кислоты замещаются на атомы металла с
образованием растворимой соли и водорода.
Например:
Не все металлы способны вытеснять водород из
растворов кислот. Этот процесс возможен только
для тех металлов, которые стоят в ряду напряжений
(ряд активности) до водорода (рис. 3, см. с. 20):
 |
Рис. 3. Ряд напряжений металлов |
Задание 2.17. Составьте уравнения
возможных реакций:
серная кислота + алюминий,
соляная кислота + серебро,
бромоводородная кислота + цинк.
При составлении уравнений пользуйтесь рядом
напряжений. Не забывайте, составляя формулы
солей, учитывать валентности металла и
кислотного остатка.
Некоторые кислоты могут растворять металлы,
которые стоят в ряду напряжения после водорода,
но водород при этом не выделяется:
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O.
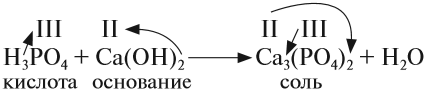
• Кислоты реагируют с основаниями, образуя
соль и воду**. Это реакция
обмена, и поэтому валентность составных частей в
результате реакции не меняется:
Расставим коэффициенты:
2Н3РО4 + 3Са(ОН)2 = Са3(РО4)2
+ 6Н2О.
Задание 2.18. Составьте уравнения реакций:
серной кислоты и Fe(ОН)3,
соляной кислоты и Ва(ОН)2,
сернистой кислоты и NаОН.
Не забудьте порядок действий: составить
формулу соли по валентности металла и кислотного
остатка; расставить коэффициенты.
• Кислоты могут реагировать с солями. При этом
сильная кислота вытесняет более слабую из ее
соли.
К сильным кислотам относятся серная, азотная,
соляная и др.
К слабым кислотам относятся угольная,
кремниевая, сероводородная, азотистая.
В реакции обмена кислоты с солью образуются
новая соль и новая кислота. Например:
2HNO3 + CaCO3 = Ca(NO3)2 + H2CO3.
Более подробно о подобных реакциях см. главу 6.
Задание 2.19. Составьте, не обращаясь к
учебнику и пособиям, формулы: а) сильных кислот;
б) слабых кислот.
Задание 2.20. Составьте уравнения реакций:
соляная кислота + FeS,
азотная кислота + Na2SiO3,
серная кислота + K2CO3.
• Как обнаружить кислоту в растворе? Например,
в одном стакане налита вода, а в другом – раствор
кислоты. Как определить, где кислота? Хотя все
кислоты кислые на вкус, пробовать их нельзя, это
опасно. Выручают особые вещества – индикаторы.
Это соединения, которые изменяют цвет в
присутствии кислот.
Синий лакмус в кислоте становится красным;
оранжевый метилоранж тоже становится красным в
присутствии кислот.
В ы в о д ы по главе 2.2
Кислоты классифицируют:
по числу атомов водорода – на одноосновные,
двухосновные и т.д.;по наличию атома кислорода в составе
молекулы – на бескислородные и
кислородсодержащие;по силе – на сильные и слабые;
по устойчивости – на устойчивые и
неустойчивые.
Кислоты реагируют:
с активными металлами (стоящими в ряду
активности до Н),с основаниями,
с основными и амфотерными оксидами,
с солями более слабых кислот.
Кислоты обнаруживаются индикаторами в кислой
(«красной») области.
* В химических формулах
органических кислот атом водорода стоит в конце,
например CH3COOH – уксусная кислота.
** Реакция между кислотой и
основанием называется реакцией нейтрализации.
Продолжение следует
Совет 1: Как составить формулы оксидов
Оксиды – это трудные химические вещества, которые состоят из 2-х элементов. Одним из них является кислород. Оксиды в большинстве случаев бывают кислотными и основными. Как легко осознать из наименования, кислотные оксиды реагируют с основаниями, образуя соль, то есть, проявляя свойства кислоты. Как составлять формулы оксидов ?
Инструкция
1. Многие из оксидов способны реагировать с водой, образуя кислоту. Скажем:SO3 + H2O = H2SO4 (образуется серная кислота).SiO2 + 2KOH = K2SiO3 + H2O (нерастворимый в воде оксид кремния вступает в реакцию с гидроксидом калия.
2. Основные оксиды, наоборот, вступают в реакции с кислотами, также образуя соль и воду. Те же из них, которые растворимы в воде, реагируют с ней, образуя основание. Характерные примеры:ZnO + 2HCl = ZnCl2 + H2O (нерастворимый в воде оксид цинка реагирует с соляной кислотой).Na2O + H2O = 2NaOH
3. Следует запомнить, что валентность кислорода в оксиде неизменно равняется 2. Исходя из этого, при составлении формулы нужно лишь знать валентность второго элемента. Скажем: щелочные металлы первой группы – одновалентные. Следственно всеобщая формула оксидов будет выглядеть так: Эл2О. Т.е., Li2O, Na2O, K2O, Rb2O. (Эл – «Элемент»).
4. Щелочноземельные металлы 2-й группы – двухвалентные. Всеобщая формула оксидов – ЭлО. И выглядеть она будет: ВеО, MgO, СаО, SrO.
5. Амфотерные элементы третьей группы, соответственно, трехвалентные. Всеобщая формула оксидов – Эл2О3. Классический пример – теснее упоминавшийся оксид алюминия Al2O3.
6. Элементы четвертой группы проявляют либо огромнее кислотных свойств (углерод, кремний), либо огромнее основных (германий, олово, свинец). В любом случае, всеобщая формула – ЭлО2 (СО2, SiO2).
7. Всеобщая формула пятой группы – Эл2О5. Пример – высший оксид азота, N2O5, из которого получают азотную кислоту. Либо высший оксид ванадия, V2О5 (правда ванадий – металл, его высший оксид проявляет кислотные свойства).
8. Соответственно, формула шестой группы, где находится сам кислород – ЭлО3. Высшие оксиды – SO3, СrO3, WO3. Обратите внимание, что хоть хром и вольфрам – металлы, их высшие оксиды по аналогии с оксидом ванадия также проявляют кислотные свойства.
9. Следует уточнить, что указывались лишь высшие оксиды элементов. Так, скажем, помимо оксида хрома CrО3, где хром шестивалентен, есть оксид Cr2O3, где данный элемент имеет валентность, равную 3. Помимо оксида азота N2O5, существуют оксиды N2O, NO, NO2. Сходственных примеров дюже много. Следственно, при написании формулы оксида, проверяйте, какую валентность имеет в этом соединении элемент, объединенный с кислородом!
Совет 2: Как составить формулу вещества
Вам нужно составить химическую формулу , но вы безусловно позабыли основы школьной химии? Поверьте, не стоит переживать. На сегодняшний день вестимо больше 20 миллионов химических соединений, и, поверьте, никто не держит их формулы у себя в голове. Довольно знать легкой правило их написания.
Вам понадобится
- периодическая таблица Менделеева, таблица растворимости солей
Инструкция
1. Задача составления химической формулы вещества сводится к созданию электронейтральной системы. Следственно вам нужно будет подобрать некоторое число электронов для всего элемента соединения так, дабы оно было уравновешено.Впрочем перед тем, как это сделать, вам следует припомнить некоторые теоретические основы. Всякий элемент периодической таблицы Менделеева владеет своей валентностью (степенью окисления), то есть способностью отдавать либо принять некоторое число электронов, с учетом своей валентности, не больше восьми электронов. Валентность всего химического элемента соответствует номеру группы в периодической таблице (верхняя строка, написанная римскими цифрами). Стоит подметить, что все элементы таблицы Менделеева дозволено условно поделить на два класса: окислители и восстановители. Первые, как водится, только забирают электроны, вторые – отдают.
2. Для составления химической формулы также нужно знать, с каким типом соединений вы имеете дело. Их дозволено поделить на следующие группы:1. Бинарные;2. Основания, соли, кислоты.
3. Для составления формулы бинарных соединений вам понадобится таблица Менделеева, а для остальных групп – таблица растворимости солей. В формулах бинарных соединений на первом месте принято писать металл либо элемент с меньшей валентностью, на втором – неметалл либо элемент с большей валентностью. Возможен, нужно составить формулу оксида тантала. Запишите рядом обозначения этих элементов и проставьте их валентность: Та5О6. Тантал, соответственно, горазд отдать 3 электрона, а кислород – принять два, то есть: Та3+О2-. Таким образом, для создания уравновешенной системы способом «крест-на-крест» (меняя индексы химических элементов местами и отбрасывая их знаки) вы получаете следующую формулу : Та2О3.
4. Для составления формул оснований, солей и кислот нужно воспользоваться таблицей растворимости солей. В верхней ее строке указаны катионы – вещества , отдающие электроны, а в левом столбце – анионы, то есть соединения, способные принимать электроны. Пользуясь таблицей растворимости солей, дозволено получить следующую формулу для сульфата алюминия: Al3+ SO42-. Применяя тезис «крест-на-крест», окончательная формула вещества будет иметь вид: Аl2(SO4)3.Как видите, алгорифм составления химических формул дюже примитивен. Он остается непоколебимым для всяких других соединений.
Совет 3: Что такое оксиды, гидроксиды и соли
Одними из основных в химии являются 2 представления: «примитивные вещества» и «трудные вещества». Первые образованы атомами одного химического элемента и подразделяются на неметаллы и металлы. Оксиды, гидроксиды, соли – это классы трудных веществ, либо химических соединений, состоящих из атомов различных химических элементов.
Оксиды
Это трудные химические вещества, бинарные по составу, потому что состоят из 2-х компонентов, один из которых кислород в степени окисления -2. Номенклатура строится из слова «оксид» и наименования элемента, тот, что входит в состав это вещества. По химическим свойствам могут быть солеобразующими и индифферентными (не образующими соли). К первым дозволено отнести кислотные (оксиды фосфора, серы, углерода), основные (кальция, меди) либо амфотерные (цинка, алюминия). Индифферентные оксиды не проявляют упомянутые выше свойства и ранее именовались равнодушными. Впрочем они тоже могут вступать в химические реакции. Среди таких оксидов, скажем, оксиды азота.Множество кислотных оксидов представлены газами, некоторые жидкостями, в их составе неметаллы. А вот основные почаще твердые вещества, кристаллической конструкции, состоят из кислорода и металла. Самый общеизвестный из оксидов – это вода.Химические свойства: вступают в реакции с кислотами, гидроксидами и водой.
Гидроксиды
К ним относят неорганические вещества, имеющие в составе –ОН (гидроксильную) группу. По систематизации схожи с оксидами и делятся в зависимости от химических свойств на кислотные, основные и амфотерные. Растворимые в воде гидроксиды называют щелочами, они имеют самый низкий рН и состоят из одновалентного металла и –ОН-группы. С увеличением числа гидрокси-групп и валентностью металла растворимость падает, а значение рН возрастает.По физическим свойствам гидроксиды твердые. Использование гидроксидам находят в производстве сообщи, аккумуляторов, мыла. К примеру, при применении КОН мыло будет жидким, а если взять NaOH, то твердым. Химические свойства: с кислотами образуют соли, с солями же реагируют только при летучести либо нерастворимости продукта.
Соли
Это также трудные соединения, в их состав включены атом металла и кислотный остаток. Образуются они реакциями нейтрализации (взаимодействие кислоты и основания с приобретение соли и воды). Если в молекуле кислоты один из ионов водорода замещен на металл, то соль считается кислой, а если это происходит с гидрокси-группой, то соль основная. По физическим свойствам они твердые кристаллические вещества.Самая вестимая соль – NaCl. Используется фактически повсюду в пищевой промышленности и является неотделимой частью рациона человека.Химические свойства: взаимодействуют с крепкими кислотами, со щелочами образуют нерастворимую соль либо основание, больше мощные металлы (в электрохимическом ряду) вытесняют из них слабый металл, при нерастворимости одного из продуктов соли реагируют с солями.
.
Порядок составления формул оксидов
Формулы
оксидов можно составлять по правилу креста:

Рис.1

формул первым ставят
элемент степень окисления. которого со знаком +, а
вторым элемент с отрицательной степенью окисления. Для оксидов это
всегда кислород.
Далее
необходимо:
1. расставить степени
окисления
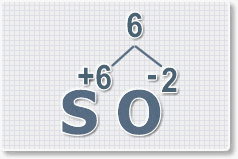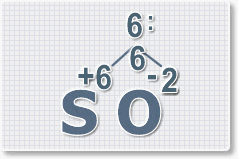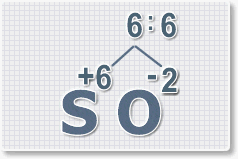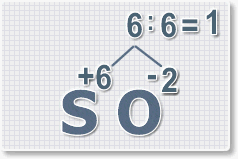
(с.о.) для каждого атома. Кислород в оксидах всегда имеет с.о. -2
(минус два).
2. Для того чтобы
правильно
определить степень окисления. второго элемента необходимо познакомится
с таблицей возможных степеней окисления некоторых элементов:
Таблица.1 Степени окисления некоторых элементов
|
Элемент |
Возможные степени окисления |
| N (азот) | -3, 0, +1, +2, +3, +4,+5. |
| P (фосфор) | -3, 0, +3, +5. |
| S (сера) | -2, 0, +4, +6. |
| C (углерод) | -4, 0, +2, +4. |
Степень окисления «0» —
ноль имеют:
1. Простые вещества: Н2,
Са, О2 …
2. Сложные в-ва (в сумме): Са+2О-2 (+2 – 2 =0)
Степень окисления со знаком +
характерна для элементов которые отдают свои электроны в соединениях
другим атомам или от которых оттянуты общие электронные пары, т.е.атомы
менее электроотрицательных элементов. например металлы
всегда имеют положительную степени окисления.
Подсказка: Узнать степени окисления для металлов
можно в таблице «растворимости…«.
В ней представлены заряды ионов металлов они обычно совпадают со
степенью окисления.
С неметаллами кислород образует оксид, если только этот неметалл менее
электроотрицательный, чем сам кислород см. таблицу
электроотрицательности.
рис.2

окисления.
элементов в бинарных соединениях равны по модулю, то индексы в формуле
не ставятся: Сa+2О-2.
Составим формулу
оксида натрия:
По
таблице растворимости заряд иона натрия +,
соответственно степень окисления натрия имеет значение +1 (Na+1),
с.о. кислорода в оксидах всегда -2.
Натрий
имеет положительный заряд, значит, его ставим первым, а вторым
ставим кислород и по правилу креста получим: Na2+1O-2
или Na2O.
Правило
наименьшего общего кратного
это способ наиболее универсальный для составления формул. Как им
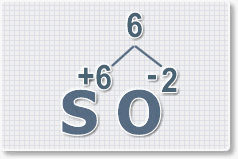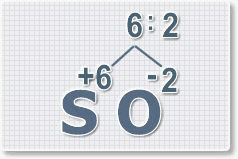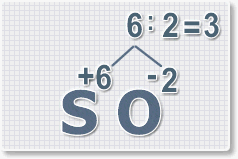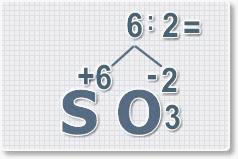
пользоваться рассмотрим на примере.
Составить формулу
оксида серы (VI).
1.
У кислорода с.о. -2 следовательно в формуле он ставиться вторым, а
первым элементом будет сера ее с.о. указана в названии оксида VI, т. е
+6. S+6O-2.
2.
Найдем наименьшее общее кратное. Для чисел 2 и 6 это будет 6.
3.
Находим индексы и расставляем для каждого элемента. См. рисунки ниже.
6 : 6 = 1 это индекс для серы.
Индексы со значением 1 в формулах не ставятся.
Рис.3
6 : 2 = 3
это индекс для кислорода
Рис.4
В результате получим
формулу оксида серы (VI):
* * *