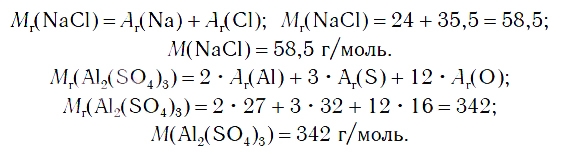В уроке 25 «Соли» из курса «Химия для чайников» узнаем, как правильно называть соли, их состав и научимся составлять химические формулы солей.
Как отмечалось в предыдущем уроке, в реакциях кислот с металлами выделяется простое вещество водород Н2. Кроме водорода, образуются и сложные вещества: ZnCl2, MgSO4 и др. Это представители класса широко распространенных в химии соединений — солей (рис. 102).
Здесь же мы рассмотрим состав солей, научимся составлять их формулы, узнаем, как называть соли.
Cостав солей
Сравним формулы кислот HCl и H2SO4 c формулами солей ZnCl2 и FeSO4. Мы видим, что в этих формулах одинаковые кислотные остатки Cl(I) и SO4(II). Но в молекулах кислот они соединены с атомами водорода Н, а в формульных единицах солей — с атомами цинка Zn и железа Fe. Значит, эти и другие соли можно рассматривать как продукты замещения атомов водорода в молекулах кислот на атомы металлов. Вещества, подобные ZnCl2 и FeSO4, относят к классу солей.
Соли — это сложные вещества, состоящие из атомов металлов и кислотных остатков.
В солях кислотные остатки соединяются с атомами металлов в соответствии с их валентностью. Для составления химической формулы соли необходимо знать валентность атома металла и валентность кислотного остатка. При этом пользуются тем же правилом, что и при составлении формул бинарных соединений. Для солей это правило следующее: сумма единиц валентности всех атомов металла должна быть равна сумме единиц валентности всех кислотных остатков.
Для примера составим формулу соли, в которую входят атомы кальция и кислотный остаток фосфорной кислоты PO4(III). Кальций проявляет постоянную валентность II, а валентность кислотного остатка PO4 равна III.
Названия солей
Соли образованы атомами разных металлов и различными кислотными остатками. Поэтому состав солей самый разнообразный. Давайте научимся давать им правильные названия.
Название соли состоит из названия кислотного остатка и названия металла в родительном падеже. Например, соль состава NaCl называют «хлорид натрия».
Если входящий в формульную единицу соли атом металла имеет переменную валентность, то она указывается римской цифрой в круглых скобках после его названия. Так, соль FeCl3 называют «хлорид железа(III)», а cоль FeCl2 — «хлорид железа(II)».
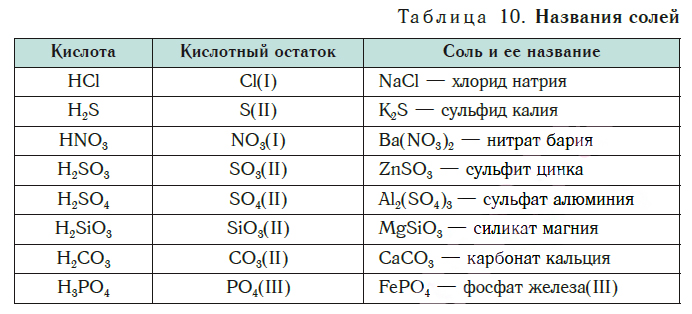
В таблице 10 приведены названия некоторых солей.
Соли — это вещества немолекулярного строения. Поэтому их состав выражают с помощью формульных единиц. В них отражено соотношение атомов металлов и кислотных остатков. Например, в формульной единице NaCl на один атом Na приходится один кислотный остаток Cl.
По химической формуле соли можно вычислить ее относительную формульную массу Mr, а также молярную массу M, например:
К солям относится не только поваренная соль (NaCl), но и мел, мрамор (СаСО3), сода (Na2CO3), марганцовка (KMnO4) и др.
Краткие выводы урока:
- Соли — сложные вещества, которые состоят из атомов металлов и кислотных остатков.
- Соли образуются при замещении атомов водорода в молекулах кислот на атомы металлов.
- Соли — вещества немолекулярного строения.
Надеюсь урок 25 «Соли» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Методическая
разработка:
«Алгоритм
составления названий и формул солей».
При изучении химии в 8
классе учащиеся сталкиваются с затруднениями в названии химических веществ и
составления формул химических соединений. Для лучшего усвоения данного
материала им помогут «Алгоритмы» — краткая запись последовательности действий.
При составлении
названий и формул солей необходимо знать состав и название кислот, и
соответственно название кислотных остатков, входящих в эти кислоты. Для
удобства, они указаны в данной разработке.
Названия
кислот и кислотных остатков этих кислот, образующих соли.
—
HCl соляная
кислота Cl хлорид
—
HF фтороводородная
кислота F фторид
—
HBr бромоводородная
кислота Br бромид
—
HI иодоводородная
кислота I иодид
2-
H2S
сероводородная кислота S сульфид
2-
H2SO3
сернистая кислота SO3
сульфит
2-
H2SO4
серная
кислота SO4
сульфат
—
HNO3
азотная кислота NO3 нитрат
—
HNO2
азотистая кислота NO2
нитрит
2-
H2CO3
угольная
кислота CO3
карбонат
2-
H2SiO3
кремниевая
кислота SiO3 силикат
3-
H3PO4
фосфорная кислота PO4
фосфат
АЛГОРИТМ
СОСТАВЛЕНИЯ НАЗВАНИЙ СОЛЕЙ.
Соли – сложные
химические соединения, состоящие из ионов металла, связанного с ионами
кислотного остатка.
При составлении
названия соли, совершаются поочередно следующие шаги:
1. Называется
кислотный остаток, который стоит в формуле соли в конце.
2. Называется
металл ( в родительном падеже). Он записан перед кислотным остатком.
3. Если
заряд металла переменный, в скобках указывается валентность металла.
ПРИМЕР:
CuSO4
сульфат меди (II) NaCl хлорид
натрия
АЛГОРИТМ
СОСТАВЛЕНИЯ ФОРМУЛ СОЛЕЙ.
1. Записываем
химические символы металла и кислотного остатка, образующих соль. Металл
записываем перед кислотным остатком.
2. Над
хим. элементами указываем заряды ионов металла и кислотного остатка.
3. Находим
Наименьшее Общее Кратное между зарядами ионов.
4. НОК
делим поочередно: на заряд металла и заряд кислотного остатка.
5. Ставим
полученные при расчете индексы справа, внизу возле химических элементов. Если
кислотных остатков несколько, заключаем его в скобки. Индекс ставиться за
скобками.
ПРИМЕР:
Нитрат железа (III)
1. Fe
NO3
2.
3+
_
Fe NO3
3.
3
3+
—
Fe NO3
4. 3
: 3 = 1 , 3 :1 = 3
5. Fe(NO3)3
Сульфат
алюминия
1. Al
SO4
2. 3+
2-
Al
SO4
3.
6
3+
2-
Al SO4
4. 6
:3 = 2 , 6 :2 = 3
5. Al2(SO4)3
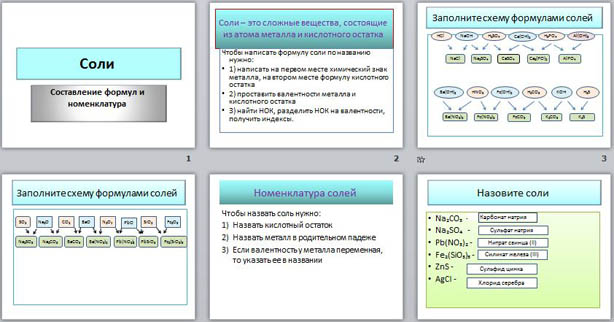
Презентация может быть использована на уроке химии в 8 классе по теме «Соли» для отработки навыков составления формул солей или первичного закрепления темы «Соли«, или для проверки умения составлять формулы и давать названия солям.
На первом слайде дается алгоритм составления формул солей.
На втором слайде в овальных фигурах записаны формулы кислот и оснований, используя которые ученик должен составить формулу соли. Правильность выполнения проверяется по клику мышки (в прямоугольнике под формулами кислот и оснований пояляется формула соли). Овалы закрашены в цвета лакмуса в кислой и щелочной средах соответственно, для повторения и визуального закрепеления.
На третьем слайде в прямоугольниках записаны формулы килотных и основных оксидов, используя которые ученик должен составить формулу соли. Правильность выполнения проверяется по клику мышки (в прямоугольнике под формулами оксидов пояляется формула соли). Овалы закрашены в цвета лакмуса в кислой и щелочной средах соответственно, для повторения и визуального закрепеления. Задания расположены в порядке усложнения.
На четвертом слайде дан алгоритм составления названий солей.
На пятом слайде даны формулы солей, которые ученик должен назвать. Правильность названия проверяется по клику мышки (в прямоугольнике справа появляется название соли).
Соли – это сложные вещества, состоящие из атома металла и кислотного остатка.
Чтобы написать формулу соли по названию нужно:
1) написать на первом месте химический знак металла, на втором месте формулу кислотного остатка
2) проставить валентности металла и кислотного остатка
3) найти НОК, разделить НОК на валентности, получить индексы.
Правила
составления формул основных солей по
названию.
Пример
1.
1)
Прочитайте название вещества и напишите
составные части символами элементов:
-
Название
вещества:
Выполненное
действие:
Пояснения:
гидроксохлорид
железа
(III)FeOHCl
Приставка
ГИДРОКСО означает, что соль основная,поэтому,
в составе — одна ОН группаНазвание
ХЛОРИД означает, что это соль солянойкислоты,
поэтому, в составе кислотного остатка
Cl
2)
Проставьте заряды частиц, входящих в
состав формулы. Заряд металла положителен
и равен численно валентности металла.
Заряд ОН группы равен ( — 1 ). Заряд
кислотного остатка отрицателен и чсленно
равен валентности кислотного остатка:
-
Название
вещества:
Выполненное
действие:
Пояснения:
гидроксохлорид
железа
(III)+3
-1 -1FeOHCl
Валентность
железа равна III ( указано в названии
),поэтому,
заряд атома железа равен ( + 3 )Валентность
кислотного остатка Cl
равна
I , т.к. в НCl один атом водорода, поэтому,
заряд хлора равен ( — 1 )Заряд
ОН группы всегда равен ( -1 )
3)
Формула основной соли делится на две
части: первая часть — металл с ОН группой;
вторая часть — кислотный остаток.
Посчитайте суммы зарядов в составных
частях.
-
П
ервая
часть: металл и ОН группа+3
-1(
FeOH )Заряд
первой части равен:+3
+ (-1) = +2+3
-1 -1FeOHCl
+2
-1Вторая
часть: кислотный остаток(
Cl )Заряд
второй части равен: -1
4)
Используя принцип электронейтральности
молекулы вещества ( сумма зарядов
составных частей равна нулю ), проставьте
в формулу индексы.
-
П
ервая
часть: металл и ОН группа(
FeOH )Заряд
первой части равен:+3
+ (-1) = +2У
группы FeOH индекс1
не пишем+3
-1 -1FeOHCl2
+2
+ (-2) = 0Вторая
часть: кислотный остаток ( Cl )Для
равенства зарядов у кислотногоостатка
Cl пишем индекс: 2Заряд
второй части равен:-1
•
2 = — 2
¾
12 ¾
Пример
2.
1)
Прочитайте название вещества и напишите
составные части символами элементов:
-
Название
вещества:
Выполненное
действие:
Пояснения:
дигидроксохлорид
железа
(III)Fe(OH)2Cl
Приставка
ДИГИДРОКСО означает, что соль
основная,и
в её составе — две ОН группы“ДИ”
означает ДВЕ ( две ОН группы )Название
ХЛОРИД означает, что это соль солянойкислоты,
поэтому, в составе кислотного остатка
группа Cl
2)
Проставьте заряды частиц, входящих в
состав формулы. Заряд металла положителен
и равен численно валентности металла.
Заряд ОН группы равен ( — 1 ). Заряд
кислотного остатка отрицателен и чсленно
равен валентности кислотного остатка:
-
Название
вещества:
Выполненное
действие:
Пояснения:
дигидроксохлорид
железа
(III)+3
-1 -1Fe(OH)2Cl
Валентность
железа равна III ( указано в названии
),поэтому,
заряд атома железа равен ( + 3 )Валентность
кислотного остатка Cl
равна
I , т.к. в НCl один атом водорода, поэтому,
заряд хлора равен ( — 1 )Заряд
ОН группы всегда равен ( -1 )
3)
Формула основной соли делится на две
части: первая часть — металл с ОН группой;
вторая часть — кислотный остаток.
Посчитайте суммы зарядов в составных
частях.
-
П
ервая
часть: металл и ОН группы+3
-1(
Fe(OH)2
)Заряд
первой части равен:+3
+ ( -1 •
2
) = +1+3
-1 -1Fe(OH)2Cl
+1
-1Вторая
часть: кислотный остаток(
Cl )Заряд
второй части равен: -1
4)
Используя принцип электронейтральности
молекулы вещества ( сумма зарядов
составных частей равна нулю ), проставьте
в формулу индексы.
-
П
ервая
часть: металл и ОН группа+3
-1(
Fe(OH)2
)Заряд
первой части равен:+3
+ ( -1 •
2
) = +1+3
-1 -1Fe(OH)2Cl
+1
+ ( -1 ) = 0Вторая
часть: кислотный остаток ( Cl )Заряд
второй части равен:-1
•
1 = — 1Заряды
частей равны, поэтому, индексы ставить
не надо, т.к. формула составлена.
¾
13 ¾
Пример
3.
1)
Прочитайте название вещества и напишите
составные части символами элементов:
-
Название
вещества:
Выполненное
действие:
Пояснения:
гидроксокарбонат
меди
(II)СuOHCO3
Приставка
ГИДРОКСО означает, что соль основная,поэтому,
в составе — одна ОН группаНазвание
КАРБОНАТ означает, что это соль
угольнойкислоты,
поэтому, в составе кислотного остатка
группа CО3
2)
Проставьте заряды частиц, входящих в
состав формулы. Заряд металла положителен
и равен численно валентности металла.
Заряд ОН группы равен ( — 1 ). Заряд
кислотного остатка отрицателен и чсленно
равен валентности кислотного остатка:
-
Название
вещества:
Выполненное
действие:
Пояснения:
гидроксокарбонат
меди
(II)+2
-1 -2СuOHCO3
Валентность
меди равна II ( указано в названии ),поэтому,
заряд атома меди равен ( + 2 )Валентность
кислотного остатка CО3
равна
II , т.к.в
Н2CО3
два атома водорода, поэтому, заряд
CО3равен
( — 2 )Заряд
ОН группы всегда равен ( -1 )
3)
Формула основной соли делится на две
части: первая часть — металл с ОН группой;
вторая часть — кислотный остаток.
Посчитайте суммы зарядов в составных
частях.
-
П
ервая
часть: металл и ОН группа+2
-1(
СuOH )Заряд
первой части равен:+2
+ (-1) = +1+2
-1 -2CuOHCO3
+1
-2Вторая
часть: кислотный остаток(
CO3
)Заряд
второй части равен: -2
4)
Используя принцип электронейтральности
молекулы вещества ( сумма зарядов
составных частей равна нулю ), проставьте
в формулу индексы.
-
П
ервая
часть: металл и ОН группа(
CuOH )Заряд
первой части равен:+2
+ (-1) = +1У
группы CuOH запишите индекс 2+2
-1 -2(СuOH)2CO3
+1
+ (-2) = -1Вторая
часть: кислотный остаток ( Cl )Заряд
второй части равен:-1
•
2 = — 2У
кислотного остатка CO3индекс
1 не пишем
¾
14 ¾
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Слайд 1
Вещества Простые Сложные Металлы Неметаллы Оксиды Основание ? кислоты
Слайд 2
2 3 К какому классу соединений относятся вещества, дать им названия
Слайд 3
Задание1 На какие группы и по каким признакам можно разделить вещества , формулы которых приведены ниже ? Na 2 O ; H 2 CO 3 ; ; H 2 SiO 3 Ca (NO 3 ) 2 Ca CO 3 Na Cl Cr 2 S 3 Na OH ; О 2 ; Al 2 O 3 ; Ca (OH) 2 ; С Са O ; А l; N 2 ; Al (OH) 3 ; S ; С О 2 ; H 2 SO 3 ; SO 2 ; Ca; Na формулы запишите в схему:
Слайд 4
Вещества Простые Сложные Металлы А l , Ca , Na Неметаллы S , С , N 2 , , О 2 Оксиды Na 2 O , Al 2 O 3 , Са O , СО 2 , SO 2 Основание Ca (OH) 2 , NaOH , Al(OH) 3 Ca ( NO 3 ) 2 Ca CO 3 Na Cl Cr 2 S 3 ? кислоты H 2 CO 3 ; , H 2 SiO 3 , H 2 SO 3
Слайд 5
Задание 2 Вставьте пропущенный фрагмент. S —— S О 2 —— H 2 SO 3 Na —-Х—— Na ОН С ——- Х —- H 2 CO 3 Ca —— Ca O —— Ca (OH) 2 Х ХХ Ca CO 3
Слайд 6
проверка S —— S О 2 —— H 2 SO 3 Na —- Na 2 O —— Na ОН ? ? ? С ——- С О 2 —- H 2 CO 3 Ca —— Ca O —— Ca (OH) 2 Na 2 SO 3 Ca CO 3
Слайд 9
Цель урока: Изучить состав, названия солей, классификацию, свойства и применение. План 1.Соли. Их состав и номенклатура ( название). 2. Составление формул солей по их названиям. 3. Классификация. 4. Представители данного класса. 5. Проверка знаний. 6. Подведение итогов урока. 7. Домашнее задание.
Слайд 10
1. Соли. Их состав и номенклатура (название).
Слайд 11
СОЛИ Na OH H Cl + — + _
Слайд 12
Соли — это сложные вещества, которые состоят из ионов металла и кислотного остатка
Слайд 13
3 задание. Определить : почему у солей разное количество кислотных остатков Дайте обоснованный ответ. NaNO 3 Ca (NO 3 ) 2 Al (NO 3 ) 3
Слайд 14
3 задание. Na +1 Ca +2 Al +3 Имеют разную степень окисления. (см. таблицу растворимости)
Слайд 15
задание 4 . Определить : почему у солей разное количество ионов металла? Дайте обоснованный ответ. Na NO 3 Na 2 С O 3 Na 3 Р — O 4
Слайд 16
Так как кислотные остатки имеют свою степень окисления: (см. таблицу растворимости) NO 2 -1 — нитрит NO 3 -1 — нитрат SO 3 -2 — сульфит SO 4 -2 — сульфат С O 3 -2 — карбонат Р — O 4 -3 — фосфат Cl -1 — хлорид SiO 3 -2 -силикат
Слайд 17
Выведем общую формулу солей ? Ме + n (К. О. — m ) n
Слайд 18
Алгоритм названия солей Название Соли Название кислотного остатка Название металла в родительном падеже Кислотные остатки NO 2 -1 — нитрит NO 3 -1 — нитрат SO 3 -2 — сульфит SO 4 -2 — сульфат С O 3 -2 — карбонат Р — O 4 -3 — фосфат Cl -1 — жлорид SiO 3 -2 -силикат Стр. 76 таблица С.О. римскими цифрами + + = 8
Слайд 19
Алгоритм названия солей Fe +2 ( NO 3 -1 ) 2 – нитрат железа ( II ) Fe +3 ( NO 3 -1 ) 3 – нитрат железа ( III ) Название металла в родительном падеже С.О. римскими цифрами Название Соли Название кислотного остатка = + + Назовите соль: Zn SO 4 -2 Al Cl 3 Cu ( NO 3 -1 ) 2
Слайд 20
задание 5 . НАЗОВИТЕ СОЛИ Na Cl Fe +2 SO 4 Al 3 ( PO 4 ) 3 Ca (NO 3 ) 2 Cu +2 CO 3 Cr 2 +3 S 3 Na 2 SO 4 Ba (NO 3 ) 2
Слайд 21
задание 5 . НАЗОВИТЕ СОЛИ Na Cl — хлорид натрия Fe +2 SO 4 — сульфат железа ( II ) Al 3 ( PO 4 ) 3 – фосфат алюминия Ca (NO 3 ) 2 — нитрат кальция Cu +2 CO 3 – карбонат меди ( II ) Cr 2 +3 S 3 – сульфид хрома ( III ) Na 2 SO 4 – сульфат натрия Ba (NO 3 ) 2 — нитрат бария
Слайд 22
Контрольное задание1 Установите соответствие между формулой вещества и его названием ФОРМУЛА ВЕЩЕСТВА НАЗВАНИЕ ВЕЩЕСТВА 1 Na 2 SO 4 А Сульфид меди ( I) 2 Cu 2 S Б Сульфид меди ( II ) 3 Cu S В Сульфат натрия 1 2 3 В А Б
Слайд 23
2. Составление формул солей по их названиям.
Слайд 24
1. Запиши рядом знаки химических элементов, которые входят в состав вещества. Алгоритм составления формул солей : Составить химическую формулу сульфата железа ( III ) (первый способ) Fe SO 4 Соли — это сложные вещества, которые состоят из ионов металла и кислотного остатка Первый пункт выполнили переходим ко второму
Слайд 25
2 . Над знаками химических элементов поставь их степень окисления. Пример: Fe SO 4 +3 -2 Второй пункт выполнили переходим к третьему
Слайд 26
7 42 35 28 21 14 7 7 42 6 30 12 6 6 6 6 35 30 5 20 15 10 5 5 28 24 20 4 12 4 4 4 21 6 15 12 3 6 3 3 14 6 10 4 6 2 2 2 7 6 5 4 3 2 1 1 7 6 5 4 3 2 1 Таблица для определения Н.О.К. 3 . Определи Н.О.К. чисел выражающих степень окисления этих элементов. Запиши Н.О.К. в квадратике над формулой. Пример: Составить химическую формулу сульфата железа ( III ). Fe SO 4 +3 -2 6 Третий пункт выполнили переходим ко четвертому Н.О.К. (наименьшее общее кратное) – это число, которое делится на исходные числа без остатка.
Слайд 27
4. Раздели Н.О.К. на степень окисления каждого элемента. Запиши полученный индекс. Пример: Составить химическую формулу сульфата железа ( III ).. Fe ( SO 4 ) +3 -2 2 3 6 2 3 Формула составлена 6 6 3 2 : : = =
Слайд 28
Составить формулу сульфата алюминия: (второй способ) Составьте формулы: Упр. 3 стр. 78 Al 2 + SO 4 3 9 3 2
Слайд 29
Составьте формулу хлорида кальция Са Cl 2 Составьте формулу нитрата натрия Na NO 3 Zn( SO 4 ) 2 Cu NO 3 Составьте формулу сульфата цинка Составьте формулу хлорида свинца ( II ) Составьте формулу нитрата меди ( I ) Pb Cl 2 Контрольное задание 2
Слайд 30
3. Отдельные Представители стр.77 в таблицу 2 хлорид натрия название формула Нахождение в природе Значение и применение хлорид натрия
Слайд 31
NaCl
Слайд 32
«Среди всех природных минеральных солей, самая главная та, которую мы называем просто “соль” А.Е.Ферсман
Слайд 33
За 4 года человек съедает пуд соли (в год человек с пищей потребляет 3-5,5 кг соли)
Слайд 34
Соль в геральдике российских городов Герб Бахмута Герб Солигалича Герб Сольвычегодска Герб Энгельса Герб Усолья-Сибирского Герб Дрогобыча
Слайд 35
Добыча соли из соляных шахт из соленых озер
Слайд 36
На озере Баскунчак ежегодно добывается около 5 млн. тонн соли
Слайд 37
Применение NaCl
Слайд 38
Д/З: CaCO 3
Слайд 39
Моллюски, раки, радиолярии, кораллы – все имеют известковый скелет
Слайд 40
Большой Барьерный риф в Австралии
Слайд 41
Меловые горы
Слайд 42
Минералы карбоната кальция находятся в горных породах: Известняк Мел Мрамор Мрамор Мрамор Мрамор Травертин
Слайд 43
Мрамор – строительный материал Единственное в России здание, полностью построенное из нешлифованного мрамора — железнодорожный вокзал в городе Слюдянка Иркутской области
Слайд 44
Д/З: Фосфат кальция — основа минералов фосфоритов и апатитов
Слайд 45
3.КЛАССИФИКАЦИЯ: а)по растворимости СОЛИ
Слайд 46
Лабораторный опыт. №1 Определите растворимость солей Для этого: -прибавьте в первую пробирку к хлориду натрия 5-10 мл воды ; прибавьте во вторую пробирку к карбонату кальция 5-10 мл воды Что произошло? Вывод:
Слайд 47
3.КЛАССИФИКАЦИЯ: а)по растворимости NaCl CaCO 3 таблица растворимости СОЛИ Растворимые Нерастворимые
Слайд 48
а)по составу СОЛИ ? ? ?
Слайд 49
Лабораторный опыт. №2 Определите в какой из трех пробирок находятся кислота, в какой щелочь, в какой соль, хлорид натрия. прибавьте в пробирку №1 универсальный лакмус прибавьте в пробирку №2 универсальный лакмус прибавьте в пробирку №3 универсальный лакмус Что произошло? Результаты опыта оформите в таблицу:
Слайд 50
Изменение окраски индикатора Для кислот, также как и для щелочей, существуют качественные реакции с помощью которых растворы кислот можно распознать среди растворов других веществ. Это реакции с индикаторами. Название индикатора Окраска индикатора универсального лакмуса В кислой среде ( H +1 ) В нейтральной среде ( H +1 = О H -1 ) В щелочной среде (О H -1 )
Слайд 51
Что сделали Что наблюдали Вывод Контрольное задание3 Ответте на вопросы: 1.Какая окраска индикатора в растворе хлорида натрия. Почему? 2.Раствор хлорида натрия. является : кислым, щелочным или нейтральным? 3. Следовательно соль хлорид натрия какая?
Слайд 52
а)по составу NaCl Ba(NO 3 ) 2 СОЛИ средние Кислые ? Основные ?
Слайд 53
Подведем итоги?
Слайд 54
Контрольное задание — итоговое Часть А (задания с выбором ответа) 1. Соли – это сложные вещества: А) состоящие из ионов металлов и связанных с ними одного или нескольких гидроксид- ионов. Б) состоящие из ионов металлов и кислотных остатков; В) состоящие из двух химических элементов, один из которых – кислород со степенью окисления -2; Г) молекулы, которых состоят из ионов водорода и кислотных остатков. 2. Хлорид железа ( III ) имеет формулу: А) FeCl 3 ; B ) Fe 2 O 3 ; Б) FeCl 2 ; Г) FeO .
Слайд 55
Контрольное задание — итоговое Часть В Выбери лишнее вещество и объясни почему? Игра « Третий лишний» 1. Ba SO 4 ; Ca CO 3 ; NaCl . 2. NaCl, Na 2 SO 4 , NaOH 3 Al 2 (SO 4 ) 3 , H 2 SO 4 , CaSO 4 4. Cu(NO 3 ) 2 , CuO, CuCl 2 5. CaCl 2 , PbS, Ba SO 4 .
Слайд 56
Контрольное задание — итоговое Часть А Г А Часть В объясни почему? 1. NaCl . т.к… 2. NaOH т.к… 3 H 2 SO 4 , т.к… 4. CuO, т.к… 5. CaCl 2 т.к…
Слайд 57
Домашнее задание §,21 упр.3 стр. 78 Составить презентацию фосфата кальция или опорный конспект в форме таблицы
Слайд 58
Рефлексия 1. Сегодня я узнал… 2. Было интересно… 3. Было трудно… 4. Я выполнял задания… 5. Я понял, что… 6. Теперь я могу… 7. Я почувствовал, что… 8. Я приобрёл… 9. Я научился… 10. У меня получилось… 11. Я смог… 12. Попробую… 13. Меня удивило… 14.Урок мне дал для жизни… 15. Мне захотелось…