Многоатомные спирты (полиспирты, полиолы) – органические соединения, в молекулах которых содержится несколько гидроксильных групп (-ОН), соединённых с углеводородным радикалом.
Многоатомные спирты — соединения, у которых две или несколько гидроксильных групп расположены у соседних атомов углерода.
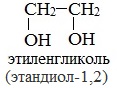
Важнейшими представителями многоатомных спиртов являются двухатомный спирт этандиол-1,2 (этиленгликоль), и трехатомный спирт пропантриол-1,2,3 (глицерин):
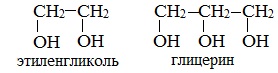
Существуют многоатомные спирты, содержащие и большее количество групп -ОН в молекуле, например, пятиатомный спирт ксилит, который используют в качестве заменителя сахара:
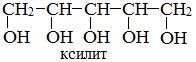
или шестиатомный спирт гексанол (сорбит):
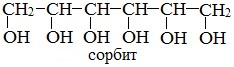
Двухатомные спирты, содержащие две гидроксильные группы -ОН, называются гликолями, или диолами, трехатомные спирты, содержащие три гидроксильные группы, — глицеринами, или триолами.
I. Гликоли (диолы)
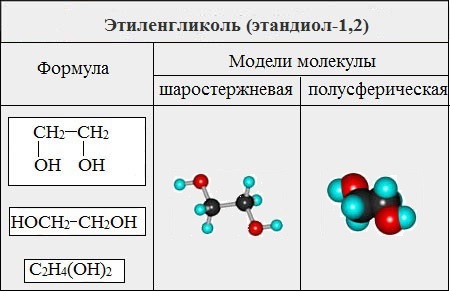
Этиленгликоль С2Н4(ОН)2 — представитель предельных двухатомных спиртов — гликолей.
Общая формула ряда гликолей СnН2n(ОН)2.
Название гликоли получили вследствие сладкого вкуса многих представителей ряда (греч. «гликос» — сладкий).
II. Глицерины (триолы)
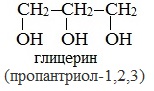
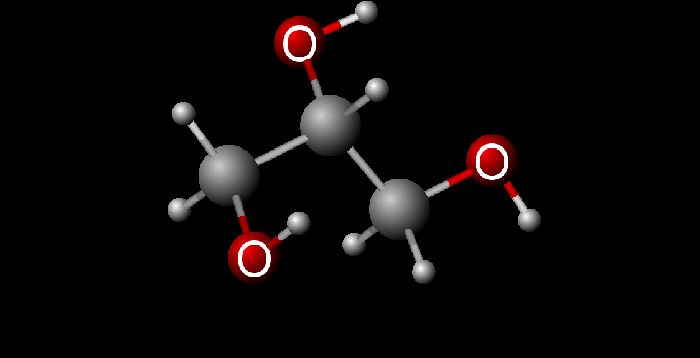
Глицерин (С3Н5ОН)3 — простейший представитель трехатомных предельных спиртов — глицеринов.
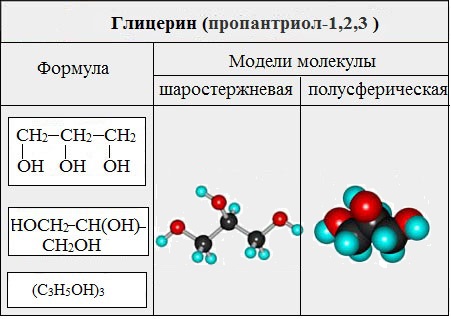
Номенклатура
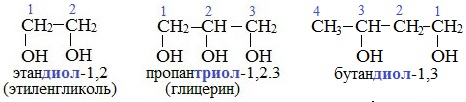
В названиях многоатомных спиртов (полиолов) положение и число гидроксильных групп указывают соответствующими цифрами и суффиксами —диол (две ОН-группы), -триол (три ОН-группы) и т.д. Например:
Физические свойства
Этиленгликоль — сиропообразная, вязкая бесцветная жидкость, tпл = 11,50C, tкип = 197,60C. Этиленгликоль гигроскопичен, смешивается с водой и этиловым спиртом в любых отношениях. Он сильно понижает температуру замерзания воды, поскольку раствор этиленгликоля в воде имеет низкую температуру замерзания (60%-ый раствор замерзает при -490С).
Поэтому этиленгликоль широко используется в системах охлаждения двигателей в качестве антифриза (от анг. to freeze — «замерзать») – вещества с низкой температурой замерзания, заменяющего воду в радиаторах автомобильных и авиационных моторов в зимнее время. Антифризы также замедляют ее испарение летом.
Этиленгликоль используется также для производства синтетического волокна полиэфирного волокна – лавсана.
Этиленгликоль очень токсичен! Это сильный яд! Этиленгликоль вызывает длительное угрожающее жизни угнетение центральной нервной системы и поражение почек. Продуктами его превращения в организме являются щавелевая кислота и другие не менее ядовитые соединения. Он имеет спиртовой запах, в связи, с чем может быть принят за этиловый спирт и стать причиной тяжелых отравлений.

Видеоопыт «Изучение физических свойств глицерина»
Глицерин – бесцветная, вязкая, сиропообразная жидкость, сладкая на вкус. Не ядовит. Глицерин не имеет запаха, его tпл = 180С, tкип = 2900С. Глицерин гигроскопичен, хорошо смешивается с водой и этанолом. На этом свойстве основано применение глицерина в косметической промышленности, где глицерин используется для увлажнения кожи.

Абсолютно чистый безводный глицерин затвердевает при +180С, но получить его в твердом виде чрезвычайно сложно.
Глицерин широко распространен в живой природе. Он играет важную роль в процессах обмена в организмах животных, входит в состав большинства липидов – жиров и других веществ, содержащихся в животных и растительных тканях и выполняющих в живых организмах важнейшие функции. Благодаря этим свойствам глицерин является важным компонентов многих пищевых продуктов, кремов, косметических средств.
Этиленгликоль и глицерин, благодаря наличию гидроксильных групп, могут образовывать водородные связи с молекулами воды, этим объясняется их не ограниченная растворимость в воде.
Спирты
Химические свойства многоатомных спиртов
Получение многоатомных спиртов
Применение многоатомных спиртов
Многоатомные спирты

4.3
Средняя оценка: 4.3
Всего получено оценок: 724.
4.3
Средняя оценка: 4.3
Всего получено оценок: 724.
Органические углеводороды, в молекулярной структуре которых находится две и более группы -ОН, называются многоатомными спиртами. По-другому соединения называются полиспиртами или полиолами.
Представители
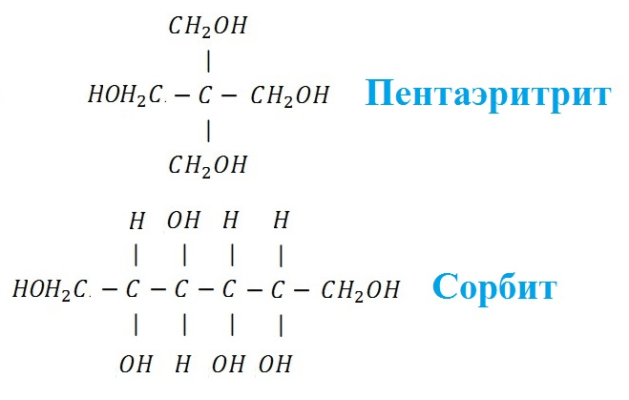
В зависимости от строения выделяют двухатомные, трёхатомные, четырёхатомные и т.д. спирты. Они отличаются на одну гидроксильную группу -ОН. Общую формулу многоатомных спиртов можно записать как CnH2n+2(OH)n. Однако количество атомов углерода не всегда соответствует количеству гидроксильных групп. Такое несоответствие объясняется разной структурой углеродного скелета. Например, пентаэритрит содержит пять атомов углерода и четыре группы -ОН (один углерод посередине), а сорбит – по шесть атомов углерода и групп -ОН.
В таблице описаны наиболее известные представители полиолов.
|
Вид спирта |
Название |
Формула |
Физические свойства |
|
Двухатомные (диолы) |
Этиленгликоль |
HO-CH2-CH2-OH |
Прозрачная маслянистая сильно токсичная жидкость без запаха, со сладким привкусом |
|
Трёхатомные (триолы) |
Глицерин |
C3H5(OH)3 |
Вязкая прозрачная жидкость. Смешивается с водой в любых пропорциях. Имеет сладкий вкус |
|
Четырёхатомные |
Пентаэритрит |
C(CH2OH)4 |
Кристаллический белый порошок со сладким вкусом. Растворяется в воде и органических растворителях |
|
Пятиатомные |
Ксилит |
CH2OH(CHOH)3CH2OH |
Кристаллическое бесцветное вещество сладкое на вкус. Хорошо растворяется в воде, спиртах, органических кислотах |
|
Шестиатомные |
Сорбит (глюцит) |
C6H8(HO)6 |
Сладкое кристаллическое вещество, хорошо растворимое в воде, но плохо растворимое в этаноле |
Некоторые кристаллические многоатомные спирты, например, ксилит, сорбит, используют в качестве сахарозаменителя и пищевой добавки.
Получение
Полиолы получают лабораторным и промышленным путём:
- гидратацией оксида этилена (получение этиленгликоля):
С2Н4О + Н2О → HO-CH2-CH2-OH;
- взаимодействием галогеналканов с раствором щелочей:
R-CHCl-CH2Cl + 2NaOH → R-CHOH-CH2OH + 2NaCl;
- окислением алкенов:
R-CH=CH2 + H2O + KMnO4 → R-CHOH-CH2OH + MnO2 + KOH;
- омылением жиров (получение глицерина):
C3H5(COO)3-R + 3NaOH → C3H5(OH)3 + 3R-COONa
Свойства
Химические свойства многоатомных спиртов обусловлены нахождением в молекуле нескольких гидроксильных групп. Их близкое положение способствует более лёгким разрывам водородных связей, чем у одноатомных спиртов. Многоатомные спирты проявляют кислотные и основные свойства.
Основные химические свойства описаны в таблице.
|
Реакция |
Описание |
Уравнение |
|
Со щелочными металлами |
Замещая атом водорода в группе -ОН атомом металла, образуют соли с активными металлами и их щелочами |
|
|
С галогеноводородами |
Одна из групп -ОН замещается на галоген |
HO-CH2-CH2-OH + HCl → Cl-CH2-CH2-OH (этиленхлоргидрин) + H2O |
|
Этерификация |
Реагируют с органическими и минеральными кислотами с образованием жиров – сложных эфиров |
C3H8O3 + 3HNO3 → C3H5O3(NO2)3 (нитроглицерин) + 3H2O |
|
Качественная реакция |
При взаимодействии с гидроксидом меди (II) в щелочной среде образуется тёмно-синий раствор |
HO-CH2-CH2-OH + Cu(OH)2 → C4H10O4 + 2H2O |
Соли двухатомных спиртов называются гликолятами, трёхатомных – глицератами.
Что мы узнали?
Из урока химии узнали, что такое многоатомные спирты или полиолы. Это углеводороды, содержащие несколько гидроксильных групп. В зависимости от количества -ОН различают двухатомные, трёхатомные, четырёхатомные, пятиатомные и т.д. спирты. Наиболее простой двухатомный спирт – этиленгликоль. Полиолы обладают сладким вкусом и хорошо растворяются в воде. Диолы и триолы – вязкие жидкости. Высшие спирты – кристаллические вещества.
Тест по теме
Доска почёта

Чтобы попасть сюда — пройдите тест.
-
Azillo Saipov
4/5
Оценка доклада
4.3
Средняя оценка: 4.3
Всего получено оценок: 724.
А какая ваша оценка?
Гидроксисоединения – это органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Гидроксисоединения делят на спирты и фенолы.
Строение, изомерия и гомологический ряд спиртов
Химические свойства спиртов
Способы получения спиртов
Если гидроксогруппа ОН соединена с бензольным кольцом, то вещество относится к фенолам.
Общая формула предельных нециклических спиртов: CnH2n+2Om, где m ≤ n.
Классификация спиртов
По числу гидроксильных групп:
- одноатомные спирты — содержат одну группу -ОН. Общая формула CnH2n+1OH или CnH2n+2O.
- двухатомные — содержат две группы ОН. Общая формула CnH2n(OH)2 или CnH2n+2O2.
- трехатомные спирты — содержат три группы ОН. Общая формула CnH2n-1(OH)3 или CnH2n+2O3.
Двухатомные спирты с двумя и тремя гидроксогруппами у одного атома углерода R‒CH(OH)2 или R-C(OH)3 неустойчивы, от них легко отрывается вода и образуется карбонильное соединение.
Классификация по числу углеводородных радикалов у атома углерода при гидроксильной группе
- Первичные спирты – группа ОН соединена с первичным атомом углерода. Например, этанол СН3–СН2–ОН.
- Вторичные спирты – группа ОН соединена с вторичным атомом углерода. Например, пропанол-2: СН3–СН(СН3)–ОН.
- Третичные спирты – группа ОН соединена с третичным атомом углерода. Например, 2-метилпропанол-2: (СН3)3С–ОН.
- Метанол не относится ни к первичным, ни к вторичным, ни к третичным спиртам.
Классификация по строению углеводородного радикала
- Предельные спирты – группа ОН соединена с предельным радикалом. Например, пропанол-1: СН3–СН2–СН2–ОН.
- Непредельные спирты – группа ОН соединена с непредельным радикалом. Например, алкенолы: СН2=СН–СН2–ОН.
Непредельные спирты, в которых гидроксильная группа соединена с атомом углерода при двойной связи (алкенолы), неустойчивы и изомеризуются в соответствующие карбонильные соединения.
- Ароматические спирты – содержат в радикале ароматическое кольцо, не связанное непосредственно с группой ОН. Например, бензиловый спирт.
Строение спиртов и фенолов
В молекулах спиртов, помимо связей С–С и С–Н, присутствуют ковалентные полярные химические связи О–Н и С–О.
Электроотрицательность кислорода (ЭО = 3,5) больше электроотрицательности водорода (ЭО = 2,1) и углерода (ЭО = 2,4).
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:
Атом кислорода в спиртах находится в состоянии sp3-гибридизации.
В образовании химических связей с атомами C и H участвуют две 2sp3-гибридные орбитали, а еще две 2sp3-гибридные орбитали заняты неподеленными электронными парами атома кислорода.
Поэтому валентный угол C–О–H близок к тетраэдрическому и составляет почти 108о.
Водородные связи и физические свойства спиртов
Спирты образуют межмолекулярные водородные связи. Водородные связи вызывают притяжение и ассоциацию молекул спиртов:
Поэтому спирты – жидкости с относительно высокой температурой кипения (температура кипения метанола +64,5оС). Температуры кипения многоатомных спиртов и фенолов значительно выше.
Таблица. Температуры кипения некоторых спиртов и фенола.
| Название вещества | Температура кипения |
| Метанол | 64 |
| Этанол | 78 |
| Пропанол-1 | 92 |
| Бутанол-1 | 118 |
| Этиленгликоль | 196 |
| Фенол | 181,8 |
Водородные связи образуются не только между молекулами спиртов, но и между молекулами спиртов и воды. Поэтому спирты очень хорошо растворимы в воде. Молекулы спиртов в воде гидратируются:
Чем больше углеводородный радикал, тем меньше растворимость спирта в воде. Чем больше ОН-групп в спирте, тем больше растворимость в воде.
Низшие спирты (метанол, этанол, пропанол, изопропанол, этиленгликоль и глицерин) смешиваются с водой в любых соотношениях.
Номенклатура спиртов
- По систематической номенклатуре к названию углеводорода добавляют суффикс «-ОЛ» и цифру, указывающую номер атома углерода, к которому присоединена гидроксильная группа.
Нумерация ведется от ближайшего к ОН-группе конца цепи.
- По радикально-функциональной номенклатуре названия спиртов составляют от названий углеводородных радикалов, соединенных с группой ОН, с добавлением слова «спирт».
Например: СН3ОН – метиловый спирт, С2Н5ОН – этиловый спирт и т.д.
- В названиях многоатомных спиртов количество групп ОН указывают суффиксами -диол в при наличии двух ОН-групп, -триол при наличии трех ОН-групп и т.д. После этого добавляют номера атомов углерода, связанных с гидроксильными группами.
Например, пропандиол-1,2 (пропиленгликоль):
Изомерия спиртов
Структурная изомерия
Для спиртов характерна структурная изомерия – изомерия углеродного скелета, изомерия положения гидроксильной группы и межклассовая изомерия.
Структурные изомеры — это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры углеродного скелета характерна для спиртов, которые содержат не менее четырех атомов углерода.
Например. Формуле С4Н9ОН соответствуют четыре структурных изомера, из них два различаются строением углеродного скелета
Межклассовые изомеры — это вещества разных классов с различным строением, но одинаковым составом. Спирты являются межклассовыми изомерами с простыми эфирами. Общая формула и спиртов, и простых эфиров — CnH2n+2О.
Например. Межклассовые изомеры с общей формулой С2Н6О этиловый спирт СН3–CH2–OH и диметиловый эфир CH3–O–CH3
| Этиловый спирт | Диметиловый эфир |
| СН3–CH2–OH | CH3–O–CH3 |
Изомеры с различным положением группы ОН отличаются положением гидроксильной группы в молекуле. Такая изомерия характерна для спиртов, которые содержат три или больше атомов углерода.
Например. Пропанол-1 и пропанол-2
Химические свойства спиртов
Спирты – органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Химические реакции гидроксисоединений идут с разрывом одной из связей: либо С–ОН с отщеплением группы ОН, либо связи О–Н с отщеплением водорода. Это реакции замещения, либо реакции отщепления (элиминирования).
Свойства спиртов определяются строением связей С–О–Н. Связи С–О и О–Н — ковалентные полярные. При этом на атоме водорода образуется частичный положительный заряд δ+, на атоме углерода также частичный положительный заряд δ+, а на атоме кислорода — частичный отрицательный заряд δ–.
Такие связи разрываются по ионному механизму. Разрыв связи О–Н с отрывом иона Н+ соответствует кислотным свойствам гидроксисоединения. Разрыв связи С–О соответствует основным свойствам и реакциям нуклеофильного замещения.
С разрывом связи О–Н идут реакции окисления, а с разрывом связи С–О — реакции восстановления.
- слабые кислотные свойства, замещение водорода на металл;
- замещение группы ОН
- отрыв воды (элиминирование) – дегидратация
- окисление
- образование сложных эфиров — этерификация
1. Кислотные свойства
Спирты – неэлектролиты, в водном растворе не диссоциируют на ионы; кислотные свойства у них выражены слабее, чем у воды.
1.1. Взаимодействие с раствором щелочей
При взаимодействии спиртов с растворами щелочей реакция практически не идет, т. к. образующиеся алкоголяты почти полностью гидролизуются водой.
Равновесие в этой реакции так сильно сдвинуто влево, что прямая реакция не идет. Поэтому спирты не взаимодействуют с растворами щелочей.
Многоатомные спирты также не реагируют с растворами щелочей.
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Спирты взаимодействуют с активными металлами (щелочными и щелочноземельными). При этом образуются алкоголяты. При взаимодействии с металлами спирты ведут себя, как кислоты.
Например, этанол взаимодействует с калием с образованием этилата калия и водорода.
Видеоопыт взаимодействия спиртов (метанола, этанола и бутанола) с натрием можно посмотреть здесь.
Алкоголяты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла.
Например, этилат калия разлагается водой:
CH3OH > первичные спирты > вторичные спирты > третичные спирты
Многоатомные спирты также реагируют с активными металлами:
Видеоопыт взаимодействия глицерина с натрием можно посмотреть здесь.
1.3. Взаимодействие с гидроксидом меди (II)
Многоатомные спирты взаимодействуют с раствором гидроксида меди (II) в присутствии щелочи, образуя комплексные соли (качественная реакция на многоатомные спирты).
Например, при взаимодействии этиленгликоля со свежеосажденным гидроксидом меди (II) образуется ярко-синий раствор гликолята меди:
Видеоопыт взаимодействия этиленгликоля с гидроксидом меди (II) можно посмотреть здесь.
2. Реакции замещения группы ОН
2.1. Взаимодействие с галогеноводородами
При взаимодействии спиртов с галогеноводородами группа ОН замещается на галоген и образуется галогеналкан.
Например, этанол реагирует с бромоводородом.
Видеоопыт взаимодействия этилового спирта с бромоводородом можно посмотреть здесь.
третичные > вторичные > первичные > CH3OH.
Многоатомные спирты также, как и одноатомные спирты, реагируют с галогеноводородами.
Например, этиленгликоль реагирует с бромоводородом:
2.2. Взаимодействие с аммиаком
Гидроксогруппу спиртов можно заместить на аминогруппу при нагревании спирта с аммиаком на катализаторе.
Например, при взаимодействии этанола с аммиаком образуется этиламин.
2.3. Этерификация (образование сложных эфиров)
Одноатомные и многоатомные спирты вступают в реакции с карбоновыми кислотами, образуя сложные эфиры.
Например, этанол реагирует с уксусной кислотой с образованием этилацетата (этилового эфира уксусной кислоты):
Многоатомные спирты вступают в реакции этерификации с органическими и неорганическими кислотами.
Например, этиленгликоль реагирует с уксусной кислотой с образованием ацетата этиленгликоля:
2.4. Взаимодействие с кислотами-гидроксидами
Спирты взаимодействуют и с неорганическими кислотами, например, азотной или серной.
Например, при взаимодействии этанола с азотной кислотой образуется сложный эфир этилнитрат:
Например, глицерин под действием азотной кислоты образует тринитрат глицерина (тринитроглицерин):
3. Реакции замещения группы ОН
В присутствии концентрированной серной кислоты от спиртов отщепляется вода. Процесс дегидратации протекает по двум возможным направлениям: внутримолекулярная дегидратация и межмолекулярная дегидратация.
3.1. Внутримолекулярная дегидратация
При высокой температуре (больше 140оС) происходит внутримолекулярная дегидратация и образуется соответствующий алкен.
Например, из этанола под действием концентрированной серной кислоты при температуре выше 140 градусов образуется этилен:
В качестве катализатора этой реакции также используют оксид алюминия.
Отщепление воды от несимметричных спиртов проходит в соответствии с правилом Зайцева: водород отщепляется от менее гидрогенизированного атома углерода.
Например, в присутствии концентрированной серной кислоты при нагревании выше 140оС из бутанола-2 в основном образуется бутен-2:
3.2. Межмолекулярная дегидратация
При низкой температуре (меньше 140оС) происходит межмолекулярная дегидратация по механизму нуклеофильного замещения: ОН-группа в одной молекуле спирта замещается на группу OR другой молекулы. Продуктом реакции является простой эфир.
Например, при дегидратации этанола при температуре до 140оС образуется диэтиловый эфир:
4. Окисление спиртов
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
В зависимости от интенсивности и условий окисление можно условно разделить на каталитическое, мягкое и жесткое.
Первичный спирт → альдегид → карбоновая кислота
Метанол → формальдегид → углекислый газ
Вторичные спирты окисляются в кетоны: вторичные спирты → кетоны
Типичные окислители — оксид меди (II), перманганат калия KMnO4, K2Cr2O7, кислород в присутствии катализатора.
Легкость окисления спиртов уменьшается в ряду:
метанол < первичные спирты < вторичные спирты < третичные спирты
Продукты окисления многоатомных спиртов зависят от их строения. При окислении оксидом меди многоатомные спирты образуют карбонильные соединения.
4.1. Окисление оксидом меди (II)
Cпирты можно окислить оксидом меди (II) при нагревании. При этом медь восстанавливается до простого вещества. Первичные спирты окисляются до альдегидов, вторичные до кетонов, а метанол окисляется до метаналя.
Например, этанол окисляется оксидом меди до уксусного альдегида
Видеоопыт окисления этанола оксидом меди (II) можно посмотреть здесь.
Например, пропанол-2 окисляется оксидом меди (II) при нагревании до ацетона
Третичные спирты окисляются только в жестких условиях.
4.2. Окисление кислородом в присутствии катализатора
Cпирты можно окислить кислородом в присутствии катализатора (медь, оксид хрома (III) и др.). Первичные спирты окисляются до альдегидов, вторичные до кетонов, а метанол окисляется до метаналя.
Например, при окислении пропанола-1 образуется пропаналь
Видеоопыт каталитического окисления этанола кислородом можно посмотреть здесь.
Например, пропанол-2 окисляется кислородом при нагревании в присутствии меди до ацетона
Третичные спирты окисляются только в жестких условиях.
4.3. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) первичные спирты окисляются до карбоновых кислот, вторичные спирты окисляются до кетонов, метанол окисляется до углекислого газа.
При нагревании первичного спирта с перманганатом или дихроматом калия в кислой среде может образоваться также альдегид, если его сразу удаляют из реакционной смеси.
Третичные спирты окисляются только в жестких условиях (в кислой среде при высокой температуре) под действием сильных окислителей: перманганатов или дихроматов. При этом происходит разрыв углеродной цепи и могут образоваться углекислый газ, карбоновая кислота или кетон, в зависимости от строения спирта.
| Спирт/ Окислитель | KMnO4, кислая среда | KMnO4, H2O, t |
| Метанол СН3-ОН | CO2 | K2CO3 |
| Первичный спирт R-СН2-ОН | R-COOH/ R-CHO | R-COOK/ R-CHO |
| Вторичный спирт R1-СНОН-R2 | R1-СО-R2 | R1-СО-R2 |
Например, при взаимодействии метанола с перманганатом калия в серной кислоте образуется углекислый газ
Например, при взаимодействии этанола с перманганатом калия в серной кислоте образуется уксусная кислота
Например, при взаимодействии изопропанола с перманганатом калия в серной кислоте образуется ацетон
4.4. Горение спиртов
Образуются углекислый газ и вода и выделяется большое количество теплоты.
CnH2n+1ОН + 3n/2O2 → nCO2 + (n+1)H2O + Q
Например, уравнение сгорания метанола:
2CH3OH + 3O2 = 2CO2 + 4H2O
5. Дегидрирование спиртов
При нагревании спиртов в присутствии медного катализатора протекает реакция дегидрирования. При дегидрировании метанола и первичных спиртов образуются альдегиды, при дегидрировании вторичных спиртов образуются кетоны.
Например, при дегидрировании этанола образуется этаналь
Например, при дегидрировании этиленгликоля образуется диальдегид (глиоксаль)
Получение спиртов
1. Щелочной гидролиз галогеналканов
При взаимодействии галогеналканов с водным раствором щелочей образуются спирты. Атом галогена в галогеналкане замещается на гидроксогруппу.
Например, при нагревании хлорметана с водным раствором гидроксида натрия образуется метанол
Например, глицерин можно получить щелочным гидролизом 1,2,3-трихлорпропана:
2. Гидратация алкенов
Гидратация (присоединение воды) алкенов протекает в присутствии минеральных кислот. При присоединении воды к алкенам образуются спирты.
Например, при взаимодействии этилена с водой образуется этиловый спирт.
Гидратация алкенов также протекает по ионному (электрофильному) механизму.
Для несимметричных алкенов реакция идёт преимущественно по правилу Марковникова.
Например, при взаимодействии пропилена с водой образуется преимущественно пропанол-2.
3. Гидрирование карбонильных соединений
Присоединение водорода к альдегидам и кетонам протекает при нагревании в присутствии катализатора. При гидрировании альдегидов образуются первичные спирты, при гидрировании кетонов — вторичные спирты, а из формальдегида образуется метанол.
Например, при гидрировании этаналя образуется этанол
Например: при гидрировании ацетона образуется изопропанол
Например, гидрирование диальдегида – один из способов получения этиленгликоля
4. Окисление алкенов холодным водным раствором перманганата калия
Алкены реагируют с водным раствором перманганата калия без нагревания. При этом образуются двухатомные спирты (гликоли).
5. Промышленное получение метанола из «синтез-газа»
Каталитический синтез метанола из монооксида углерода и водорода при 300-400°С и давления 500 атм в присутствии смеси оксидов цинка, хрома и др.
Сырьем для синтеза метанола служит «синтез-газ» (смесь CO и H2), обогащенный водородом:
CO + 2H2 ⇄ CH3OH
6. Получение этанола спиртовым брожением глюкозы
Для глюкозы характерно ферментативное брожение, то есть распад молекул на части под действием ферментов. Один из вариантов — спиртовое брожение.
7. Гидролиз жиров – способ получения многоатомных спиртов
Под действием кислоты жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
Например: при гидролизе тристеарата глицерина образуется глицерин и стеариновая кислота
При щелочном гидролизе жиров образуется глицерин и соли карбоновых кислот, входивших в состав жира.
Например: при щелочном гидролизе тристеарата глицерина образуется глицерин и соль стеариновой кислоты (стеарат)

Валерий Мигунов
Сначала выбирается самая длинная углеродная цепь, содержащая наибольшее число гидроксильных групп. Потом перечисляются углеводородные радикалы. Далее, указывается число гидроксильных групп при помощи суффиксов -ди, -три, -тетра и т.д. Указываем цифры, которые указывают положение гидроксильных групп. И добавляем суффикс -ол.
Например, СН2ОН-СН(С2Н5)-СН(СН3)-СН2ОН-СН2ОН-СН(СН3)-СН2ОН — 2,5-диметил-6-этил-гептатетра-1,3,4,7-ол.
Также используются тривиальные названия (этиленгликоль — простейший двухатомный спирт, глицерин — простейший трехатомный спирт, сорбит — простейший шестиатомный спирт и т.п.).