-
Маруня
18 октября, 05:14
+3
Cu+H2SO4=CuSO4+H2 (газ)
CuSO4+2NaOH=Cu (OH) 2+Na2SO4
Cu (OH) 2+2HNO3=Cu (NO3) 2+2H2O
- Комментировать
- Жалоба
- Ссылка
-
Рипсимия
18 октября, 06:30
-1
Cu+H2SO4=CuSO4
CuSO4+2NaOH=Cu (OH) 2+Na2SO4
Cu (OH) 2+2HNO3=Cu (NO3) 2+2H2O
Второго — это для второй реакции? Если да, то
Cu+2OH=Cu (OH) 2
- Комментировать
- Жалоба
- Ссылка
Найди верный ответ на вопрос ✅ «Cu — CuSO4 — Cu (OH) 2 — (HNO3 — то что нужно добавить) — X. Напишите уравнения реакций и для второго составьте сокращенное ионное …» по предмету 📙 Химия, а если ответа нет или никто не дал верного ответа, то воспользуйся поиском и попробуй найти ответ среди похожих вопросов.
Искать другие ответы
Главная » Химия » Cu — CuSO4 — Cu (OH) 2 — (HNO3 — то что нужно добавить) — X. Напишите уравнения реакций и для второго составьте сокращенное ионное уравнение.

14) Напишите молекулярные и там, где это имеет место, — ионные уравнения реакций согласно схеме:
Cu-CuO-CuSO4-Cu(OH)2
Укажите типы реакций по числу и составу исходных веществ и продуктов реакции.
15)Даны вещества, формулы которых: NaOH, SO3, H2O, CuCL. Составьте уравнения возможных реакций между ними.
Составьте уравнения соответствующих реакций. Реакции ионного обмена запишите также в ионной форме CuSO4 ⟶ Cu(OH)2 ⟶ CuO ⟶ Cu
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,405
- гуманитарные 33,632
- юридические 17,905
- школьный раздел 607,990
- разное 16,855
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
11 класс
- Как вы можете объяснить такие термины, как «твердые растворы» и «жидкие кристаллы», которые на первый взгляд не соответствуют традиционным представлениям о растворах и кристаллах. Какими свойствами обладают твердые растворы и жидкие кристаллы?
Химик получил образцы трех металлов серебристо-белого цвета и нашел способ как их быстро различить. Для этого он подверг образцы действию кислот и раствора гидроксида натрия. Результаты его исследования представлены ниже.
HCl (конц.)
HNO3(конц.)
NaOH
водный раствор
Металл I
—
+
—
Металл II
+
—
+
Металл III
+
+
+
Условные обозначения : «+» — реакция идет, «–» — металл не реагирует.
Определите какие металлы могли быть получены химиком и напишите соответствующие уравнения реакций.
После обработки смеси двух сложных эфиров избытком раствора щелочи в полученном водном растворе найдены следующие вещества: глицерин, фенолят натрия, ацетат натрия и нитрат натрия. Определить формулы сложных эфиров, написать уравнения реакций и указать условия их протекания.
Составьте уравнения реакций по схеме:
А реакция замещения > В реакция соединения > С реакция замещения > D реакция обмена > Е
Составьте уравнения реакций по схеме:
Cu → CuSO4 → Cu(OH)2 → Cu2O → CuO
- Под термином раствор обычно подразумевают жидкость, в которой равномерно распределено растворенное вещество. Такая система характеризуется определенным набором свойств. Истинные растворы имеют одинаковый состав в каждой точке объема.
Твердый раствор — система переменного состава, где атомы различных примесных элементов распределены в общей кристаллической решетке основного кристаллического вещества. Твердые растворы способны образовывать все кристаллические вещества. Атомы примеси могут располагаться в основной кристаллической решетке по-разному: упорядоченно и хаотически. Принято считать, что твердые растворы образуются лучше в том случае, если различие радиусов атомов основного и примесного вещества не превышает 15%.
Жидкие кристаллы образуют вещества, имеющие молекулы удлиненной формы. По степени упорядоченности жидкие кристаллы занимают промежуточное положение между жидкостями и твердыми кристаллами. Жидкие кристаллы характеризуются свойствами жидкости — текучестью и твердого кристалла — анизотропией, т.е. зависимостью физических свойств от направления. Другими словами, структура жидкого кристалла легко изменяется при некоторых внешних воздействиях (магнитное или электрическое поле) с изменением свойств. Таким образом, кажущаяся парадоксальность этих терминов на самом деле оборачивается точным обозначением сути явления.
По совокупности свойств, т.е. по поведению в реакциях с кислотами и гидроксидом натрия заключаем: I металл — серебро,(медь не подходит по цвету), металл II — алюминий, металл III — цинк.
Уравнения реакций:
2Al + 6HCl = 2AlCl3 + 3H2
Zn + 2HCl = ZnCl2 + 2H2
Ag + 2HNO3 (конц.) = AgNO3 + NO2 + H2O
Al + HNO3 (конц.) Нет реакции
Zn + 4HNO3 (конц.) + Zn(NO3)2 + 2NO2 + 2H2O
Zn + 2NaOH + 2H2O = Na2[Zn(OH)4] + H2
2Al + 6NaOH + 6H2O = 2Na3[Al(OH)6] + 3H2
Ответы могут быть различные.
Cu + 2H2SO4 (конц.) → СuSO4 + SO2 + 2H2O
CuSO4 + 2NaOH → Cu(OH)2 ↓ + Na2SO4
Cu(OH)2 + глюкоза (альдегид) + NaOH → (нагревание)
→ Cu2O + H2O + глюконат натрия (натриевая соль карбоновой кислоты)
2Сu2O + O2 → 4CuO (прокаливание)
Горение углеводорода СxНy описывается схемой реакции:
СxНy + (ч + 0,25у)О2 = хСО2 + 0,5уН2О … + О2остаток
Количество вещества углекислого газа в х раз больше количества вещества исходного углеводорода. Количественные соотношения равны объемным, следовательно, объем углекислого газа в х раз больше объема исходного углеводорода.
Так как сумма объемов углекислого газа и остаточного кислорода составляет 120 мл, то , откуда и .
По условию х не равен единице (…искомый углеводород не является метаном), и не может быть дробным числом, следовательно, .
Воспользуемся еще раз уравнением: 50х + V(О2)ост. = 120
Отсюда объем избыточного кислорода составляет
Напишите уравнения химических реакций, соответствующие следующим превращениям:
а) Ca → CaO → Ca(OH)2;
б) Cu → CuO → CuSO4;
в) P → P2O5 → H3PO4;
г) SO3 + … → K2SO4 + …;
д) N2O5 + LiOH → …;
е) P2O5 + … → Ca3(PO4)2 + …
Цитата:
Ближайший предмет химии составляет изучение однородных веществ, из сложения которых составлены все тела мира, превращений их друг в друга и явлений, сопровождающих такие превращения.
Дмитрий Иванович Менделеев
русский учёный-энциклопедист, создатель периодической таблицы химических элементов.
Внимание! Решения предоставлены обычными людьми, поэтому в решениях могут быть ошибки или неточности. Используя решения, не забудьте их перепроверить!
Решение Решения:
1, 2
Похожие задачи:
Внимание! Решения предоставлены обычными людьми, поэтому в решениях могут быть ошибки или неточности. Используя решения, не забудьте их перепроверить!
Решение Осуществите следующие превращения: Cu → CuSO4 → Cu(OH)2 → CuO → Cu
Решение Осуществить превращение и записать уравнение в ионном и молекулярном видах CuSO4 → Cu(OH)2 → CuO → CuCl2
Решение Cu → CuO → Cu(OH)2 → Cu(NO3)2 → Cu(OH)2 → CuO → CU
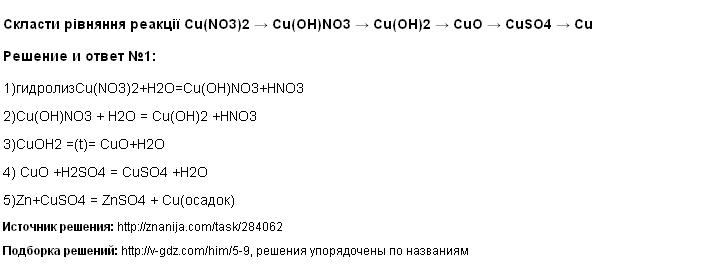
Решение Скласти рівняння реакції Cu(NO3)2 → Cu(OH)NO3 → Cu(OH)2 → CuO → CuSO4 → Cu
Решение CU → CUO → CU(NO3)2 → CU(OH)2 → CUO → CU
Решение Cu → CuO → CuSO4 → Cu(OH)2
Решение CuSO4 → Cu(OH)2 → CuO → cu
Решение CuSO4 → Cu(OH)2 → CuO → CuCl → Cu(NO3)2 → CuS.
Решение Осуществить практически следующие превращения :CuCO3 → CuCl2 → Cu (OH)2 → CuO → CuCl2 → AgCl
Решение CuCl2 → Cu → CuO → Cu(NO3)2 → Cu(OH)2
Решение проведите химические реакции FeSO4 → Fe(OH)2 → FeCl2 CuSO4 → Cu(OH)2 → Cu(NO3)2
Решение CuO → CU → CuCl2 → Cu(OH)2 → CuSO4
Решение Осуществите превращения K → KON → Cu(OH)2 → CuO. Укажите типы хим.реакций
Решение Составьте уравнения реакций следующих превращений:Cu → Cu(No3)2 → Cu(OH)2 → CuO → Cu
Решение Осуществить превращение: Cu → CuO → Cu(NO3)2 → Cu(OH)2 → CuSO4.
Решение Cu → CuSO4 → Cu(OH)2 → CuO → Cu
Решение Здийснити перетворення: Сu(No3)2 → CuO → Cu(OH)2 → Cu(NO3)2 → CuSO4 → PaSO4
Решение осуществите превращения по схеме: Cu → CuS → CuO → Cu → CuCl2 → Cu(OH)2 → CuO
Решение Осуществить практически следующие превращения CuCO3 → CuCl2 → Cu (OH)2 → CuO
Решение Осуществить превращения Cu(NO3)2 → Cu(OH)2 → CuO
Решение Cu → CuSO4 → CuCl2 → Cu(NO3)2 → Cu(OH)2 → CuO
Решение Cu(OH)2 → CuO → CuSO4 → Cu(OH)2
Решение выполнить цепочку превращений CuSO4 → Cu(OH)2 → CuO → Cu
Решение Осуществите следующие превращения: Mg → MgSO4 → Mg(OH)2 Zn → ZnSO4 → Zn(OH)2 CuO → CuSO4 → Cu(OH)2
Решение HNO3 → Cu(NO3)2 → Cu → CuO → CuSO4
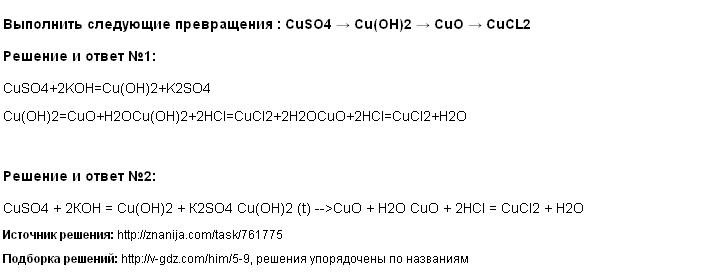
Решение Выполнить следующие превращения : CuSO4 → Cu(OH)2 → CuO → CuCL2
Решение Помогите разобрать уравнение реакций, осуществив превращение Cu → CuCl → Cu(Oh)2 → CuO → CuSO4 → Cu
Решение напишите молекулярные уравнения реакции, с помощью которых можно осуществить следующие превращения:Cu(NO3)2 → Cu → X → Cu(OH)2
Решение CuSO4 → Cu(OH)2 → CuO → Cu. Составьте уравнения соответствующих реакций. Реакции ионного обмена запишите также в ионной форме.
Решение Складіть рівняння реакцій за поданою схемою: Cu → CuO → Cu(NO3)2 → Cu(OH)2 → CuSO4
Решение Cu → CuO → CuCl2 → Cu(OH)2 → CuO → Cu → CuSO4 → Cu(OH)2
Решение Напишите уравнения реакций,при помощи которых можно осуществить следующие превращения: CuSO4 → Cu → CuO → CuCl2 → Cu(OH)2 → Cu(NO3)2.
Cu + CuSO4 -> Cu(OH)2 (сверху над стрелкой: HNO3) -> X
Напишите молекулярные уравнения реакции, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте полное и сокращённое ионное уравнение реакции.