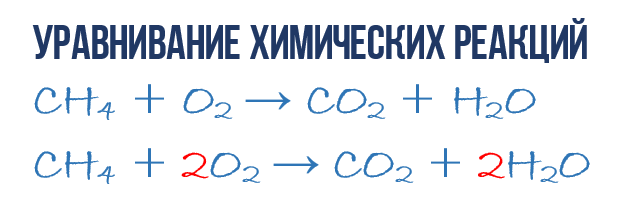Типы химических реакций в органической химии
При протекании химических реакций происходит разрыв одних и возникновение других связей. Химические реакции условно делят на органические и неорганические. Органическими реакциям принято считать реакции, в которых, по крайней мере, одно из реагирующих веществ является органическим соединением, изменяющим свою молекулярную структуру в процессе реакции. Отличием органических реакций от неорганических является то, что, как правило, в них участвуют молекулы. Скорость таких реакции низка, а выход продукта обычно составляет всего лишь 50-80 %. Для повышения скорости реакции применяют катализаторы, повышают температуру или давление. Далее рассмотрим типы химических реакций в органической химии.
Классификация по характеру химических превращений
- Реакции замещения
- Реакции присоединения
- Реакция элиминирования (отщепления)
- Реакция изомеризации и перегруппировка
- Реакции окисления
- Реакции конденсации и поликонденсации
- Реакции разложения
Реакции замещения
В ходе реакций замещения один атом или группа атомов в начальной молекуле замещается на иные атомы или группы атомов, образуя новую молекулу. Как правило, такие реакции характерны для насыщенных и ароматических углеводородов, например:
Реакции присоединения
При протекании реакций присоединения из двух или более молекул веществ образуется одна молекула нового соединения. Такие реакции характерны для ненасыщенных соединений. Различают реакции гидрирования (восстановления), галогенирования, гидрогалогенирования, гидратации, полимеризации и т.п:
- Гидрирование – присоединение молекулы водорода:
- Галогенирование — присоединение молекулы галогена:
- Гидрогалогенирование — присоединение молекулы галогенводорода:
- Гидратация — присоединение молекулы воды:
- Полимеризация – образование высокомолекулярного соединения посредством многократного присоединения низкомолекулярного соединения, например:
Реакция элиминирования (отщепления)
В результате реакций отщепления органические молекулы теряют атомы или группы атомов, и образуется новое вещество, содержащее одну или несколько кратных связей. К реакциям элиминирования относятся реакции дегидрирования, дегидратации, дегидрогалогенирования и т.п.:
- Дегидрирование – отщепления молекулы водорода:
- Дегидратация – отщепление молекулы воды:
- Дегидрогалогенирования – отщепления молекулы галогеноводородов:
Реакции изомеризации и перегруппировка
В ходе таких реакций происходит внутримолекулярная перестройка, т.е. переход атомов или групп атомов с одного участка молекулы в другое без изменения молекулярной формулы вещества, участвующего в реакции, например:
Реакции окисления
В результате воздействия окисляющего реагента происходит повышение степени окисления углерода в органическом атоме, молекуле или ионе процесс за счет отдачи электронов, вследствие чего образуется новое соединение:
Реакции конденсации и поликонденсации
Заключаются во взаимодействии нескольких (двух и более) органических соединений с образованием новых С-С связей и низкомолекулярного соединения:
Поликонденсация – образование молекулы полимера из мономеров, содержащих функциональные группы с выделением низкомолекулярного соединения. В отличие от реакции полимеризации, в результате которых образуется полимер, имеющий состав, аналогичный мономеру, в результате реакций поликонденсации состав образованного полимера отличается от его мономера:
Реакции разложения
Это процесс расщепления сложного органического соединения на менее сложные или простые вещества:
Классификация химических реакций по механизмам
Протекание реакций с разрывом ковалентных связей в органических соединениях возможно по двум механизмам (т.е. пути, приводящему к разрыву старой связи и образованию новой) – гетеролитическому (ионному) и гомолитическому (радикальному).
Гетеролитический (ионный) механизм
В реакциях, протекающих по гетеролитическому механизму образуются промежуточные частицы ионного типа с заряженным атомом углерода. Частицы, несущие положительный заряд называются карбкатионы, отрицательный – карбанионы. При этом происходит не разрыв общей электронной пары, а ее переход к одному из атомов, с образованием иона:
Склонность к гетеролитическому разрыву проявляют сильно полярные, например Н–O, С–О и легко поляризуемые, например С–Вr, С–I связи.
Реакции, протекающие по гетеролитическому механизму делят на нуклеофильные и электрофильные реакции. Реагент, располагающий электронной парой для образования связи называют нуклеофильным или электронодонорным. Например, HO — ,RO — , Cl — , RCOO — , CN — , R — , NH2, H2O, NH3, C2H5OH, алкены, арены.
Реагент, имеющий незаполненную электронную оболочку и способные присоединить пару электронов в процессе образования новой связи.называют электрофильным реагентам относятся следующие катионы: Н + , R3C + , AlCl3, ZnCl2, SO3, BF3, R-Cl, R2C=O
Реакции нуклеофильного замещения
Характерны для алкил- и арилгалогенидов:
Реакции нуклеофильного присоединения
Реакции электрофильного замещения
Реакции электрофильного присоединения
Гомолитический (радикальный механизм)
В реакциях, протекающих по гомолитическому (радикальному) механизму на первой стадии происходит разрыв ковалентной связи с образованием радикалов. Далее образовавшийся свободный радикал выступает в качестве атакующего реагента. Разрыв связи по радикальному механизму свойственен для неполярных или малополярных ковалентных связей (С–С, N–N, С–Н).
Различают реакции радикального замещения и радикального присоединения
Реакции радикального замещения
Характерны для алканов
Реакции радикального присоединения
Характерны для алкенов и алкинов
Таким образом, мы рассмотрели основные типы химических реакций в органической химии
Химические реакции в органической химии
Существуют разные системы классификации органических реакций, которые основаны на различных признаках. Среди них можно выделить классификации:
по конечному результату реакции, то есть изменению в структуре субстрата;
по механизму протекания реакции, то есть по типу разрыва связей и типу реагентов.
Взаимодействующие в органической реакции вещества подразделяют на реагент и субстрат. При этом считается, что реагент атакует субстрат.
Реагент — вещество, действующее на объект — субстрат — и вызывающее в нем изменение химической связи. Реагенты делятся на радикальные, электрофильные и нуклеофильные.
Субстратом , как правило, считают молекулу, которая предоставляет атом углерода для новой связи.
В органической химии различают четыре вида реакций по конечному результату и изменению в структуре субстрата: присоединения, замещения, отщепления, или элиминирования (от англ. to eliminate — удалять, отщеплять), и перегруппировки (изомеризации). Такая классификация аналогична классификации реакций в неорганической химии по числу исходных реагентов и образующихся веществ, с изменением или без изменения состава. Классификация по конечному результату основана на формальных признаках, так как стехиометрическое уравнение, как правило, не отражает механизм реакции. Сравним типы реакций в неорганической и органической химии.
Тип реакции в неорганической химии
Пример
Тип реакции в органической химии
Присоединение по кратным связям
частный случай — этерификация
Разновидность
и пример
реакции
4. Обмен (частный случай — нейтрализация)
Pкрасн.⇔P бел.Pкрасн.⇔P бел.
п) без замены их другими.
В зависимости от того, какие атомы отщепляются — соседние C – C или изолированные двумя-тремя или более атомами углерода – C –C–C– C –, – C –C–C–C– C –, могут образовываться соединения с кратными связями или циклические соединения. Отщепление галогеноводородов из алкилгалогенидов либо воды из спиртов происходит по правилу Зайцева.
Правило Зайцева : атом водорода Н отщепляется от наименее гидрогенизированного атома углерода.
Например, отщепление молекулы бромоводорода происходит от соседних атомов в присутствии щелочи, при этом образуется бромид натрия и вода.
Перегруппировка — химическая реакция, в результате которой происходит изменение взаимного расположения атомов в молекуле, перемещение кратных связей или изменение их кратности.
Перегруппировка может осуществляться с сохранением атомного состава молекулы (изомеризация) или с его изменением.
Изомеризация — частный случай реакции перегруппировки, приводящая к превращению химического соединения в изомер путем структурного изменения углеродного скелета.
Перегруппировка тоже может осуществляться по гомолитическому или гетеролитическому механизму. Молекулярные перегруппировки могут классифицироваться по разным признакам, например по насыщенности систем, по природе мигрирующей группы, по стереоспецифичности и др. Многие реакции перегруппировки имеют специфические названия — перегруппировка Кляйзена, перегруппировка Бекмана и др.
Реакции изомеризации широко используются в промышленных процессах, например при переработке нефти для повышения октанового числа бензина. Примером изомеризации является превращение н-октана в изооктан:
Разрыв связи в органических соединениях может гомолитическим и гетеролитическим.
Гомолитический разрыв связи — это такой разрыв, в результате которого каждый атом получает неспаренный электрон и образуются две частицы, имеющие сходное электронное строение — свободные радикалы .
Гомолитический разрыв характерен для неполярных или слабополярных связей, например C–C, Cl–Cl, C–H, и требует большого количества энергии.
Образующиеся радикалы, имеющие неспаренный электрон, обладают высокой реакционной способностью, поэтому химические процессы, протекающие с участием таких частиц, часто носят «цепной» характер, их трудно контролировать, а в результате реакции получается набор продуктов замещения. Так, при хлорировании метана продуктами замещения являются хлорметан CH3ClCH3Cl, дихлорметан CH2Cl2CH2Cl2, хлороформ CHCl3CHCl3 и четыреххлористый углерод CCl4CCl4. Реакции с участием свободных радикалов протекают по обменному механизму образования химических связей.
Образующиеся в ходе такого разрыва связи радикалы обуславливают радикальный механизм протекания реакции. Радикальные реакции обычно протекают при повышенных температурах или при излучении (например, свет).
В силу своей высокой реакционной способности свободные радикалы могут оказывать негативное воздействие на организм человека, разрушая клеточные мембраны, воздействуя на ДНК и вызывая преждевременное старение. Эти процессы связаны, в первую очередь, с пероксидным окислением липидов, то есть разрушением структуры полиненасыщенных кислот, образующих жир внутри клеточной мембраны.
Гетеролитический разрыв связи — это такой разрыв, при котором электронная пара остается у более электроотрицательного атома и образуются две заряженные частицы — ионы: катион (положительный) и анион (отрицательный).
В химических реакциях эти частицы выполняют функции « нуклеофилов » («фил» — от гр. любить) и « электрофилов », образуя химическую связь с партнером по реакции по донорно-акцепторному механизму. Частицы-нуклеофилы предоставляют электронную пару для образования новой связи. Другими словами,
Нуклеофил — электроноизбыточный химический реагент, способный взаимодействовать с электронодефицитными соединениями.
Примерами нуклеофилов являются любые анионы (Cl−,I−,NO−3Cl−,I−,NO3− и др.), а также соединения, имеющие неподеленную электронную пару (NH3,H2ONH3,H2O).
Таким образом, при разрыве связи могут образоваться радикалы или нуклеофилы и электрофилы. Исходя из этого выделяют три механизма протекания органических реакций.
Свободно-радикальный механизм : реакцию начинают свободные радикалы, образующиеся при гомолитическом разрыве связи в молекуле.
Наиболее типичный вариант — образование радикалов хлора или брома при УФ-облучении.
Урок 13. Составление химических уравнений
В уроке 13 «Составление химических уравнений» из курса «Химия для чайников» рассмотрим для чего нужны химические уравнения; научимся уравнивать химические реакции, путем правильной расстановки коэффициентов. Данный урок потребует от вас знания химических основ из прошлых уроков. Обязательно прочитайте об элементном анализе, где подробно рассмотрены эмпирические формулы и анализ химических веществ.
Химическое уравнение
В результате реакции горения метана CH4 в кислороде O2 образуются диоксид углерода CO2 и вода H2O. Эта реакция может быть описана химическим уравнением:
Попробуем извлечь из химического уравнения больше сведений, чем просто указание продуктов и реагентов реакции. Химичекое уравнение (1) является НЕполным и потому не дает никаких сведений о том, сколько молекул O2 расходуется в расчете на 1 молекулу CH4 и сколько молекул CO2 и H 2 O получается в результате. Но если записать перед соответствующими молекулярными формулами численные коэффициенты, которые укажут сколько молекул каждого сорта принимает участие в реакции, то мы получим полное химическое уравнение реакции.
Для того, чтобы завершить составление химического уравнения (1), нужно помнить одно простое правило: в левой и правой частях уравнения должно присутствовать одинаковое число атомов каждого сорта, поскольку в ходе химической реакции не возникает новых атомов и не происходит уничтожение имевшихся. Данное правило основывается на законе сохранения массы, который мы рассмотрели в начале главы.
Уравнивание химических реакций
Уравнивание химических реакций нужно для того, чтобы из простого химического уравнения получить полное. Итак, перейдем к непосредственному уравниванию реакции (1): еще раз взгляните на химическое уравнение, в точности на атомы и молекулы в правой и левой части. Нетрудно заметить, что в реакции участвуют атомы трех сортов: углерод C, водород H и кислород O. Давайте подсчитаем и сравним количество атомов каждого сорта в правой и левой части химического уравнения.
Начнем с углерода. В левой части один атом С входит в состав молекулы CH4, а в правой части один атом С входит в состав CO2. Таким образом в левой и в правой части количество атомов углерода совпадает, поэтому его мы оставляем в покое. Но для наглядности поставим коэффициент 1 перед молекулами с углеродом, хоть это и не обязательно:
Затем переходим к подсчету атомов водорода H. В левой части присутствуют 4 атома H (в количественном смысле H4 = 4H) в составе молекулы CH4, а в правой – всего 2 атома H в составе молекулы H2O, что в два раза меньше чем в левой части химического уравнения (2). Будем уравнивать! Для этого поставим коэффициент 2 перед молекулой H2O. Вот теперь у нас и в реагентах и в продуктах будет по 4 молекулы водорода H:
Обратите свое внимание, что коэффициент 2, который мы записали перед молекулой воды H2O для уравнивания водорода H, увеличивает в 2 раза все атомы, входящие в ее состав, т.е 2H2O означает 4H и 2O. Ладно, с этим вроде бы разобрались, осталось подсчитать и сравнить количество атомов кислорода O в химическом уравнении (3). Сразу бросается в глаза, что в левой части атомов O ровно в 2 раза меньше чем в правой. Теперь-то вы уже и сами умеете уравнивать химические уравнения, поэтому сразу запишу финальный результат:
Как видите, уравнивание химических реакций не такая уж и мудреная штука, и важна здесь не химия, а математика. Уравнение (4) называется полным уравнением химической реакции, потому что в нем соблюдается закон сохранения массы, т.е. число атомов каждого сорта, вступающих в реакцию, точно совпадает с числом атомов данного сорта по завершении реакции. В каждой части этого полного химического уравнения содержится по 1 атому углерода, по 4 атома водорода и по 4 атома кислорода. Однако стоит понимать пару важных моментов: химическая реакция — это сложная последовательность отдельных промежуточных стадий, и потому нельзя к примеру истолковывать уравнение (4) в том смысле, что 1 молекула метана должна одновременно столкнуться с 2 молекулами кислорода. Процессы происходящие при образовании продуктов реакции гораздо сложнее. Второй момент: полное уравнение реакции ничего не говорит нам о ее молекулярном механизме, т.е о последовательности событий, которые происходят на молекулярном уровне при ее протекании.
Коэффициенты в уравнениях химических реакций
Еще один наглядный пример того, как правильно расставить коэффициенты в уравнениях химических реакций: Тринитротолуол (ТНТ) C7H5N3O6 энергично соединяется с кислородом, образуя H2O, CO2 и N2. Запишем уравнение реакции, которое будем уравнивать:
Проще составлять полное уравнение, исходя из двух молекул ТНТ, так как в левой части содержится нечетное число атомов водорода и азота, а в правой — четное:
- 2C7H5N3O6 + O2 → CO2 + H2O + N2 (6)
Тогда ясно, что 14 атомов углерода, 10 атомов водорода и 6 атомов азота должны превратиться в 14 молекул диоксида углерода, 5 молекул воды и 3 молекулы азота:
Теперь в обеих частях содержится одинаковое число всех атомов, кроме кислорода. Из 33 атомов кислорода, имеющихся в правой части уравнения, 12 поставляются двумя исходными молекулами ТНТ, а остальные 21 должны быть поставлены 10,5 молекулами O2. Таким образом полное химическое уравнение будет иметь вид:
Можно умножить обе части на 2 и избавиться от нецелочисленного коэффициента 10,5:
Но этого можно и не делать, поскольку все коэффициенты уравнения не обязательно должны быть целочисленными. Правильнее даже составить уравнение, исходя из одной молекулы ТНТ:
Полное химическое уравнение (9) несет в себе много информации. Прежде всего оно указывает исходные вещества — реагенты, а также продукты реакции. Кроме того, оно показывает, что в ходе реакции индивидуально сохраняются все атомы каждого сорта. Если умножить обе части уравнения (9) на число Авогадро NA=6,022·10 23 , мы сможем утверждать, что 4 моля ТНТ реагируют с 21 молями O2 с образованием 28 молей CO2, 10 молей H2O и 6 молей N2.
Есть еще одна фишка. При помощи таблицы Менделеева определяем молекулярные массы всех этих веществ:
- C 7 H 5 N 3 O 6 = 227,13 г/моль
- O 2 = 31,999 г/моль
- CO 2 = 44,010 г/моль
- H 2 O = 18,015 г/моль
- N 2 = 28,013 г/моль
Теперь уравнение 9 укажет еще, что 4·227,13 г = 908,52 г ТНТ требуют для осуществления полной реакции 21·31,999 г = 671,98 г кислорода и в результате образуется 28·44,010 г = 1232,3 г CO2, 10·18,015 г = 180,15 г H2O и 6·28,013 г = 168,08 г N2. Проверим, выполняется ли в этой реакции закон сохранения массы:
| Реагенты | Продукты | |
| 908,52 г ТНТ | 1232,3 г CO 2 | |
| 671,98 г CO 2 | 180,15 г H 2 O | |
| 168,08 г N 2 | ||
| Итого | 1580,5 г | 1580,5 г |
Но необязательно в химической реакции должны участвовать индивидуальные молекулы. Например, реакция известняка CaCO 3 и соляной кислоты HCl, с образованием водного раствора хлорида кальция CaCl 2 и диоксида углерода CO 2 :
Химическое уравнение (11) описывает реакцию карбоната кальция CaCO3 (известняка) и хлористоводородной кислоты HCl с образованием водного раствора хлорида кальция CaCl2 и диоксида углерода CO2. Это уравнение полное, так как число атомов каждого сорта в его левой и правой частях одинаково.
Смысл этого уравнения на макроскопическом (молярном) уровне таков: 1 моль или 100,09 г CaCO3 требует для осуществления полной реакции 2 моля или 72,92 г HCl, в результате чего получается по 1 молю CaCl2 (110,99 г/моль), CO2 (44,01 г/моль) и H2O (18,02 г/моль). По этим численным данным нетрудно убедиться, что в данной реакции выполняется закон сохранения массы.
Интерпретация уравнения (11) на микроскопическом (молекулярном) уровне не столь очевидна, поскольку карбонат кальция представляет собой соль, а не молекулярное соединение, а потому нельзя понимать химическое уравнение (11) в том смысле, что 1 молекула карбоната кальция CaCO3 реагирует с 2 молекулами HCl. Тем более молекула HCl в растворе вообще диссоциирует (распадается) на ионы H + и Cl — . Таким образом более правильным описанием того, что происходит в этой реакции на молекулярном уровне, дает уравнение:
Здесь в скобках сокращенно указано физическое состояние каждого сорта частиц (тв. — твердое, водн. — гидратированный ион в водном растворе, г. — газ, ж. — жидкость).
Уравнение (12) показывает, что твердый CaCO3 реагирует с двумя гидратированными ионами H + , образуя при этом положительный ион Ca 2+ , CO2 и H2O. Уравнение (12) как и другие полные химические уравнения не дает представления о молекулярном механизме реакции и менее удобно для подсчета количества веществ, однако, оно дает лучшее описание происходящего на микроскопическом уровне.
Закрепите полученные знания о составлении химических уравнений, самостоятельно разобрав пример с решением:
Надеюсь из урока 13 «Составление химических уравнений» вы узнали для себя что-то новое. Если у вас возникли вопросы, пишите их в комментарии.
http://www.sites.google.com/site/abrosimovachemy/materialy-v-pomos-ucenikam/distancionnoe-obucenie/10-klass/himiceskie-reakcii-v-organiceskoj-himii
1. р. присоединения (+Н2, +Вr2,+НI) у циклов с 3,4 5 атомами углеродаC3H6 +Br2=Br—CH2—CH2—CH2Br;
2. р. замещения – аналогично алканам (циклы с 6 и атомами углерода);
3. р. элиминирования (дегидрирования) С6Н12 → С6Н6 + 3Н2↑(катализ: Ni, t)
4. р. окисления – на примере циклогексана сильным окислителем: С6Н12 + 4[О] → СН2-СН2-СООН
3. Алкены (непредельные). Общая формула – СпН2п. М (СпН2п)= 14п г/моль, σ- и π-связи, SP2-гибридизация,
1.р. присоединение Н2, НГ, Г2 и Н2О (разрыв С=С связи, электрофильный мех-зм)
а) гидрогалогенирование:СН2=СН2 + НBr → СН3-СН2Br
в случае несимметричной π-связи по правилу Марковникова (Н к СН2):
СН3-СН=СН2 + НBr → СН3-СНBr-СН3; продолжение см. дальше.
б) гидратация:СН3-С=СН2 + НОН → СН3-С(ОН)-СН3 (в присутствии минерал кислот)
│ │
СН3 СН3
в) галогенирование (обесцвечивание раствора бромной воды – Br2) – качественная реакция на кратную связь, как и реакция с раствором КМпО4: СН2 = СН2 + Br2 → BrСН2-СН2Br
г)гидрирование: СН3-СН=СН2 + Н2 → СН3-СН2-СН3 (катализатор – Ni, t)
2.р. замещения (радикальный мех-зм) – замещение атома Н на соседнем с двойной связью атоме углерода, при t=5000С: СН3-СН=СН2 + Cl2 → ClСН2-СН=СН3 + НCl
3.р. окисления:а) мягкое – холодным раствором КМпО4(р. Вагнера)
СН2 = СН2 + [О] + Н2О → СН2ОН-СН2ОН (упрощенная запись)
или 3СН2 = СН2 + 2КМпО4 + 4Н2О → 3СН2ОН-СН2ОН + 2МпО2↓ + 2КОН
б)жесткое – кипящим раствором КМпО4 в кислой среде СН3-СН=СН-СН3 + 4[О] → 2 СН3-СООН
4.р. полимеризации: пСН2=СН2 → ( — СН2-СН2 — ) в кислой среде.
5.получение алкенов: а) С7Н16 —→ C4Н10 + CН3—CН=CН2 (t,Kat);
б) СН3-СН2-СНBr-СН3 + КОН (спирт)→СН3-СН=СН-СН3 + КBr + Н2О
в) СН3-СН-СН3 → СН3-СН=СН2 + Н2О (t=1500С, в кислой среде) по правилу Зайцева
│
ОН
г) СН2Br— СНBr-СН3 + 2К → СН2=СН-СН3 + 2КBr – синтез Вюрца—Крафтса
д) СН3-СН2-СН3 → СН3-СН=СН2 + Н2↑ в присутствии Kat – Cr2O3
4. Алкадиены (непредельные). Общая формула – СпН2п-2. М (СпН2п-2)= (14п-2) г/моль, σ- и 2π-связи, SP2-гибридизация.
1. р. присоединения: СН2=СН-СН=СН2 ++ Br2→СН2Br-СНBr-СН=СН2 (присоединение по 1,2)
СН2=СН-СН=СН2 + Br2 →[→ СН2Br-СН=СН=СН2Br (присоединение по 1,4)
2. р. полимеризации: пСН2=СН-СН=СН2 → (-СН2-СН=СН-СН2-) в кислоте
3. диеновый синтез – р. Дильса-Альдера- р.циклизации СН2-СН=СН-СН2 + СН2=СН2 → С6Н10 при нагревании, под давлением.
4. получение алкадиенов: а) СН3-СН2-СН2-СН3 → СН2=СН-СН=СН2 + 2Н2↑ при t, Kat – Cr2O3;
б) 2С2Н5ОН → СН2=СН-СН=СН2 + Н2↑ + 2Н2О при t, Kat – Al2O3, ZnO р. Лебедева.
5. Алкины (непредельные). Общая формула – СпН2п-2. М (СпН2п-2)= (14п-2) г/моль, σ- и 2π-связи, SP-гибридизация, линейное строение обладают слабыми кислотными свойствами
1.р. электрофильного присоединения (медленнее, чем у алкенов) — Br2, Н2 и НСl
СН≡СН + Br2 → СНBr=СНBr, далее СНBr=СНBr+ Br2 → СНBr2-СНBr2
2.р. гидратации – р. Кучерова, в кислой среде, Kat – Hg2+
любой алкин образует кетон СН3-С≡СН + НОН →СН3-С (СН3)=О,
только ацетилен СН≡СН + НОН →СН3-СНО — альдегид
3. р. окисления раствором КМпО4: R—C≡C—R‘ + 3[О] + HOH → R—COOH + R‘-COOH
4.р. гидрирования СН3-С≡СН + Н2 → СН3-СН=СН2, далее СН3-СН=СН2 +Н2 →С3Н8
при нагревании, в присутствии катализатора – Pt, Pd продолжение см дальше
5.слабые кислотные свойства у алкинов с «концевой» кратной связью:
2СН≡СН + 2Na → 2NaC≡CNa + H2, с аммиачным раствором оксида серебра
СН≡СН + [Ag(NH3)2]OH → AgC≡CAg + 4NH3 + 2H2O
6. р. полимеризации: СН≡СН + СН≡СН → СН2=СН-СН=СН2, катализатор –NH4CL
или р. Зелинского 3СН≡СН → С6Н6, условия – активир-ый уголь (Сакт, t=6000С)
7. а): СаС2 + 2НОН → С2Н2↑ + Са(ОН)2↓; б) СаС2 + 2НCL → С2Н2↑ + СаCL2;
в) 2СН4 → С2Н2↑ + 3H2 при t=15000С
6
1. Р. электрофильного замещения: а) галогенирование: С6Н6 + CL2 → С6Н5CL + НCL , катализатор – АLCL3 б) нитрование: С6Н6 + НО – NО2 →С6Н5—NО2 +Н2О, в присутствии H2SO4
в) алкилирование — р. Фриделя-Крафтса – удлинение цепи атомов углерода
С6Н6 + RCl → C6H5-R + HCl, где R – CnH2n+1 (радикалы), катализатор — АLCL3
2. р. присоединения в жёстких условиях – свет, катализатор— Ni (присоединение Н2)
а) С6Н6 + 3Н2 → С6Н12 б) С6Н6 + 3CL2 → С6Н6CL6 на свету
3. для гомологов бензола: а) замещение атомов водорода в цикле (катализаторы FeBr3 и H2SO4) С6Н5-СН3 + Br2 → о-С6Н4(Br)СН3 +НBr в ортоположении, т.е. 1-бром-2-метилбензол
а также →п-С6Н4(Br)СН3 +НBr в параположении, т.е. 1-бром-4-метилбензол
помнить: у гомологов бензола замещение в цикле атомов водорода происходит с равной вероятностью в положении 2, 4, 6 относительно имеющегося радикала в присутствии катализаторов FeBr3 и H2SO4.
б
в
г) радикальное замещение в боковую цепь на свету: С6Н5-СН3 + Br2 → С6Н5-СН2Br + НBr
д) окисление кислым раствором КМпО4 С6Н5-СН3 + 2[О] → С6Н-СООН — упрощенная запись, полная запись: 5С6Н5-СН3+6КМпО4 +9H2SO4 →5С6Н5-СООН +3К2SO4 +6МпSO4 + 14Н2О
электронно-ионный баланс:
С6Н5-СН30 + 2Н2О0 −6е —_→ С6Н5-СООН0 + 6Н+ │5
МпО4— + 8Н+ +5е—→ Мп2+ + 4Н2О │6
4. получение аренов: а) С6Н14 → С6Н6 + 4Н2↑, условия: t, Р, катализатор – Сr2O3
б) С6Н12→ С6Н6 + 3Н2↑, условия: t, катализатор – Pd
в) 3СН≡СН→ С6Н6, условия – активир-ый уголь (Сакт, t=6000С)
г) С6Н5-СООNa + NaOH → C6H6 + Na2CO3 при спекании сухих веществ.
Кислородсодержащие соединения. 1. Одноатомные спирты — алканолы (предельные). Общая формула – R-ОН или СпН2п+2О, М (СпН2п+2О)= (14п+18) г/моль,
Наличие гидроксогруппы — ОН в молекулах спиртов проявляется в слабых кислотных и основных свойств.
1. проявляют кислотные свойства (только реакции с щелочными Ме), убывающие от первичных к третичным спиртам: 2 С2Н5ОН + 2К → 2 С2Н5ОК + Н2↑;
2. слабые основные свойства, возрастающие от первичных к третичным спиртам:
R – ОН + НBr → R – Br + H2O
3. р. этерификации – взаимодействие с кислотами и образование сложных эфиров:
Н+
RСООН + НОR‘ ↔ RСООR‘ + Н2О (в кислой среде);
4. р. окисления подкисленными растворами КМпО4 или К2Сr2О7: а) первичные окисляются в 2 стадии до кислот т.к. имеют 2 атома [Н] на углероде при ОН-группе: 1стад. 2 стад. R — СН2 – ОН + [О] → R — СН2 = О (альдегид); …+ [О] → R – СООН (кислота);
б) вторичные окисляются до кетонов т.к. имеют1 атом [Н] на углероде при ОН-группе: 1стад. R — СН – ОН + [О] → R — С = О
│ │
R‘ R‘
5. р. дегидратации в присутствии раствора Н2SO4 (Al2O3, H3PO4 конц) зависит от температуры:
а) при t 1500С – внутримолекулярная (Н2О отрывается от 1 молекулы):
СН3 – СН2 – СН2 – ОН (+Н2SO4) → СН3 – СН = СН2 + Н2О, продукт — алкен
б) при t 0С – межмолекулярная (Н2О отрывается от 2 молекул):
СН3 – СН2 –– ОН + СН3 – СН2 –– ОН (+Н2SO4) → СН3 –СН2 — О – СН2 – СН3+ Н2О,
продукт – простой эфир.
Различные классы спиртов дегидратируются при различных условиях:
первичные: СН2 – СН2 (конц. Н2SO4 при нагревании) → СН2 = СН2
│ │
Н ОН
вторичные: СН2 – СН – СН3 (конц. Н2SO4 при подогреве) → СН2 = СН
│ │ │
Н ОН СН3
СН3 СН3
│ │
третичные: СН2 – С – СН3 (конц. Н2SO4 на холоде) → СН2 = С
│ │ │
Н ОН СН3
6.Галогенирование: в присутствии PCl5, SOCl2 или HCl СН3–СН2 –ОН+SOCl2→СН3 –СН2–Cl+SO2+ HCl
6. Получение: а) СН3 – СН=СН2 + НОН → СН3 – С (СН3)Н — ОН (из алкенов);
б) R – Br + NaOH (раствор) → R – ОН + NaBr (щелочной гидролиз галогеналканов); в) R – СНО + 2[Н] → R — СН2 – ОН (из альдегидов); г) С≡О + 2Н2 (t, p, ZnO) → СН3ОН (из синтез-газа);
д) С6Н12О6 (брожение) → С2Н5ОН + 2СО2↑.
7. качественные реакции на: а) предельные одноатомные спирты – CuO, t
С2Н5ОН + CuO → СН3 – СНО + Cu + Н2О
б) предельные многоатомные спирты – Cu (ОН)2, свежеприготовленный раствор
2 СН2 – ОН + Cu (OН)2 → (СН2 – О)2Cu + 2 Н2О
│ │
СН2 – ОН СН2 – ОН – ярко-синий раствор.
2. Ароматические спирты – фенолы (циклические, непредельные). Общая формула – R-(ОН)m или СпН2п-6-m(ОH)m, М (СпН2п-6-m(ОН)m)= (14п-6 +16m) г/моль, SP2 – гибридизация
1. подвижность атома водорода и выраженные кислотные свойства –
а) реакции с Ме: С6Н5ОН + К → С6Н5ОК + 0,5Н2 ↑;
б) реакции со щелочами: С6Н5ОН + КОН → С6Н5ОК + НОН;
в) реакция с р-ром карбоната натрия (фенол в нём растворяется, но в отличие от обычных кислот не образует диоксида углерода): С6Н5ОН(aq) + CO32-(aq) −→ C6H5O—(aq) + HCO3—(aq)
2. реакции с хлор-альдегидом: С6Н5ОН + СН3ССlO → С6Н5 – О – C(CH3)O + HCl;
3. р. электрофильного замещения протекают легче, чем у аренов:
С6Н5ОН + СН3 – С = О −→С6Н5 – О – С = О + НСl
│ │
Cl СН3
а) реакция с раствором бромной воды – 1-я качественная реакция на фенолы
С6Н5ОН + 3 Br2 → С6Н2(ОН)Br3↓ + 3НBr – 2,4,6 – трибромфенол (белая эмульсия)
б) реакция нитрования — С6Н5ОН + 3 НО – NO2 → С6Н2(ОН)(NO2)3 + 3 НОН
в присутствии Н2SO4 получается 2,4,6 – тринитрофенол,
в) получение фенолформальдегидной смолы – р. поликонденсации
С6Н5ОН (фенол) + НСНО (формальдегид) →С6Н4(ОН) – СН2ОН — 1-я стадия;
n С6Н4(ОН) – СН2ОН + n С6Н5ОН →( С6Н4(ОН) – СН2 – С6Н4(ОН))n + n НОН.
4. реакция с раствором FeCl3 – 2-я качественная реакция на фенолы
3 C6Н5ОН + FeCl3 → (С6Н5О-)3Fe + 3НCl (ярко-фиолетовый раствор).
4. Получение: а) из каменноугольной смолы; б) С6Н5 Br + КОН → С6Н5ОН + КBr
в) С6Н5 – СН (СН3)2 + 2 [О] → С6Н5 – ОН + (СН3)2СО.
3. Альдегиды. Общая формула – R-С = О или СпН2п О.Мr (СпН2пО) =(14п+16)
│
Н SP2 – гибридизация
1.Реакции нуклеофильного присоединения:а) R – СНО + НСN −KCN→ R – CH(OH) – C ≡ N;
б) R – СНО + R‘OH −H+→ R – CH – OH −R‘OH→ R – CH — OR‘ + H2O
│ │
OR‘ (полуацеталь) OR‘ (ацеталь);
╔O ╔O
в) R – СНО + NaHSO3 (:S – ONa) → R – CH – S — ONa
│ │ O╝
OH OH
г) р. восстановления R – СНО + H2 −LiAlH4→ R – CH2 – OH
Внимание: водород легко присоединяется по связи С=С и очень трудно – по связи С=О. LiAlH4 восстанавливает связи С=О до С – ОН, не затрагивая связь С=С.
О ← ОН
║ │ │
СН3 – С – Н + Н – О – СН3 → СН3 – СН – О – СН3, LiAlH4 — алюмогидрид лития.
2. Окисление: легко окисляются в кислоты – качественные реакции на альдегиды – реакции «серебряного» и «медного» зеркала а) R – CHO + 2 [Aq(NH3)2]OH → R – COO – NH4 +2Aq↓+2NH3↑ + H2O:
реактив [Aq(NH3)2]OH – реактив Толленса б) R – CHO + 2 Cu(OH)2 → R – COOH + Cu2O↓ +2H2O:
реактив Cu(OH)2 – реактив Фелинга или упрощённо — R – CHO + [О] → R – CОOН
3. Получение: а) из спиртов R–СН2-ОН + CuО −t→ R–СНО + Н2О + Cu
б) из дигалогензамещённых алканов: R – CHCl2 + 2 NaОН → R – CHO + 2 NaCl + Н2О
4. Кетоны. Общая формула – R-С = О или СпН2п О. Мr (СпН2пО) =(14п+16)
│
R SP2 – гибридизация
1. Химические свойства отличаются от свойств альдегидов:
а) менее активны в реакциях нуклеофильного присоединения, чем альдегиды (с цианидом водорода в присутствии цианида калия) R – С=О + НСN −KCN→ R – C (OH) – C ≡ N;
│ │
R R
б) присоединение реактива Гриньяра – R – MqBr с образованием третичного спирта
R – С=О + R – MqBr −2HCl→ R – C (OH) – R + MqCl2 + HBr
│ │
R R
в) гидрирование кетонов с образованием вторичных спиртов R – С=О + Н2− → R – CН (OH)
│ │
R R
г) окисление с трудом, не взаимодействуют с соединениями серебра и меди
2. Иодоформный тест – если карбонильная группа связана со 2-ым атомом углерода от конца углеродной цепи (со щелочным раствором иода)
СН3 – СО – R + I2 −OH—→ R – COO—(aq) + CHI3(тв), жёлтый осадок, такой же, как и для CH3 – CH (OH)R.
5. Карбоновые кислоты. Общая формула – R-С = О или СпН2пО.
│
Мr (СпН2пО) =(14п+16) ОН SP2 – гибридизация
1. Диссоциируют, т.е. являются донором катиона водорода – слабые электролиты, самая сильная из них – муравьиная НСООН
R – СООН ↔ R – СОО— + Н+, сл-но, характерны свойства, типичные для кислот – взаимодействие с Ме, основными оксидами, основаниями и солями слабых кислот.
2. р.замещения группы ОН на хлор, взаимодействие с хлоридом Р(V)
R – СООН + РСl5 → R – С = О + POCl3 + HCl
│
Сl
3.межмолекулярная дегидратация в присутствии Р2О5 или НРО3
R – СООН + Н – О – СО – R — Р2О5→ R – СО – О – СО — R + Н2О (ангидрид к-ты),
4. р. этерификации – образование сложных эфиров в присутствии Н2SO4
R – СООН + Н — О R′ − Н2SO4→ R – СО — О R′ + Н2О
остаток кислоты ↓ остаток спирта
5. получение амидов в реакциях с раствором аммиака, при нагревании
R – С = О + NH3 −t→ R – С = О + H2O
│ │
ОН NH2
6. р. замещения атома водорода у α–атома (С) на атом брома, в присутствии Ркр
СН3 – СН2 – СООН + Br2 − Ркр→ CH3 – CHBr – COOH + HBr;
7. р. дегидратации и гидрирование, в присутствии LiAlH4 (см. «альдегиды»)
R – С = О + 2 Н2 −LiAlH4→ R – СН2ОН + Н2О т.е. восстановление до спиртов.
│
ОН
8.Внимание: муравьиная кислота – самая сильная из органических кислот и сильный восстановитель,
а) НСООН − Н2SO4→ СО2↑ + Н2О;
б) р. «зеркала» НСООН + 2 [Ag(NH3)2]OH −t→ 2 Ag↓ + (NH4)2CO3 + 2NH3 + H2O
или упрощенно НСООН + Ag2О −t→ 2Ag↓ + СО2↑ + Н2О;
в) НСООН + Cl2 → CO2↑ + 2HCl
9. Получение: а) из спиртов (окисление, т.е. + [О])
R – СН2 – ОН + [О] → R – СНО (альдегид) и дальше + [О] → R – СООН (кислота);
б) из альдегидов – р. «серебряного и медного зеркала»
R – СНО + [Ag(NH3)2]OH −t→ Ag↓ + R – СООNН4 + Н2О + NH3
б) из реактива Гриньяра (R – MgBr) – р. элиминирования и гидратации (последовательное взаимодействие с СО2 и Н2О): R – MgBr + CO2 → R – COO – MgBr…….. + H2O → R –COOH +Mg (OH) Br
в) из трихлорзамещенного алкана (последовательное замещение атомов хлора на группы ОН из щелочей и дегидратация) R – С (Cl)3 + 2 NaOH → 3NaCl + R – C(OH)3….→ R – COOH + H2O
R – C (OH)3 – трёхатомный спирт – вещество очень слабое и нестабильное.
6. Сложные эфиры карбоновых кислот. Общая формула – R-С = О
│
О R′ Мr (СпН2п+1СОО)(СпН2п+1)′ = (14п+46)
1. р. гидролиза: а) кислотного СН3СООСН3 + НОН −H+→ СН3СООН + НОСН3
(кислота) (спирт)
б) щелочного СН3СООСН3 + NaOH → СН3СООNa + СН3ОН
р. гидролиза с Н2О идёт медленно, её катализируют (ускоряют) кислоты и щёлочи
2. р. восстановления, в присутствии LiAlH4 с образованием 2-х спиртов:
R – СОО — R′ + 4 [Н+] −LiAlH4→ R – CH2 – OH + R′ОН (аналогично альдегидам);
3. Получение: а) р. этерификации R – СООН + НО R′ − Н2SO4↔ R – СОО — R′ + Н2О
особенность: медленная реакция, обратимая, с низким выходом.
б) р. ацилирования спирта хлоридом кислоты СН3СОCl + НОСН2СН3 → СН3СООСН2СН3 + HCl (р. быстрая, хороший выход).
Хлорангидриды и ангидриды кислот
Эти два вида производных карбоновых кислот химически очень активны. Хлорангидриды даже более активны, чем ангидриды, и более летучи, что делает обращение с ними очень трудным. Они вступают в быструю реакцию на холоде с водой, аммиаком и с их производными, спиртами и аминами. В каждом случае атом водорода реагирующей молекулы замещается ацильной группой – это реакции ацилирования, а хлорангидриды и ангидриды кислот-ацилирующие агенты. С хлорангидридами:
а) вода: СН3СОCl + НОН → СН3СО – ОН (кислота) + HCl;
б) спирт: СН3СОCl + НОСН2СН3 → СН3СО – ОСН2СН3 (эфир) + HCl;
в) аммиак: СН3СОCl + 2Н−NH2 → СН3СО – NH2 (амид) + NH4Cl;
г) амин: СН3СОCl + НNHСН3 → СН3СО – NHСН3 (замещ. амид) + HCl;
↑ этот атом водорода замещается на ацильную группу.
С ангидридами кислот:
а) вода: СН3СОООССН3 + НОН → СН3СО – ОН + СН3СООН;
б) спирт: СН3СОООССН3 + НОСН2СН3 → СН3СО – ОСН2СН3 + СН3СООН;
в) аммиак: СН3СОООCСН3 + Н−NH2 → СН3СО – NH2 + СН3СООН;
г) амин: СН3СОООCН3 + НNHСН3 → СН3СО – NHСН3 + СН3СООН.
7. Углеводы. Общая формула – Сn (Н2О)m. Mr = 12n + 18m.
1. Глюкоза – альдегидоспирт СН2ОН – (СНОН)4 — СНО, т.е. имеет р. «зеркала»
СН2ОН – (СНОН)4 – СНО + 2 [Ag(NH3)2]OH −t→ СН2ОН – (СНОН)4 – СОО — NH4 + 3NH3 + H2O +2 Ag↓
2. р. восстановления до многоатомных спиртов:
СН2ОН – (СНОН)4 – СНО + 2[Н] → СН2ОН – (СНОН)4 – СН2ОН (сорбит);
3. синее окрашивание с Си(ОН)2, как у многоатомных спиртов;
4. р. межмолекулярной дегидратации со спиртами: → простые эфиры;
5. р. этерификации с альдегидами → сложные эфиры;
6. брожение: С6Н12О6 −дрожжи→ 2 С2Н5ОН + 2 СО2↑ — спиртовое брожение;
С6Н12О6 −→ 2 СН3 – СН (ОН) – СООН — молочнокислое брожение.
8. Азотсодержащие соединения – амины. Общая формула – R— NH2,
R – NH – R или N(R)3. Мr (R— NH2) = (14п+17)
1. Амины обладают основными свойствами, поэтому, как основания,
а) реагируют с водой: R— N:H2 + Н2О ↔ [R— NH3]+ ОН−
б) реагируют с кислотами: R— N:H2 + Нδ+Cl δ- ↔ [R— NH3]+ Cl−
2. Реакция горения: 4 С2Н5 + N:H2 + 15О2 → 8СО2↑ + 2N2↑ + 14Н2О.
3. Р. нитрирования (с НО – NО) проходит по-разному:
а) у первичных аминов: R— NH2 + НО – NО (NaNO2 + HCl) → R – OH + N2↑ + NaCl + H2O;
б) у вторичных аминов:R2 – NH + НО – NО (NaNO2 + HCl) → R2N – N=O + NaCl + H2O.
4. Анилин – ароматический амин с формулой С6Н5 — NH2
в реакции нитрирования: С6Н5 — NH2 + НО – NО (NaNO2 + HCl) → [С6Н5 — N≡N]+Cl− + NaCl + 2H2O;
5. Качественная реакция на анилин –реакция с раствором брома:С6Н5 — NH2+3Br2 → C6H2Br3NH2↓+3 HBr
6. Получение аминов: а)NH3+CH3Cl −t→ CH3–NH2 + HCl; б) R–NO2+4[H]−LiAlH4→R –NH2 + 2H2O
7. Получение анилина: C6H5 – NO2 + 6 [H] −Fe + HCl→ C6H5 – NH2 + 2H2O
9. Азотсодержащие соединения – аминокислоты …β α Мr (к-ты) = (14п+75)
Общая формула – R – СН — СООН
│
NH2
1.Аминокислоты обладают амфотерными свойствами, поэтому реагируют:
а) с кислотами H2N – CH2 – COOH + HCl → Cl [NH3 – CH2 — COOH];
б) c щелочами H2N – CH2 – COOH + NaOH → NH2 – CH2 – COONa + H2O.
2. Р. этерификации – взаимодействие со спиртами:H2N –CH2 –COOH +С2Н5OH−H+→H2N –CH2 – COO – С2Н5 + Н2О
3. Р. поликонденсации — взаимодействие кислот между собой с образованием пептидов: пептидная связь H2N – CH2 – COOH + H—N – CH2 – COOH → H2N – CH2 – CO—N – CH2 – COOH
│ Дипептид │
Н Н
4. Получение: α- аминокислоты из α-хлорзамещенных карбоновых кислот
R – СН – СООН + 2 H3N → R – СН – СООН + NH4 Cl
│ │
Cl NH2
Окислительно – восстановительные реакции в органической химии.
А. Углеводороды.
1. СН2 = СН – СН2 – СН3 + КМпО4 + Н2О → СН2 – СН – СН2 – СН3 + МпО2 + КОН
│ │
ОН ОН
2. С6Н5 – СН2 – СН3 + КМпО4 + Н2SО4 → С6Н5СOOН + MnSO4 + K2SO4 + CO2 + H2O
3. СН2 = СН – СН2 – СН3 + КМпО4+ Н2SО4 → HCOOH + CH3COOH + MnSO4 + K2SO4 + H2O
4. CH ≡ CH + КМпО4 + Н2О → H2C2O4 + MnO2 + KOH
5. С6Н5 – СН3 + КМпО4 + Н2SО4 → С6Н5СOOН + MnSO4 + K2SO4 + H2O
Органика. Учимся составлять и читать химические уравнения в органической химии.
Смотреть видео:
Свежая информация для ЕГЭ и ОГЭ по Химии (листай):
С этим видео ученики смотрят следующие ролики:

Учимся составлять уравнения для задачи 33 егэ химия 2022 часть1
Видеоуроки по химии

Учимся составлять уравнения реакций для задачи 33 егэ химия часть 2
Видеоуроки по химии

Как составлять химические уравнения
Oksana Antares

Химические уравнения. Как составлять химические уравнения.
Oksana Antares
Облегчи жизнь другим ученикам — поделись! (плюс тебе в карму):
24.09.2019
- Комментарии
RSS
Написать комментарий
Нет комментариев. Ваш будет первым!
Ваше имя:
Загрузка…
Химические реакции в органической химии
Существуют разные системы классификации органических реакций, которые основаны на различных признаках. Среди них можно выделить классификации:
-
по конечному результату реакции, то есть изменению в структуре субстрата;
-
по механизму протекания реакции, то есть по типу разрыва связей и типу реагентов.
Взаимодействующие в органической реакции вещества подразделяют на реагент и субстрат. При этом считается, что реагент атакует субстрат.
ОПРЕДЕЛЕНИЕ
Реагент — вещество, действующее на объект — субстрат — и вызывающее в нем изменение химической связи. Реагенты делятся на радикальные, электрофильные и нуклеофильные.
ОПРЕДЕЛЕНИЕ
Субстратом, как правило, считают молекулу, которая предоставляет атом углерода для новой связи.
КЛАССИФИКАЦИЯ РЕАКЦИЙ ПО КОНЕЧНОМУ РЕЗУЛЬТАТУ (ИЗМЕНЕНИЮ В СТРУКТУРЕ СУБСТРАТА)
КЛАССИФИКАЦИЯ РЕАКЦИЙ ПО КОНЕЧНОМУ РЕЗУЛЬТАТУ (ИЗМЕНЕНИЮ В СТРУКТУРЕ СУБСТРАТА)
В органической химии различают четыре вида реакций по конечному результату и изменению в структуре субстрата: присоединения, замещения, отщепления, или элиминирования (от англ. to eliminate — удалять, отщеплять), и перегруппировки (изомеризации). Такая классификация аналогична классификации реакций в неорганической химии по числу исходных реагентов и образующихся веществ, с изменением или без изменения состава. Классификация по конечному результату основана на формальных признаках, так как стехиометрическое уравнение, как правило, не отражает механизм реакции. Сравним типы реакций в неорганической и органической химии.
Тип реакции в неорганической химии
1. Соединение
Тип реакции в органической химии
Присоединение по кратным связям
Элиминирование
Замещение
частный случай — этерификация
Изомеризация
Разновидность
и пример
реакции
Гидрирование
2. Разложение
3. Замещение
4. Обмен (частный случай — нейтрализация)
5.Аллотропизация
Zn+2HCl=ZnCl2+H2
H2SO4+2NaOH=Na2SO4+2H2O
графит⇔ алмаз
Pкрасн.⇔P бел.Pкрасн.⇔P бел.
Sромб.⇔Sпласт.Sромб.⇔Sпласт.
п) без замены их другими.
В зависимости от того, какие атомы отщепляются — соседние C–C или изолированные двумя-тремя или более атомами углерода –C–C–C–C–, –C–C–C–C–C–, могут образовываться соединения с кратными связями или циклические соединения. Отщепление галогеноводородов из алкилгалогенидов либо воды из спиртов происходит по правилу Зайцева.
ОПРЕДЕЛЕНИЕ
Правило Зайцева: атом водорода Н отщепляется от наименее гидрогенизированного атома углерода.
Например, отщепление молекулы бромоводорода происходит от соседних атомов в присутствии щелочи, при этом образуется бромид натрия и вода.
ОПРЕДЕЛЕНИЕ
Перегруппировка — химическая реакция, в результате которой происходит изменение взаимного расположения атомов в молекуле, перемещение кратных связей или изменение их кратности.
Перегруппировка может осуществляться с сохранением атомного состава молекулы (изомеризация) или с его изменением.
ОПРЕДЕЛЕНИЕ
Изомеризация — частный случай реакции перегруппировки, приводящая к превращению химического соединения в изомер путем структурного изменения углеродного скелета.
Перегруппировка тоже может осуществляться по гомолитическому или гетеролитическому механизму. Молекулярные перегруппировки могут классифицироваться по разным признакам, например по насыщенности систем, по природе мигрирующей группы, по стереоспецифичности и др. Многие реакции перегруппировки имеют специфические названия — перегруппировка Кляйзена, перегруппировка Бекмана и др.
Реакции изомеризации широко используются в промышленных процессах, например при переработке нефти для повышения октанового числа бензина. Примером изомеризации является превращение н-октана в изооктан:
КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ РЕАКЦИЙ ПО ТИПУ РЕАГЕНТА
КЛАССИФИКАЦИЯ ОРГАНИЧЕСКИХ РЕАКЦИЙ ПО ТИПУ РЕАГЕНТА
Разрыв связи в органических соединениях может гомолитическим и гетеролитическим.
ОПРЕДЕЛЕНИЕ
Гомолитический разрыв связи — это такой разрыв, в результате которого каждый атом получает неспаренный электрон и образуются две частицы, имеющие сходное электронное строение — свободные радикалы.
Гомолитический разрыв характерен для неполярных или слабополярных связей, например C–C, Cl–Cl, C–H, и требует большого количества энергии.
Образующиеся радикалы, имеющие неспаренный электрон, обладают высокой реакционной способностью, поэтому химические процессы, протекающие с участием таких частиц, часто носят «цепной» характер, их трудно контролировать, а в результате реакции получается набор продуктов замещения. Так, при хлорировании метана продуктами замещения являются хлорметан CH3ClCH3Cl, дихлорметан CH2Cl2CH2Cl2, хлороформ CHCl3CHCl3 и четыреххлористый углерод CCl4CCl4. Реакции с участием свободных радикалов протекают по обменному механизму образования химических связей.
Образующиеся в ходе такого разрыва связи радикалы обуславливают радикальный механизм протекания реакции. Радикальные реакции обычно протекают при повышенных температурах или при излучении (например, свет).
В силу своей высокой реакционной способности свободные радикалы могут оказывать негативное воздействие на организм человека, разрушая клеточные мембраны, воздействуя на ДНК и вызывая преждевременное старение. Эти процессы связаны, в первую очередь, с пероксидным окислением липидов, то есть разрушением структуры полиненасыщенных кислот, образующих жир внутри клеточной мембраны.
ОПРЕДЕЛЕНИЕ
Гетеролитический разрыв связи — это такой разрыв, при котором электронная пара остается у более электроотрицательного атома и образуются две заряженные частицы — ионы: катион (положительный) и анион (отрицательный).
В химических реакциях эти частицы выполняют функции «нуклеофилов» («фил» — от гр. любить) и «электрофилов», образуя химическую связь с партнером по реакции по донорно-акцепторному механизму. Частицы-нуклеофилы предоставляют электронную пару для образования новой связи. Другими словами,
ОПРЕДЕЛЕНИЕ
Нуклеофил — электроноизбыточный химический реагент, способный взаимодействовать с электронодефицитными соединениями.
Примерами нуклеофилов являются любые анионы (Cl−,I−,NO−3Cl−,I−,NO3− и др.), а также соединения, имеющие неподеленную электронную пару (NH3,H2ONH3,H2O).
Таким образом, при разрыве связи могут образоваться радикалы или нуклеофилы и электрофилы. Исходя из этого выделяют три механизма протекания органических реакций.
МЕХАНИЗМЫ ПРОТЕКАНИЯ ОРГАНИЧЕСКИХ РЕАКЦИЙ
МЕХАНИЗМЫ ПРОТЕКАНИЯ ОРГАНИЧЕСКИХ РЕАКЦИЙ
Свободно-радикальный механизм: реакцию начинают свободные радикалы, образующиеся при гомолитическом разрыве связи в молекуле.
Наиболее типичный вариант — образование радикалов хлора или брома при УФ-облучении.
1. Свободно-радикальное замещение
метан бромметан
Инициирование цепи
Рост цепи
2. Свободно-радикальное присоединение
этен полиэтилен
Электрофильный механизм: реакцию начинают частицы-электрофилы, получающие положительный заряд в результате гетеролитического разрыва связи. Все электрофилы — кислоты Льюиса.
Такие частицы активно образуются под действием кислот Льюиса, которые усиливают положительный заряд частицы. Чаще других используются AlCl3,FeCl3,FeBr3,ZnCl2AlCl3,FeCl3,FeBr3,ZnCl2, выполняющие функции катализатора.
Местом атаки частицы-электрофила являются те участки молекулы, которые имеют повышенную электронную плотность, т. е. кратная связь и бензольное кольцо.
Общий вид реакций электрофильного замещения можно выразить уравнением:
1. Электрофильное замещение
бензол бромбензол
2. Электрофильное присоединение
пропин 1,2-дихлорпропен
Присоединение к несимметричным непредельным углеводородам происходит в соответствии с правилом Марковникова.
ОПРЕДЕЛЕНИЕ
Правило Марковникова: присоединение к несимметричным алкенам молекул сложных веществ с условной формулой НХ (где Х — это атом галогена или гидроксильная группа ОН–) атом водорода присоединяется к наиболее гидрогенизированному (содержащему больше всего атомов водорода) атому углерода при двойной связи, а Х — к наименее гидрогенизированному.
Например, присоединение хлороводорода HCl к молекуле пропена CH3–CH=CH2CH3–CH=CH2.
Реакция протекает по механизму электрофильного присоединения. За счет электронодонорного влияния CH3CH3-группы электронная плотность в молекуле субстрата смещена к центральному атому углерода (индуктивный эффект), а затем по системе двойных связей — к концевому атому углерода CH2CH2-группы (мезомерный эффект). Таким образом, избыточный отрицательный заряд локализован именно на этом атоме. Поэтому атаку начинает протон водорода H+H+, являющийся электрофильной частицей. Образуется положительно заряженный карбеновый ион [CH3–CH−CH3]+[CH3–CH−CH3]+, к которому присоединяется анион хлора Cl−Cl−.
ОПРЕДЕЛЕНИЕ
Исключения из правила Марковникова: реакция присоединения протекает против правила Марковникова, если в реакцию вступают соединения, у которых атом углерода, соседний с атомом углерода двойной связи, оттягивает на себя частично электронную плотность, то есть при наличии заместителей, проявляющих значительный электроноакцепторный эффект (–CCl3,–CN,–COOH(–CCl3,–CN,–COOH и др.).
Нуклеофильный механизм: реакцию начинают частицы-нуклеофилы, имеющие отрицательный заряд, образовавшиеся в результате гетеролитического разрыва связи. Все нуклеофилы — основания Льюиса.
В нуклеофильных реакциях реагент (нуклеофил) имеет на одном из атомов свободную пару электронов и является нейтральной молекулой или анионом (Hal–,OH–,RO−,RS–,RCOO–,R–,CN–,H2O,ROH,NH3,RNH2Hal–,OH–,RO−,RS–,RCOO–,R–,CN–,H2O,ROH,NH3,RNH2 и др.).
Нуклеофил атакует в субстрате атом с наименьшей электронной плотностью (т. е. с частичным или полным положительным зарядом). Первой стадией реакции нуклеофильного замещения является ионизация субстрата с образованием карбкатиона. При этом новая связь образуется за счет электронной пары нуклеофила, а старая претерпевает гетеролитический разрыв с последующим отщеплением катиона. Примером нуклеофильной реакции может служить нуклеофильное замещение (символ SNSN) у насыщенного атома углерода, например щелочной гидролиз бромпроизводных.
1. Нуклеофильное замещение
2. Нуклеофильное присоединение
этаналь циангидрин
ИСТОЧНИК HTTP://FOXFORD.RU/WIKI/HIMIYA