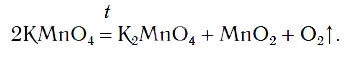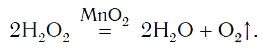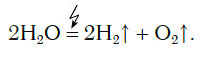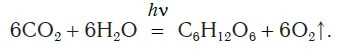В уроке 17 «Получение кислорода» из курса «Химия для чайников» выясним, как получают кислород в лабораторных условиях; узнаем, что такое катализатор, и как растения влияют на производство кислорода на нашей планете.
Наиболее важным для человека и других живых организмов веществом, входящим в состав воздуха, является кислород. Большие количества кислорода используются в промышленности, поэтому важно знать, как можно его получать.
Содержание
- Получение кислорода в лабораторных условиях
- Кислород в природе
- Получение кислорода и азота из воздуха
Получение кислорода в лабораторных условиях
В химической лаборатории кислород можно получать нагреванием некоторых сложных веществ, в состав которых входят атомы кислорода. К числу таких веществ относится вещество KMnO4, которое имеется в вашей домашней аптечке под названием «марганцовка».
Вы знакомы с простейшими приборами для получения газов. Если в один из таких приборов поместить немного порошка KMnO4 и нагреть, то будет выделяться кислород (рис. 76):
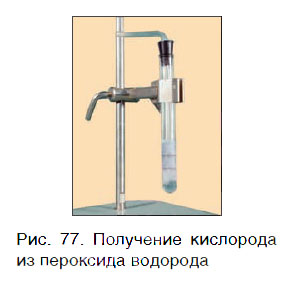
Кислород можно также получить разложением пероксида водорода H2O2. Для этого в пробирку с H2O2 следует добавить очень небольшое количество особого вещества — катализатора — и закрыть пробирку пробкой с газоотводной трубкой (рис. 77).
Для данной реакции катализатором является вещество, формула которого MnO2. При этом протекает следующая химическая реакция:
Обратите внимание на то, что ни в левой, ни в правой частях уравнения формулы катализатора нет. Его формулу принято записывать в уравнении реакции над знаком равенства. Для чего же добавляется катализатор? Процесс разложения H2O2 при комнатных условиях протекает очень медленно. Поэтому для получения заметных количеств кислорода необходимо много времени. Однако эту реакцию можно резко ускорить путем прибавления катализатора.
Катализатор — это вещество, которое ускоряет химическую реакцию, но само в ней не расходуется.
Именно потому, что катализатор не расходуется в реакции, мы не записываем его формулу ни в одной из частей уравнения реакции.
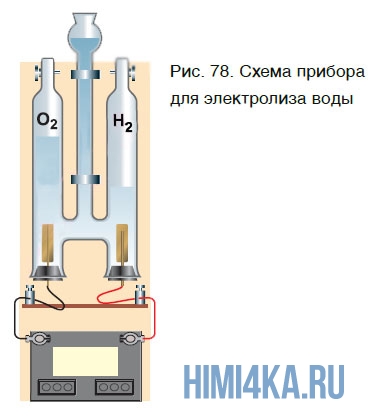
Еще один способ получения кислорода — разложение воды под действием постоянного электрического тока. Этот процесс называется электролизом воды. Получить кислород можно в приборе, схематично изображенном на рисунке 78.
При этом протекает следующая химическая реакция:
Кислород в природе
Огромное количество газообразного кислорода содержится в атмосфере, растворено в водах морей и океанов. Кислород необходим всем живым организмам для дыхания. Без кислорода невозможно было бы получать энергию за счет сжигания различных видов топлива. На эти нужды ежегодно расходуется примерно 2% атмосферного кислорода.
Откуда берется кислород на Земле и почему его количество остается примерно постоянным, несмотря на такой расход? Единственным источником кислорода на нашей планете являются зеленые растения, производящие его под действием солнечного света в процессе фотосинтеза. Это очень сложный процесс, включающий много стадий. В результате фотосинтеза в зеленых частях растений углекислый газ и вода превращаются в глюкозу C6H12O6 и кислород. Суммарное
уравнение реакций, протекающих в процессе фотосинтеза, можно представить следующим образом:
Установлено, что примерно одну десятую часть (11%) производимого зелеными растениями кислорода дают наземные растения, а остальные девять десятых (89%) — водные растения.
Получение кислорода и азота из воздуха
Огромные запасы кислорода в атмосфере позволяют получать и использовать его в различных производствах. В промышленных условиях кислород, азот и некоторые другие газы (аргон, неон) получают из воздуха.
Для этого воздух сначала превращают в жидкость (рис. 79) путем охлаждения до такой низкой температуры, при которой все его компоненты переходят в жидкое агрегатное состояние.
Затем эту жидкость медленно нагревают, в результате чего при разных температурах происходит последовательное выкипание (т. е. переход в газообразное состояние) веществ, которые содержатся в воздухе. Собирая выкипающие при разных температурах газы, по отдельности получают азот, кислород и другие вещества.
Краткие выводы урока:
- В лабораторных условиях кислород получают разложением некоторых сложных веществ, в состав которых входят атомы кислорода.
- Катализатор — вещество, которое ускоряет протекание химической реакции, но само при этом не расходуется.
- Источником кислорода на нашей планете являются зеленые растения, в которых протекает процесс фотосинтеза.
- В промышленности кислород получают из воздуха.
Надеюсь урок 17 «Получение кислорода» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Здравствуйте. Вы уже читали мои статьи в блоге Tutoronline.ru. Сегодня я расскажу Вам о кислороде и о способах его получения. Напоминаю, если у Вас будут ко мне вопросы, Вы можете писать их в комментариях к статье. Если же Вам понадобиться любая помощь по химии, записывайтесь на мои занятия в расписании. Буду рад Вам помочь.
Кислород распространён в природе в виде изотопов 16О, 17О, 18О, которые имеют следующее процентное содержание на Земле – 99,76%, 0,048%, 0,192% соответственно.
В свободном состоянии кислород находится в виде трёх алло-тропных модификаций: атомарного кислорода — Оо , дикислорода – О2 и озона – О3. Причём, атомарный кислород может быть получен следующим образом:
КClO3 = KCl + 3O0
KNO3 = KNO2 + O0
Кислород входит в состав более 1400 различных минералов и органических веществ, в атмосфере его содержание составляет 21% по объёму. А в человеческом теле содержится до 65% кислорода. Кислород газ без цвета и запаха, мало растворим в воде (в 100 объёмах воды при 20оС растворяется 3 объёма кислорода).
В лаборатории кислород получают умеренным нагреванием некоторых веществ:
1) При разложении соединений марганца (+7) и (+4):
2KMnO4 → K2MnO4 + MnO2 + O2
перманганат манганат
калия калия
2MnO2 → 2MnO + O2
2) При разложении перхлоратов:
2KClO4 → KClO2 + KCl + 3O2
перхлорат
калия
3) При разложении бертолетовой соли (хлората калия).
При этом образуется атомарный кислород:
2KClO3 → 2 KCl + 6O0
хлорат
калия
4) При разложении на свету солей хлорноватистой кислоты — гипохлоритов:
2NaClO → 2NaCl + O2
Ca(ClO)2 → CaCl2 + O2
5) При нагревании нитратов.
При этом образуется атомарный кислород. В зависимости от того, какое положение в ряду активности занимает металл нитрата, образуются различные продукты реакции:
2NaNO3 → 2NaNO2 + O2
Ca(NO3)2 → CaO + 2NO2 + O2
2AgNO3 → 2 Ag + 2NO2 + O2
6) При разложении пероксидов:
2H2O2 ↔ 2H2O + O2
7) При нагревании оксидов неактивных металлов:
2Аg2O ↔ 4Аg + O2
Данный процесс имеет актуальное значение в быту. Дело в том, что посуда, изготовленная из меди или серебра, имея естественный слой оксидной плёнки, при нагревании образует активный кислород, что является антибактериальным эффектом. Растворение солей неактивных металлов, особенно нитратов, также приводит к образованию кислорода. Например, суммарный процесс растворения нитрата серебра можно представить по этапам:
AgNO3 + H2O → AgOH + HNO3
2AgOH → Ag2O + O2
2Ag2O → 4Ag + O2
или в суммарном виде:
4AgNO3 + 2H2O → 4Ag + 4HNO3 + 7O2

4K2Cr2O7 → 4K2CrO4 + 2Cr2O3 + 3 O2
бихромат хромат
калия калия
В промышленности кислород получают:
1) Электролитическим разложением воды:
2Н2О → 2Н2 + О2
2) Взаимодействием углекислого газа с пероксидами:
СО2 + К2О2 →К2СО3 + О2
Данный способ представляет собой незаменимое техническое решение проблемы дыхания в изолированных системах: подводных лодках, шахтах, космических аппаратах.
3) При взаимодействии озона с восстановителями:
О3 + 2КJ + H2O → J2 + 2KOH + O2
2Н2О = 4е + 4Н + О2
Накопившиеся протоны способствуют синтезу АТФ:
АДФ + Ф = АТФ
В темновую фазу происходит преобразование углекислого газа и воды в глюкозу. И побочно выделяется кислород:
6СО2 + 6Н2О = С6Н12О6 + О2
© blog.tutoronline.ru,
при полном или частичном копировании материала ссылка на первоисточник обязательна.
Получение кислорода

4.9
Средняя оценка: 4.9
Всего получено оценок: 236.
4.9
Средняя оценка: 4.9
Всего получено оценок: 236.
Кислород появился в земной атмосфере с возникновением зелёных растений и фотосинтезирующих бактерий. Благодаря кислороду аэробными организмами осуществляется дыхание или окисление. Важно получение кислорода в промышленности – он используется в металлургии, медицине, авиации, народном хозяйстве и других отраслях.
Свойства
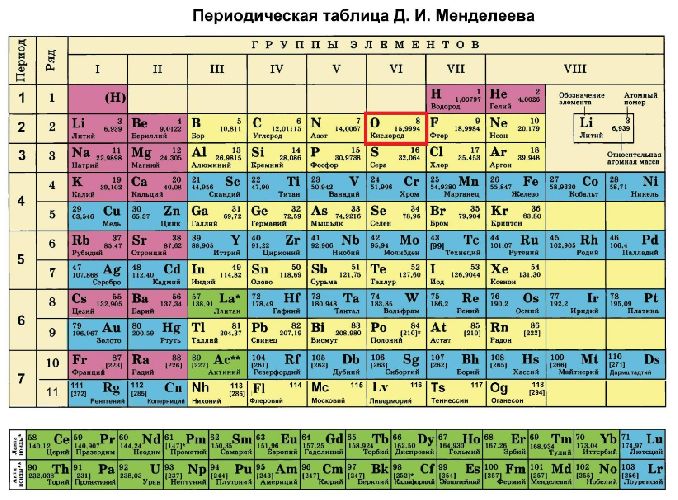
Кислород – восьмой элемент периодической таблицы Менделеева. Это газ, поддерживающий горение и осуществляющий окисление веществ.
Официально кислород был открыт в 1774 году. Английский химик Джозеф Пристли выделил элемент из оксида ртути:
2HgO → 2Hg + O2↑.
Однако Пристли не знал, что кислород является частью воздуха. Свойства и нахождение в атмосфере кислорода позже уставил коллега Пристли – французский химик Антуан Лавуазье.
Общая характеристика кислорода:
- бесцветный газ;
- не имеет запаха и вкуса;
- тяжелее воздуха;
- молекула состоит из двух атомов кислорода (О2);
- в жидком состоянии имеет бледно-голубой цвет;
- плохо растворим в воде;
- является сильным окислителем.
Присутствие кислорода легко проверить, опустив в сосуд с газом тлеющую лучину. При наличии кислорода лучина вспыхивает.
Как получают
Известно несколько способов получения кислорода из различных соединений в промышленных и лабораторных условиях. В промышленности кислород получают из воздуха путём его сжижения под давлением и при температуре в -183°С. Жидкий воздух подвергают испарению, т.е. постепенно нагревают. При -196°C азот начинает улетучиваться, а кислород сохраняет жидкое состояние.
В лаборатории кислород образуется из солей, пероксида водорода и в результате электролиза. Разложение солей происходит при нагревании. Например, хлорат калия или бертолетову соль нагревают до 500°С, а перманганат калия или марганцовку – до 240°С:
- 2KClO3 → 2KCl + 3O2↑;
- 2KMnO4 → K2MnO4 + MnO2 + O2↑.
Также можно получить кислород путём нагревания селитры или нитрата калия:
2KNO3 → 2KNO2 + O2↑.
При разложении пероксида водорода используется оксид марганца (IV) – MnO2, углерод или порошок железа в качестве катализатора. Общее уравнение выглядит следующим образом:
2Н2О2 → 2Н2О + О2↑.
Электролизу подвергается раствор гидроксида натрия. В результате образуется вода и кислород:
4NaOH → (электролиз) 4Na + 2H2O + O2↑.
Также кислород с помощью электролиза выделяют из воды, разложив её на водород и кислород:
2H2O → 2H2 + O2↑.
На атомных подводных лодках кислород получали из пироксида натрия – 2Na2O2 + 2CO2 → 2Na2CO3 + O2↑. Способ интересен тем, что вместе с выделением кислорода поглощается углекислый газ.
Как применяют
Собирание и распознавание необходимо для выделения чистого кислорода, использующегося в промышленности для окисления веществ, а также для поддержания дыхания в космосе, под водой, в задымлённых помещениях (кислород необходим пожарным). В медицине баллоны кислорода помогают дышать пациентам с затруднённым дыханием. Также кислород используется для лечения респираторных заболеваний.
Кислород применяют для сжигания топлива – угля, нефти, природного газа. Кислород широко применяется в металлургии и машиностроении, например, для плавки, резки и сварки металла.
Что мы узнали?
Кислород – бесцветный газ, необходимый для дыхания и используемый в промышленности. Кислород получают путём сжижения и испарения воздуха, электролизом воды или гидроксида натрия, выделяют из солей и пероксида водорода. Кислород используется для поддержания дыхания в местах с ограниченным запасом кислорода или его отсутствием, а также в промышленности для сжигания топлива и производства металла.
Тест по теме
Доска почёта

Чтобы попасть сюда — пройдите тест.
-
Томас Шелби
10/10
-
Лидия Маслова
10/10
-
Михаил Заричняк
5/10
-
Gordievich Igor
9/10
-
Владочка Дунина
9/10
Оценка доклада
4.9
Средняя оценка: 4.9
Всего получено оценок: 236.
А какая ваша оценка?
История открытия кислорода
Открытие кислорода ознаменовало новый период в развитии химии. С глубокой древности было известно, что для горения необходим воздух. Процесс горения веществ долгое время оставался непонятным. В эпоху алхимии широкое распространение получила теория флогистона, согласно которой вещества горят благодаря их взаимодействию с огненной материей, то есть с флогистоном, который содержится в пламени. Кислород был получен английским химиком Джозефом Пристли в 70-х годах XVIII века. Химик нагревал красный порошок оксида ртути (II), в итоге вещество разлагалось, с образованием металлической ртути и бесцветного газа:
2HgO t° → 2Hg + O2↑
Оксиды – бинарные соединения, в состав которых входит кислород При внесении тлеющей лучины в сосуд с газом она ярко вспыхивала. Ученый считал, что тлеющая лучина вносит в газ флогистон, и он загорается. Д. Пристли пробовал дышать полученным газом, и был восхищен тем, как легко и свободно им дышится. Тогда ученый и не предполагал, что удовольствие дышать этим газом предоставлено каждому. Результатами своих опытов Д. Пристли поделился с французским химиком Антуаном Лораном Лавуазье.
Имея хорошо оснащенную на то время лабораторию, А. Лавуазье повторил и усовершенствовал опыты Д. Пристли. А. Лавуазье измерил количество газа, выделяющееся при разложении определенной массы оксида ртути. Затем химик нагрел в герметичном сосуде металлическую ртуть до тех пор, пока она не превратилась в оксид ртути (II). Он обнаружил, что количество выделившегося газа в первом опыте равно газу, поглотившемуся во втором опыте. Следовательно, ртуть реагирует с каким-то веществом, содержащимся в воздухе. И это же вещество выделяется при разложении оксида. Лавуазье первым сделал вывод, что флогистон здесь совершенно ни при чем, и горение тлеющей лучины вызывает именно неизвестный газ, который в последствии был назван кислородом. Открытие кислорода ознаменовало крах теории флогистона!
Способы получения и собирания кислорода в лаборатории
Лабораторные способы получения кислорода весьма разнообразны. Существует много веществ, из которых можно получить кислород. Рассмотрим наиболее распространенные способы.
1) Разложение оксида ртути (II)
Одним из способов получения кислорода в лаборатории, является его получение по описанной выше реакции разложения оксида ртути (II). Ввиду высокой токсичности соединений ртути и паров самой ртути, данный способ используется крайне редко.
2) Разложение перманганата калия
Перманганат калия (в быту мы называем его марганцовкой) – кристаллическое вещество темно-фиолетового цвета. При нагревании перманганата калия выделяется кислород. В пробирку насыплем немного порошка перманганата калия и закрепим ее горизонтально в лапке штатива. Недалеко от отверстия пробирки поместим кусочек ваты. Закроем пробирку пробкой, в которую вставлена газоотводная трубка, конец которой опустим в сосуд- приемник. Газоотводная трубка должна доходить до дна сосуда-приемника. Ватка, находящаяся около отверстия пробирки нужна, чтобы предотвратить попадание частиц перманганата калия в сосуд-приемник (при разложении выделяющийся кислород увлекает за собой частички перманганата). Когда прибор собран, начинаем нагревание пробирки. Начинается выделение кислорода.
Уравнение реакции разложения перманганата калия:
2KMnO4 t° → K2MnO4 + MnO2 + O2↑
Как обнаружить присутствие кислорода? Воспользуемся способом Пристли. Подожжем деревянную лучину, дадим ей немного погореть, затем погасим, так, чтобы она едва тлела. Опустим тлеющую лучину в сосуд с кислородом. Лучина ярко вспыхивает! Газоотводная трубка была не случайно опущена до дна сосуда-приемника. Кислород тяжелее воздуха, следовательно, он будет собираться в нижней части приемника, вытесняя из него воздух. Кислород можно собрать и методом вытеснения воды. Для этого газоотводную трубку необходимо опустить в пробирку, заполненную водой, и опущенную в кристаллизатор с водой вниз отверстием. При поступлении кислорода газ вытесняет воду из пробирки.
Разложение пероксида водорода
Пероксид водорода – вещество всем известное. В аптеке оно продается под названием «перекись водорода». Данное название является устаревшим, более правильно использовать термин «пероксид». Химическая формула пероксида водорода Н2О2 Пероксид водорода при хранении медленно разлагается на воду и кислород. Чтобы ускорить процесс разложения можно произвести нагрев или применить катализатор.
Катализатор – вещество, ускоряющее скорость протекания химической реакции
Нальем в колбу пероксид водорода, внесем в жидкость катализатор. Катализатором может служить порошок черного цвета – оксид марганца MnO2. Тотчас смесь начнет вспениваться вследствие выделения большого количества кислорода. Внесем в колбу тлеющую лучину – она ярко вспыхивает. Уравнение реакции разложения пероксида водорода:
2H2O2 MnO2 → 2H2O + O2↑
Обратите внимание: катализатор, ускоряющий протекание реакции, записывается над стрелкой, или знаком «=», потому что он не расходуется в ходе реакции, а только ускоряет ее.
Разложение хлората калия
Хлорат калия – кристаллическое вещество белого цвета. Используется в производстве фейерверков и других различных пиротехнических изделий. Встречается тривиальное название этого вещества – «бертолетова соль». Такое название вещество получило в честь французского химика, впервые синтезировавшего его, – Клода Луи Бертолле. Химическая формула хлората калия KСlO3. При нагревании хлората калия в присутствии катализатора – оксида марганца MnO2, бертолетова соль разлагается по следующей схеме:
2KClO3 t°, MnO2 → 2KCl + 3O2↑.
Разложение нитратов
Нитраты – вещества, содержащие в своем составе ионы NO3⎺. Соединения данного класса используются в качестве минеральных удобрений, входят в состав пиротехнических изделий.
Нитраты – соединения термически нестойкие, и при нагревании разлагаются с выделением кислорода:
Обратите внимание, что все рассмотренные способы получения кислорода схожи. Во всех случаях кислород выделяется при разложении более сложных веществ.
Реакция разложения – реакция, в результате которой сложные вещества разлагаются на более простые В общем виде реакцию разложения можно описать буквенной схемой:
АВ → А + В.
Реакции разложения могут протекать при действии различных факторов. Это может быть нагревание, действие электрического тока, применение катализатора. Существуют реакции, в которых вещества разлагаются самопроизвольно.
Получение кислорода в промышленности
В промышленности кислород получают путем выделения его из воздуха.
Воздух – смесь газов, основные компоненты которой представлены в таблице.
Сущность этого способа заключается в глубоком охлаждении воздуха с превращением его в жидкость, что при нормальном атмосферном давлении может быть достигнуто при температуре около -192°С. Разделение жидкости на кислород и азот осуществляется путем использования разности температур их кипения, а именно: Ткип.
О2 = -183°С
N2 = -196°С (при нормальном атмосферном давлении).
При постепенном испарении жидкости в газообразную фазу в первую очередь будет переходить азот, имеющий более низкую температуру кипения, и, по мере его выделения, жидкость будет обогащаться кислородом. Многократное повторение этого процесса позволяет получить кислород и азот требуемой чистоты. Такой способ разделения жидкостей на составные части называется ректификацией жидкого воздуха.
Итог статьи:
- В лаборатории кислород получают реакциями разложения
- Реакция разложения – реакция, в результате которой сложные вещества разлагаются на более простые
- Кислород можно собрать методом вытеснения воздуха или методом вытеснения воды
- Для обнаружения кислорода используют тлеющую лучину, она ярко вспыхивает в нем
- Катализатор – вещество, ускоряющее химическую реакцию, но не расходующееся в ней
- В лаборатории кислород получают разложением некоторых кислородсодержащих веществ. Собирают его вытеснением воды или воздуха.
Разложение марганцовки (перманганата калия) при нагревании:
Рис. (1). Разложение перманганата калия
Разложение пероксида водорода в присутствии катализатора:
Рис. (2). Разложение пероксида
водорода
Электролиз воды:
Можно получить кислород и при разложении некоторых других веществ: бертолетовой соли
KClO3
, нитратов
NaNO3
,
KNO3
и т. д.
- В промышленных масштабах кислород получают из воздуха. Для этого воздух при повышенном давлении охлаждают и превращают в жидкость. Затем жидкий воздух нагревают. Сначала выделяется азот (температура кипения (–196) °С). Жидкий кислород остаётся, так как его температура кипения выше ((–183) °С). Хранят жидкий кислород в стальных баллонах голубого цвета.
Применение кислорода
- В металлургической промышленности кислород используется при выплавке чугуна и стали.
- В смеси с водородом или ацетиленом кислород применяется для резки и варки металлов.
- Находит применение кислород в качестве окислителя ракетного топлива.
- Используется он для обеспечения жизнедеятельности на подводных лодках и космических кораблях, при работе водолазов.
- Находит применение в медицине в лечебных целях.
Источники:
Рис. 1. Разложение перманганата калия © ЯКласс
Рис. 2. Разложение пероксида водорода © ЯКласс