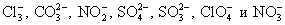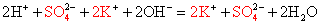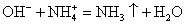Реакции ионного обмена – это реакции между сложными веществами в растворах, в результате которых реагирующие вещества обмениваются своими составными частями. Так как в этих реакциях происходит обмен ионами – они называются ионными.
Правило Бертолле: Реакции обмена в растворах электролитов протекают до конца (возможны) только тогда, когда в результате реакции образуется либо твердое малорастворимое вещество (осадок), либо газ, либо вода или любой другой слабый электролит.
Например, нитрат серебра взаимодействует с бромидом калия
AgNО3 + КВr = АgВr↓ + КNО3
Правила составления уравнений реакций ионного обмена
1. Записываем молекулярное уравнение реакции, не забывая расставить коэффициенты:
3KOH +FeCl3 = Fe(OH)3 + 3KCl
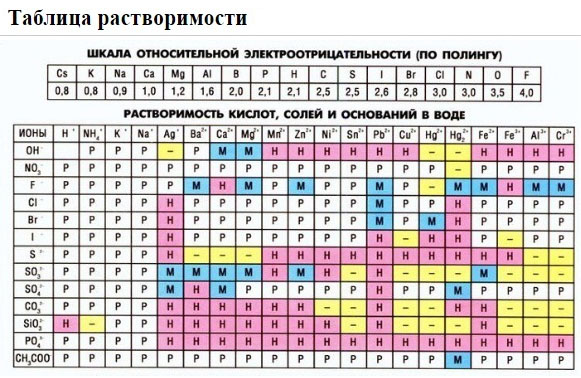
2. С помощью таблицы растворимости определяем растворимость каждого вещества. Подчеркнем вещества, которые мы не будем представлять в виде ионов.
р р н р
3KOH + FeCl3 = Fe(OH)3 + 3KCl
3. Составляем полное ионное уравнение. Сильные электролиты записываем в виде ионов, а слабые электролиты, малорастворимые вещества и газообразные вещества записываем в виде молекул.
3K+ + 3OH— + Fe3+ + 3Cl— = Fe(OH)3 + 3K+ + 3Cl—
4. Находим одинаковые ионы (они не приняли участия в реакции в левой и правой частях уравнения реакции) и сокращаем их слева и справа.
3K+ + 3OH— + Fe3+ + 3Cl— = Fe(OH)3 + 3K+ + 3Cl—
5. Составляем итоговое сокращенное ионное уравнение (выписываем формулы ионов или веществ, которые приняли участие в реакции).
Fe3+ + 3OH— = Fe(OH)3
На ионы мы не разбиваем:
- Оксиды; осадки; газы; воду; слабые электролиты (кислоты и основания)
- Анионы кислотных остатков кислых солей слабых кислот (НСО3—, Н2РО4— и т.п.) и катионы основных солей слабых оснований Al(OH)2+
- Комплексные катионы и анионы: [Al(OH)4]—
Например, взаимодействие сульфида цинка и серной кислоты
Составляем уравнение реакции и проверяем растворимость всех веществ. Сульфид цинка нерастворим.
н р р р
ZnS + H2SO4 = ZnSO4 + H2S
Реакция протекает до конца, т.к. выделяется газ сероводород, который является слабым электролитом. Полное ионно-молекулярное уравнение:
ZnS + 2H+ + SO42— = Zn2+ + SO42— + H2S
Сокращаем ионы, которые не изменились в процессе реакции – в данном случае это только сульфат-ионы, получаем сокращенное ионное уравнение:
ZnS + 2H+ = Zn2+ + H2S
Например, взаимодействие гидрокарбоната натрия и гидроксида натрия
Составляем уравнение реакции и проверяем растворимость всех веществ:
р р р
NaHCO3 + NaOH = Na2CO3 + H2O
Кислые анионы слабых кислот являются слабыми электролитами и на ионы не разбиваются:
Na+ + НСО3— + Na+ + ОН— = 2Na+ + CO32- + H2O
Сокращаем одинаковые ионы, получаем сокращенное ионное уравнение:
НСО3—+ ОН— = CO32- + H2O
Например, взаимодействие тетрагидроксоалюмината натрия и соляной кислоты
Составляем уравнение реакции и проверяем растворимость всех веществ:
р р р р
Na[Al(OH)4] + 4HCl = NaCl + AlCl3 + H2O
Комплексные ионы являются слабыми электролитами и на ионы не разбиваются:
Na+ + [Al(OH)4]— + 4H+ + 4Cl— = Na+ + Cl— + Al3+ + 3Cl— + H2O
Сокращаем одинаковые ионы, получаем сокращенное ионное уравнение:
[Al(OH)4]— + 4H+ = Al3+ + 4H2O
1.4.6. Реакции ионного обмена.
Реакции ионного обмена — реакции в водных растворах между электролитами, протекающие без изменений степеней окисления образующих их элементов.
Необходимым условием протекания реакции между электролитами (солями, кислотами и основаниями) является образование малодиссоциирующего вещества (вода, слабая кислота, гидроксид аммония), осадка или газа.
Расcмотрим реакцию, в результате которой образуется вода. К таким реакциям относятся все реакции между любой кислотой и любым основанием. Например, взаимодействие азотной кислоты с гидроксидом калия:
HNO3 + KOH = KNO3 + H2O (1)
Исходные вещества, т.е. азотная кислота и гидроксид калия, а также один из продуктов, а именно нитрат калия, являются сильными электролитами, т.е. в водном растворе они существуют практически только в виде ионов. Образовавшаяся вода относится к слабым электролитам, т.е. практически не распадается на ионы. Таким образом, более точно переписать уравнение выше можно, указав реальное состояние веществ в водном растворе, т.е. в виде ионов:
H+ + NO3− + K+ + OH‑ = K+ + NO3− + H2O (2)
Как можно заметить из уравнения (2), что до реакции, что после в растворе находятся ионы NO3− и K+ . Другими словами, по сути, нитрат-ионы и ионы калия никак не участвовали в реакции. Реакция произошла только благодаря объединению частиц H+ и OH− в молекулы воды. Таким образом, произведя алгебраически сокращение одинаковых ионов в уравнении (2):
H+ + NO3− + K+ + OH‑ = K+ + NO3− + H2O
мы получим:
H+ + OH‑ = H2O (3)
Уравнения вида (3) называют сокращенными ионными уравнениями, вида (2) — полными ионными уравнениями, а вида (1) — молекулярными уравнениями реакций.
Фактически ионное уравнение реакции максимально отражает ее суть, именно то, благодаря чему становится возможным ее протекание. Следует отметить, что одному сокращенному ионному уравнению могут соответствовать множество различных реакций. Действительно, если взять, к примеру, не азотную кислоту, а соляную, а вместо гидроксида калия использовать, скажем, гидроксид бария, мы имеем следующее молекулярное уравнение реакции:
2HCl+ Ba(OH)2 = BaCl2 + 2H2O
Соляная кислота, гидроксид бария и хлорид бария являются сильными электролитами, то есть существуют в растворе преимущественно в виде ионов. Вода, как уже обсуждалось выше, – слабый электролит, то есть существует в растворе практически только в виде молекул. Таким образом, полное ионное уравнение данной реакции будет выглядеть следующим образом:
2H+ + 2Cl− + Ba2+ + 2OH− = Ba2+ + 2Cl− + 2H2O
Сократим одинаковые ионы слева и справа и получим:
2H+ + 2OH− = 2H2O
Разделив и левую и правую часть на 2, получим:
H+ + OH− = H2O,
Полученное сокращенное ионное уравнение полностью совпадает с сокращенными ионным уравнением взаимодействия азотной кислоты и гидроксида калия.
При составлении ионных уравнений в виде ионов записывают только формулы:
1) сильных кислот (HCl, HBr, HI, H2SO4, HNO3, HClO4 ) (список сильных кислот надо выучить!)
2) сильных оснований (гидроксиды щелочных (ЩМ) и щелочно-земельных металлов(ЩЗМ))
3) растворимых солей
В молекулярном виде записывают формулы:
1) Воды H2O
2) Слабых кислот (H2S, H2CO3, HF, HCN, CH3COOH (и др. практически все органические)).
3) Слабых оcнований («NH4OH» и практически все гидроксиды металлов кроме ЩМ и ЩЗМ.
4) Малорастворимых солей (↓) («М» или «Н» в таблице растворимости).
5) Оксидов (и др. веществ, не являющихся электролитами).
Попробуем записать уравнение между гидроксидом железа (III) и серной кислотой. В молекулярном виде уравнение их взаимодействия записывается следующим образом:
2Fe(OH)3+ 3H2SO4 = Fe2(SO4)3 + 6H2O
Гидроксиду железа (III) соответствует в таблице растворимости обозначение «Н», что говорит нам о его нерастворимости, т.е. в ионном уравнении его надо записывать целиком, т.е. как Fe(OH)3 . Серная кислота растворима и относится к сильным электролитам, то есть существует в растворе преимущественно в продиссоциированном состоянии. Сульфат железа (III), как и практически все другие соли, относится к сильным электролитам, и, поскольку он растворим в воде, в ионном уравнении его нужно писать в виде ионов. Учитывая все вышесказанное, получаем полное ионное уравнение следующего вида:
2Fe(OH)3 + 6H+ + 3SO42- = 2Fe3+ + 3SO42- + 6H2O
Сократив сульфат-ионы слева и справа, получаем:
2Fe(OH)3 + 6H+ = 2Fe3+ + 6H2O
разделив обе части уравнения на 2 получаем сокращенное ионное уравнение:
Fe(OH)3 + 3H+ = Fe3+ + 3H2O
Теперь давайте рассмотрим реакцию ионного обмена, в результате которой образуется осадок. Например, взаимодействие двух растворимых солей :
Na2CO3 + CaCl2 = CaCO3↓+ 2NaCl
Все три соли – карбонат натрия, хлорид кальция, хлорид натрия и карбонат кальция (да-да, и он тоже) – относятся к сильным электролитам и все, кроме карбоната кальция, растворимы в воде, т.е. есть участвуют в данной реакции в виде ионов:
2Na+ + CO32- + Ca2+ + 2Cl− = CaCO3↓+ 2Na+ + 2Cl−
Сократив одинаковые ионы слева и справа в данном уравнении, получим сокращенное ионное:
CO32- + Ca2+ = CaCO3↓
Последнее уравнение отображает причину взаимодействия растворов карбоната натрия и хлорида кальция. Ионы кальция и карбонат-ионы объединяются в нейтральные молекулы карбоната кальция, которые, соединяясь друг с другом, порождают мелкие кристаллы осадка CaCO3 ионного строения.
Примечание важное для сдачи ЕГЭ по химии
Чтобы реакция соли1 с солью2 протекала, помимо базовых требований к протеканиям ионных реакций (газ, осадок или вода в продуктах реакции), на такие реакции накладывается еще одно требование – исходные соли должны быть растворимы. То есть, например,
CuS + Fe(NO3)2 ≠ FeS + Cu(NO3)2
реакция не идет, хотя FeS – потенциально мог бы дать осадок, т.к. нерастворим. Причина того что реакция не идет – нерастворимость одной из исходных солей (CuS).
А вот, например,
Na2CO3 + CaCl2 = CaCO3↓+ 2NaCl
протекает, так как карбонат кальция нерастворим и исходные соли растворимы.
То же самое касается взаимодействия солей с основаниями. Помимо базовых требований к протеканию реакций ионного обмена, для того чтобы соль с основанием реагировали необходима растворимость их обоих. Таким образом:
Cu(OH)2 + Na2S – не протекает,
т.к. Cu(OH)2 нерастворим, хотя потенциальный продукт CuS был бы осадком.
А вот реакция между NaOH и Cu(NO3)2 протекает, так оба исходных вещества растворимы и дают осадок Cu(OH)2:
2NaOH + Cu(NO3)2 = Cu(OH)2 ↓+ 2NaNO3
Внимание! Ни в коем случае не распространяйте требование растворимости исходных веществ дальше реакций соль1+ соль2 и соль + основание.
Например, с кислотами выполнение этого требования не обязательно. В частности, все растворимые кислоты прекрасно реагируют со всеми карбонатами, в том числе нерастворимыми.
Другими словами:
1) Соль1+ соль2 — реакция идет если исходные соли растворимы, а в продуктах есть осадок
2) Соль + гидроксид металла – реакция идет, если в исходные вещества растворимы и в продуктах есть осадок или гидроксид аммония.
Рассмотрим третье условие протекания реакций ионного обмена – образование газа. Строго говоря, только в результате ионного обмена образование газа возможно лишь в редких случаях, например, при образовании газообразного сероводорода:
K2S + 2HBr = 2KBr + H2S↑
В большинстве же остальных случаев газ образуется в результате разложения одного из продуктов реакции ионного обмена. Например, нужно точно знать в рамках ЕГЭ, что с образованием газа в виду неустойчивости разлагаются такие продукты, как H2CO3, «NH4OH» и H2SO3:
H2CO3 = H2O + CO2 ↑
«NH4OH» = H2O + NH3 ↑
H2SO3 = H2O + SO2 ↑
(«NH4OH» — такая запись формулы в кавычках подразумевает, что в реальности вещества с такой формулой не существует. Формула используется для большей простоты промежуточных записей. В реальности вместо «гидроксида аммония» правильнее писать формулу гидрата аммиака NH3·H2O).
Другими словами, если в результате ионного обмена образуются угольная кислота, гидроксид аммония или сернистая кислота, реакция ионного обмена протекает благодаря образованию газообразного продукта:
Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2 ↑
NH4NO3 + KOH = KNO3 + H2O + NH3 ↑
Na2SO3 + 2HCl = 2NaCl + H2O + SO2 ↑
Запишем ионные уравнения для всех указанных выше реакций, приводящих к образованию газов. 1) Для реакции:
K2S + 2HBr = 2KBr + H2S↑
В ионном виде будут записываться сульфид калия и бромид калия, т.к. являются растворимыми солями, а также бромоводородная кислота, т.к. относится к сильным кислотам. Сероводород же, являясь малорастворимым и плохо диссоциирцющим на ионы газом, запишется в молекулярном виде:
2K+ + S2- + 2H+ + 2Br— = 2K+ + 2Br— + H2S↑
Сократив одинаковые ионы получаем:
S2- + 2H+ = H2S↑
2) Для уравнения:
Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2 ↑
В ионном виде запишутся Na2CO3, Na2SO4 как хорошо растворимые соли и H2SO4 как сильная кислота. Вода является малодиссоциирующим веществом, а CO2 и вовсе неэлектролит, поэтому их формулы будут записываться в молекулярном виде:
2Na+ + CO32- + 2H + + SO42- = 2Na+ + SO42 + H2O + CO2 ↑
CO32- + 2H + = H2O + CO2↑
3) для уравнения:
NH4NO3 + KOH = KNO3 + H2O + NH3↑
Молекулы воды и аммиака запишутся целиком, а NH4NO3, KNO3 и KOH запишутся в ионном виде , т.к. все нитраты являются хорошо растворимыми солями, а KOH является гидроксидом щелочного металла, т.е. сильным основанием:
NH4+ + NO3−+ K+ + OH− = K+ + NO3− + H2O + NH3↑
NH4+ + OH− = H2O + NH3↑
Для уравнения:
Na2SO3 + 2HCl = 2NaCl + H2O + SO2 ↑
Полное и сокращенное уравнение будут иметь вид:
2Na+ + SO32- + 2H+ + 2Cl− = 2Na+ + 2Cl− + H2O + SO2 ↑
SO32- + 2H+ = H2O + SO2 ↑
Тонкости взаимодействия кислых солей (в частности, гидрокарбонатов, дигидрофосфатов и гидрофосфатов) со щелочами рассмотрены в данной публикации.
Реакции ионного обмена – это химические взаимодействия, в которых участвуют вещества, находящиеся в состоянии водных растворов. При этом степень окисления элементов, из которых они состоят, никогда не изменяется. Такие реакции проходят только с веществами, являющимися электролитами.
Это химические соединения, обладающие свойством проводить электрический ток.
В данных процессах реагирующие вещества обмениваются ионами друг с другом. Эти ионы образуют новые устойчивые связи.
Правило Бертолле
В соответствии с этим правилом можно определить, будет ли реакция ионного обмена протекать до конца. Такая реакция будет идти, если:
- образуется твердое вещество, являющееся практически нерастворимым (его легко обнаружить по выпавшему на дне пробирки осадку):
Ba(OH)2+H2SO4→BaSO4↓+2H2O;
- происходит образование летучего газообразного вещества (пузырьки газа всплывают из раствора на поверхность):
CaCO3+2HNO3→Ca(NO3)2+CO2↑+H2O;
- образуется хорошо растворяющееся в воде вещество, являющееся слабым малодиссоциирующим электролитом (также может образовываться вода, которая тоже относится к слабым электролитам):
3NaOH+H3PO4→Na3PO4+3H2O;
- происходит формирование комплексного иона (образуется комплексная соль):
2KOH+ZnO+H2O→K2[Zn(OH)4].
Для протекания реакции достаточно выполнения хотя бы одного из приведенных здесь условий. Если же не соблюдается ни одно условие, реакция в водном растворе так и не начнется.
Как составить ионное уравнение реакции
При составлении ионных уравнений необходимо учитывать, что:
- вещества, которые не растворяются в воде, не могут диссоциировать, т.е. в таком случае реакция ионного обмена начаться не может;
- вещества, относящиеся к малорастворимым, также присутствуют в растворах, находясь в них в виде ионов;
- если в процессе реакции образуется малорастворимое соединение, при записи уравнения в ионном виде оно условно считается нерастворимым;
- суммарные значения зарядов в левой и правой частях уравнения должны иметь одинаковую величину.
Составляя ионное уравнение, нужно всегда придерживаться следующей последовательности действий:
- Записать уравнение реакции в обычном, молекулярном виде. Чтобы правильно составить формулы образующихся соединений, необходимо к положительно заряженному иону одного реагирующего вещества (это начальный элемент его формулы) присоединить отрицательный ион другого вещества. Для оставшихся ионов следует проделать аналогичную операцию.
MgCl2+2AgNO3→2AgCl+Mg(NO3)2
- Используя таблицу растворимости, определить степень растворимости каждого соединения. Эти данные нужно получить для веществ из обеих частей уравнения.
MgCl2+2AgNO3→2AgCl+Mg(NO3)2
- Составить уравнение, которое отображает процесс диссоциации соединений, считающихся растворимыми. Это нужно сделать как для исходных компонентов, так и для конечных продуктов реакции.
MgCl2↔Mg2++2Cl—
AgNO3↔Ag++NO3—
AgCl – эта соль не диссоциирует, поскольку согласно данным, полученным из таблицы растворимости, она является нерастворимой:
Mg(NO3)2↔Mg2++2NO3—
- В соответствии с данными, полученными при выполнении предыдущего шага, составить полное ионное уравнение.
Mg2++2Cl—+2Ag++2NO3—→2AgCl↓+Mg2++2NO3—
- Записать ионное уравнение в сокращенном виде. Для этого достаточно просто убрать из левой и правой частей полного ионного уравнения совпадающие и одинаковые ионы.
Mg2++ 2Cl—+ 2Ag++2NO3— → 2AgCl↓+Mg2++2NO3—
Удалив все парные ионы, получим:
Ag++Cl—→AgCl↓
Ионное уравнение наглядно отображает сущность протекания реакции. В нем содержится информация, из которой можно узнать, что же на самом деле происходит в растворе. Что касается сокращенной записи ионного уравнения, то тут стоит отметить, что в виде одного и того же ионного уравнения может быть записано несколько реакций с разными веществами. Проиллюстрируем этот факт двумя примерами.
Примеры реакций ионного обмена
| Пример 1 | Пример 2 |
|---|---|
| HNO3+KOH→KNO3+H2O | 2HCl+Ba(OH)2→BaCl2+2H2O |
| H++NO3—+K++OH—→K++NO3—+H2O | 2H++2Cl—+Ba2++2OH—→Ba2++2Cl—+2H2O |
| H++OH—→H2O | H++OH—→H2O |
Данные примеры свидетельствуют, что химические процессы, наблюдающиеся в обеих случаях, схожи по своей сути.
Следует иметь в виду, что некоторые вещества при их растворении в воде начинают активно разлагаться. В частности, к ним относятся такие соли, как сульфид алюминия (Al2S3) и трехвалентный ацетат хрома (Cr(CH3COO)3). Это значит, что такие соединения в результате проведения реакций ионного обмена получить не удастся.
Тест по теме «Реакции ионного обмена»
Статьи
Основное общее образование
Линия УМК В. В. Лунина. Химия (8-9)
Химия
Ионные уравнения
Ионные уравнения — неотъемлемая часть сложной и интересной химической науки. Такие уравнения позволяют наглядно увидеть, какие ионы вступают в химические превращения. В виде ионов записывают вещества, которые подвергаются электролитической диссоциации. Разберем историю вопроса, алгоритм составления ионных уравнений и примеры задач.
06 июня 2019
ИСТОРИЯ ВОПРОСА
Еще древние алхимики, проводя нехитрые химические реакции в поисках философского камня и записывая в толстые фолианты результаты своих исследований, использовали определенные знаки для химических веществ. У каждого ученого была своя система, что неудивительно: каждый хотел защитить свои тайные знания от происков завистников и конкурентов. И лишь в VIII веке появляются единые обозначения для некоторых элементов.
В 1615 году Жан Бегун в своей книге «Начала химии», что по праву считается одним из первых учебников в этом разделе естествознания, предложил использовать условные обозначения для записи химических уравнений. И лишь в 1814 году шведский химик Йонс Якоб Берцелиус создал систему химических символов на основе одной или двух первых букв латинского названия элемента, подобную той, с которой ученики знакомятся на уроках.
В восьмом классе (параграф 12, учебник «Химия. 8 класс» под редакцией В.В. Еремина) ребята научились составлять молекулярные уравнения реакций, где и реагенты, и продукты реакций представлены в виде молекул.
Однако это упрощенный взгляд на химические превращения. И об этом задумывались ученые уже в XVIII веке.
Аррениус в результате своих экспериментов выяснил, что растворы некоторых веществ проводят электрический ток. И доказал, что вещества, обладающие электропроводностью, в растворах находятся в виде ионов: положительно заряженных катионов и отрицательно заряженных анионов. И именно эти заряженные частицы вступают в реакции.
ЧТО ТАКОЕ ИОННЫЕ УРАВНЕНИЯ
Ионные уравнения реакций — это химические равенства, в которых вещества, вступающие в реакцию, и продукты реакций обозначены в виде диссоциированных ионов. Уравнения данного типа подходят для записи химических реакций замещения и обмена в растворах.
Ионные уравнения — неотъемлемая часть сложной и интересной химической науки. Такие уравнения позволяют наглядно увидеть, какие ионы вступают в химические превращения. В виде ионов записывают вещества, которые подвергаются электролитической диссоциации (тема подробно разбирается в параграфе 10, учебник «Химия. 9 класс» под редакцией В.В. Еремина). В виде молекул записывают газы, вещества, выпадающие в осадок, и слабые электролиты, которые практически не диссоциируют. Газы обозначаются стрелкой вверх (↑), субстанции, выпадающие в осадок, стрелкой вниз (↓).

Химия. 8 класс. Учебник
Учебник написан преподавателями химического факультета МГУ им. М.В. Ломоносова. Отличительными особенностями книги являются простота и наглядность изложения материала, высокий научный уровень, большое количество иллюстраций, экспериментов и занимательных опытов, что позволяет использовать ее в классах и школах с углубленным изучением естественно-научных предметов.
Купить
ОСОБЕННОСТИ ИОННЫХ УРАВНЕНИЙ
1. Реакции ионного обмена, в отличие от окислительно-восстановительных реакций, протекают без нарушения валентности веществ, вступающих в химические превращения.

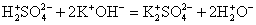
2. Реакции между ионами протекают при условии образования в ходе реакции плохорастворимого осадка, выделения летучего газа или образования слабых электролитов.
CuCl2 + 2NaOH = Cu(OH)2↓ + 2NaCl
Na2CO3 + 2HCl = 2NaCl + CO2↑+ H2O
Удивительно, что реакции обмена могут проходить даже с нерастворимыми солями слабых кислот. В этом случае сильная кислота вытесняет слабую из ее солей. В качестве примера можно привести сокращенное ионное уравнение разведения карбоната кальция в сильных кислотах.

АЛГОРИТМ СОСТАВЛЕНИЯ ИОННОГО УРАВНЕНИЯ
-
Записываем молекулярное уравнение химического процесса.
H2SO4 + KOH = K2SO4 + H2O
-
Балансируем молекулярное уравнение с помощью коэффициентов.
Чтобы правильно сбалансировать равенство, нужно вспомнить закон сохранения массы веществ (параграф 12, «Химия. 8 класс» под редакцией В.В. Еремина), согласно которому в ходе химических превращений новые атомы не появляются, а старые не разрушаются. Т.е. число атомов в продуктах реакции равно числу атомов в исходных веществах. Помним, что водород и кислород уравниваем в последнюю очередь.
H2SO4 + 2KOH = K2SO4 + 2H2O
-
Определяем, какие вещества в химической реакции диссоциируют, т.е. распадаются на ионы.
Записываем в виде ионов:
- растворимые соли;
- сильные кислоты (H2SO4, HNO3, HCl и др.);
- растворимые в воде основания.
Записываем в виде молекул:
- нерастворимые соли;
- слабые кислоты, щелочи, вода;
- оксиды;
- газы;
- простые вещества;
- большинство органических соединений.
Если есть сомнения в растворимости реагента или продукта реакции, можно проверить по специальной таблице, которая является справочным материалом, ей можно пользоваться на различных экзаменах.
В таблице, помимо растворимости соединений, представлены также заряды катионов и анионов, участвующих в реакциях.
-
Определяем многоатомные ионы.
Это необходимо сделать, т.к. данные соединения не разлагаются на отдельные атомы и имеют свой заряд. Чаще всего в химических превращениях участвуют следующие многоатомные ионы:
-
Записываем равенство таким образом, чтобы все диссоциирующие субстанции были представлены в виде катионов и анионов.
Проверяем, чтобы уравнение было сбалансировано, т.е. количество различных атомов в частях с реагентами и продуктами реакции совпадало.
На данном этапе мы получили полное ионное уравнение.
-
Вычеркиваем идентичные ионы в обеих частях равенства, т.е. катионы и анионы с одинаковыми нижними индексами и зарядами, и переписываем равенство без данных ионов.
2H + 2OH = 2H2O
Проверяем, чтобы количество атомов элементов совпадало в правой и левой частях уравнения. Таким образом получаем краткое ионное уравнение.
ПРИМЕРЫ
Задача 1
Выясните, произойдет ли химическое взаимодействие между растворами гидроксида калия и хлорида аммония. (Записать для реакции молекулярное, полное ионное и сокращенное ионное уравнение.)
-
Записываем молекулярное уравнение, проверяем коэффициенты.
KOH + NH4Cl = KCl + NH4OH
Помним, что гидроксид аммония — нестабильное соединение и разлагается на аммиак и воду.
Записываем окончательное уравнение:
KOH (p) + NH4Cl (p) = KCl (p) + NH3↑+ H2O
NB! Благодаря летучести и резкому раздражающему запаху 3%-й раствор NH3 называется «нашатырный спирт» и используется в медицине.
-
Подсматривая в таблицу растворимости, помечаем полное ионное уравнение, не забывая о зарядах ионов.
-
Вычеркивая идентичные катионы и анионы в обеих частях реакции, составляем краткое ионное уравнение.
-
Делаем вывод: химическая реакция между гидроксидом калия и хлоридом аммония протекает с образованием воды и выделением аммиака — летучего газа с резким запахом.
Задача 2
А сейчас выполним задание из учебника «Химия. 9 класс» под редакцией В.В. Еремина.
Налейте в пробирку 1 мл раствора карбоната натрия и аккуратно прилейте к нему пару капелек соляной кислоты.
Что происходит?
Составьте уравнение реакции, напишите полное и сокращенное ионные уравнения.
-
Записываем реакцию в молекулярном виде, расставляем коэффициенты, если это необходимо.
Na2CO3 + 2HCl = 2NaCl + H2O + CO2
-
Подсматривая в таблицу растворимости, записываем полное ионное уравнение, не забывая отмечать заряды ионов.
-
Вычеркивая одинаковые катионы и анионы в правой и левой частях равенства, составляем краткое ионное уравнение.
Вопрос «Что происходит?» остался без ответа. К сожалению, в домашних условиях этот опыт осуществить трудновато, так как стиральной содой уже давно никто не пользуется, да и соляную кислоту в аптеке уже не продают. Но примерно такой же визуальный эффект можно наблюдать, если смешать раствор пищевой соды с раствором уксусной кислоты.
#ADVERTISING_INSERT#