Среднее значение квадрата скорости
Нас будет интересовать
средний квадрат проекции скорости. Он
находится так же, как квадрат модуля
скорости (см. выражение (4.1.2)):
(4.3.2)
Скорости
молекул принимают непрерывный ряд
значений. Определить точные значения
скоростей и вычислить среднее значение
(статистическое среднее) с помощью
формулы (4.3.2) практически невозможно.
Определим
несколько иначе, более реалистично.
Обозначим черезп1
число
молекул в объеме 1 см3,
имеющих проекции скоростей, близкие к
v1х;
через
п2
—
число молекул в том же объеме, но со
скоростями, близкими к vkx,
и
т. д.* Число молекул со скоростями,
близкими к максимальной vkx,
обозначим
через nk
(скорость
vkx
может
быть сколь угодно велика). При этом
должно выполняться условие: п1
+ п2
+ …
+ ni
+
… + nk
= п, где
п
— концентрация
молекул. Тогда для среднего значения
квадрата проекции скорости вместо
формулы (4.3.2) можно написать следующую
эквивалентную формулу:
* О том, как эти
числа могут быть определены, будет
рассказано в §4.6.
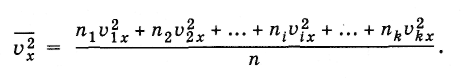
(4.3.3)
Так
как направление X
ничем
не отличается от направлений Y
и Z
(опять-таки
из-за хаоса в движении молекул), справедливы
равенства:
(4.3.4)
Для каждой молекулы
квадрат скорости равен:
Значение среднего
квадрата скорости, определяемое так
же, как средний квадрат проекции скорости
(см. формулы (4.3.2) и (4.3.3)), равно сумме
средних квадратов ее проекций:
(4.3.5)
Из выражений
(4.3.4) и (4.3.5) следует, что
(4.3.6)
т.
е. средний квадрат проекции скорости
равен
среднего квадрата самой скорости.
Множительпоявляется вследствие трехмерности
пространства и, значит, существования
трех проекций у любого вектора.
Скорости
молекул беспорядочно меняются, но
среднее значение проекций скорости на
любое направление и средний квадрат
скорости —
вполне
определенные величины.
§ 4.4. Основное уравнение молекулярно-кинетической теории
Вычислим с помощью
молекулярно-кинетической теории давление
газа. На основе проделанных расчетов
можно будет сделать очень важный вывод
о связи температуры газа со средней
кинетической энергией молекул.
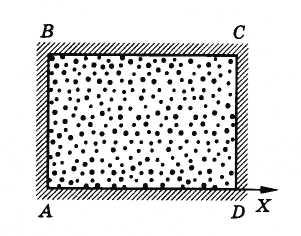
Пусть газ находится
в прямоугольном сосуде с твердыми
стенками. Газ и сосуд имеют одинаковые
температуры, т. е. находятся в состоянии
теплового равновесия. Будем считать
столкновения молекул со стенками
абсолютно упругими. При этом условии
кинетическая энергия молекул в результате
столкновения не меняется.
Требование того,
чтобы столкновения были абсолютно
упругими, не является строго обязательным.
В точности оно и не реализуется. Молекулы
могут отражаться от стенки под разными
углами и со скоростями, не равными по
модулю скоростям до соударения. Но в
среднем кинетическая энергия отраженных
стенкой молекул будет равна кинетической
энергии падающих молекул, если только
существует тепловое равновесие.
Результаты расчета не зависят от
детальной картины столкновений молекул
со стенкой. Поэтому вполне допустимо
считать столкновения молекул подобными
столкновениям упругих шаров с абсолютно
гладкой твердой стенкой.
Вычислим
давление газа на стенку сосуда CD,
имеющую
площадь S
и расположенную перпендикулярно оси X
(рис.
4.3).
Рис. 4.3
Соседние файлы в предмете [НЕСОРТИРОВАННОЕ]
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Газов в природе
существует великое множество, и все они имеют определенные отличительные свойства.
Но для исследований необходимо ввести некую идеализированную модель, которая
так и называется: идеальный газ. Впервые ввести модель идеального газа
предложил Михаил Ломоносов. Большой вклад в создание такой модели, как
идеальный газ, внес Джеймс Джоуль, но все же, основной труд принадлежит
Рудольфу Клаузиусу. Именно Клаузиус ввел модель идеального газа в 1857 году.
Итак, идеальный газ — это
модель реального газа, взаимодействие между молекулами которого, пренебрежимо
мало.
Упоминая об идеальном
газе, мы предполагаем следующее:
·
Молекулы
газа очень малы и представляют собой упругие шарики.
·
Молекулы
этого газа двигаются беспорядочно.
·
Взаимодействия
между молекулами газа происходят только при соударениях, а соударения считаются
абсолютно упругими.
Конечно, такого газа в
природе не существует. Однако данная модель очень хорошо подходит для
исследования тех свойств газов, которые мы будем рассматривать в дальнейшем.
Надо сказать, что разряжённый водород, практически полностью соответствует
модели идеального газа. Впрочем, при привычных нам температурах, таких, как
комнатная температура, например, модель идеального газа достаточно хорошо
описывает реальные газы, такие, как воздух.
Рассмотрим давление газа
на стенки закрытого сосуда. Как вы знаете, давление газа возникает в результате
соударений молекул газа со стенками сосуда. Прибор, измеряющий давление,
называется манометр.
Манометр
Конечно, манометр не
может улавливать силу удара отдельных молекул. Манометр регистрирует среднюю
по времени силу, которая действует на единицу площади поверхности. Если мы
построим график зависимости давления от времени, то убедимся, что давление
постоянно меняется.
Однако наблюдаются не
хаотичные скачки давления, а сравнительно небольшие колебания вокруг какого-то
среднего значения. Поэтому, давление оказывается вполне определенной величиной.
В одном из предыдущих уроков мы убедились, что газы легко сжимаются, но при
этом повышается давление. Теперь мы можем в этом ещё раз убедиться: очевидно,
что если газ поместить в меньший объём, то количество соударений в единицу
времени увеличится. Это увеличит среднюю силу, а, значит, давление тоже
увеличится.
Но, чтобы вычислить
среднее давление, необходимо знать среднюю скорость молекул. Точнее, как мы
убедимся чуть позже, нам нужно знать значение не самой средней скорости, а
квадрата средней скорости. Конечно же, проследить за всеми молекулами газа
просто невозможно. Их очень много, все они движутся по хаотичной траектории,
преодолевая несколько сотен метров в секунду. Но нас не интересует скорость
отдельной молекулы. Нас интересует, к какому результату приводит движение всех
молекул газа.
Приведем простой пример.
Когда повар готовит ужин для большого количества людей, он не знает, кто
сколько съест.
Но повар знает какое-то
среднее количество еды, которое может съесть за ужином среднестатистический
человек, и, исходя из этого, рассчитывает количество еды, которое необходимо
приготовить.
Точно также, нам не надо
знать скорости отдельных молекул. Нам необходимо знать какое-то среднее
значение скорости, и, исходя из него, производить те или иные расчеты.
Обозначим скорости
молекул за 𝑣1,𝑣2,…,𝑣𝑛.
Тогда среднее значение квадрата скорости будет вычисляться по формуле:
Напомним, что скорость —
это векторная величина, а квадрат любого вектора равен сумме квадратов его
проекций. Значит, среднее значение квадрата скорости будет равно сумме
квадратов средних значений проекций скорости на координатные оси:
Разумеется, средние
значения квадратов проекций на оси можно определить тем же способом:
Конечно, молекулы
двигаются абсолютно беспорядочно, поэтому мы можем считать проекции на все три
оси равноправными. То есть, мы справедливо можем предположить, что проекция на
ось х равна проекциям на оси у и z.
Таким образом, мы можем заключить, что среднее значение квадрата проекции
скорости на любую ось равно одной третьей среднего значения квадрата самой
скорости:
Напомним, что каждое
тело, в частности газ, обладает макроскопическими и микроскопическими
параметрами. К макроскопическим параметрам относятся давление, температура и
объём. Как правило, именно с помощью макроскопических параметров мы
характеризуем то или иное тело. Но макроскопические параметры зависят от
микроскопических, таких, как масса, размеры и скорости молекул. В ближайшее
время мы будем заниматься изучением того, как макроскопические параметры газа
зависят от микроскопических.
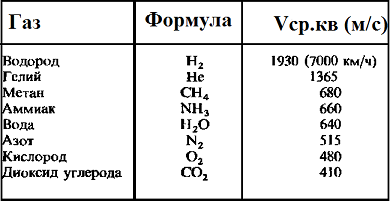
Средняя квадратичная скорость молекул — среднее квадратическое значение модулей скоростей всех молекул рассматриваемого количества газа
Таблица значений средней квадратичной скорости молекул некоторых газов
Для того чтоб понять, откуда же у нас получается эта формула, мы выведем среднюю квадратичную скорость молекул. Вывод формулы начинается с основного уравнения молекулярно кинетический теории (МКТ):
Где у нас количество вещества, для более легкого доказательства, возьмем на рассмотрение 1 моль вещества, тогда у нас получается:
Если посмотреть, то PV это две третьих средней кинетической энергии всех молекул (а у нас взят 1 моль молекул):
Тогда, если приравнять правые части, у нас получается, что для 1 моля газа средняя кинетическая энергия будет равняться:
Но средняя кинетическая энергия, так же находится, как :
А вот теперь, если мы приравняем правые части и выразим из них скорость и возьмем квадрат,Число Авогадро на массу молекулы , получается Молярная масса то у нас и получится формула для средней квадратичной скорости молекулы газа:
А если расписать универсальную газовую постоянную, как , и за одно молярную массу
, то у нас получится?
В Формуле мы использовали :
— Средняя квадратичная скорость молекул
— Постоянная Больцмана
— Температура
— Масса одной молекулы
— Универсальная газовая постоянная
— Молярная масса
— Количество вещества
— Средняя кинетическая энергия молекул
— Число Авогадро
Векторная величина, то есть она имеет абсолютную величину и направление.
Движение тела можно представить как совокупность мгновенных пребываний его в последовательных точках траектории, поэтому указанную характеристику движения называют мгновенной скоростью.
Вектор скорости нередко выражают в проекциях на координатные оси:
v=vxi+vyj+vzkv={{v}_{x}}i+{{v}_{y}}j+{{v}_{z}}k
или в виде
v=dxdti+dydtj+dzdtkv=frac{dx}{dt}i+frac{dy}{dt}j+frac{dz}{dt}k
а модуль вектора находят по формуле
v=vx2+vy2+vz2v=sqrt{{{v}_{x}}^{2}+{{v}_{y}}^{2}+{{v}_{z}}^{2}}
Такой чисто физический смысл скорости как меры движения отдельного тела.
Средняя скалярная скорость
Наряду с этим на практике в описаниях движений часто удовлетворяются средней скалярной скоростью – характеристикой движения, которая определяется как отношение пути к промежутку времени, за который тело преодолело этот путь:
v=s/Δtv = s/Δt,
где vv – средняя скорость, ss – путь, ΔtΔ t – промежуток времени.
Это определение отличается от определения собственно скорости тем, что скорость является отношением перемещения к промежутку времени, а следовательно векторной величиной.
Например, болид Формулы 1, преодолев круг, и вернувшись на свое место, совершил нулевое перемещение, но прошел путь, равный длине окружности. То есть, можно посчитать среднюю скорость его движения.
Единицы измерения средней скалярной скорости те же, что и для скорости, м/с, км/ч и т.д.
При предельном переходе Δt→0Δt → 0, значение средней скалярной скорости стремится к модулю скорости.
Средне-квадратичная скорость
При определении скорости движения частиц в статистической физике удобнее усреднять не модуль скорости, а квадрат её значения. Тогда средняя скорость определяется как
v=⟨v2⟩v = ⟨v2⟩.
Усреднения проводится по всем частицам и по времени.
При отсутствии упорядоченного движения, то есть течения, среднее перемещение отдельной частицы на достаточно большом промежутке времени равно нулю, поэтому среднее значение векторной скорости тоже равна нулю. Однако среднее значение квадрата скорости отличное от нуля и связано с температурой.
Тангенциальная скорость
Линейная скорость, определяет расстояние пройденное за единицу времени, в то время как тангенциальная скорость это линейная скорость чего-то, что движется вокруг круговой траектории. Точка на внешней части карусели проходит большую дистанцию при одном полном обороте чем точка ближе к центру.
Прохождение большего расстояния за одинаковое время означает, что данная точка будет иметь большую скорость, и поэтому линейная скорость будет больше на внешнем крае вращающегося объекта, чем более близкого к оси вращения. Такую скорость вдоль круговой траектории называют тангенциальной скоростью поскольку направлением движения является прямая, касательная к дуге окружности.
Для кругового движения, тангенциальная скорость и линейная скорость являются взаимозаменяемыми и обе выражаются в м/с, км/ч или т.д.
Тест по теме «Средняя скорость»
Средняя квадратичная скорость — среднее квадратическое значение скоростей всех молекул данного количества газа. Измеряется в (м^2/с^2.)
Что оказывает влияние на скорость молекул
На быстроту движения молекул в газе оказывают влияние следующие параметры:
- Давление (возникает в результате ударов частиц о стенки сосуда).
- Концентрация частиц (количество частиц в единице объема).
- Температура (с увеличением температуры, частицы начинают двигаться быстрее, с уменьшением — замедляются).
- Масса молекул.
Эта взаимозависимость выражается главным уравнением молекулярно-кинетической теории идеального газа:
Осторожно! Если преподаватель обнаружит плагиат в работе, не избежать крупных проблем (вплоть до отчисления). Если нет возможности написать самому, закажите тут.
(P=frac13times m_0times ntimes V^2)
Где P — давление газа в Паскалях, (m_0) — масса молекулы в килограммах, n — концентрация частиц в (м^3), V — скорость движения молекул в м/с.
Расчет по формуле
Для определения средней квадратичной скорости (обозначение — v) всех молекул в газе, нужно вычислить квадратный корень из средней арифметической величины квадратов скоростей каждой частицы.
В виде формулы это выглядит так:
(v=sqrt{frac{v_1^2+v_2^2+…v_n^2}N})
Где (v_1) — (v_n) — это скорости молекул, N — их число в газе.
Расчет значения по такой формуле очень громоздок и сложен, поэтому для определения значения средней квадратичной скорости используют следующее уравнение:
(v=sqrt{frac{3times Rtimes T}M})
Где R — универсальная газовая постоянная, равная примерно 8,31 Дж/Кхмоль, T — температура в Кельвинах, M — молярная масса в кг/моль.
Получается такое уравнение путем преобразования основного уравнения кинетической теории газов.