Ученые НМИЦ онкологии имени Н. Н. Петрова разработали уникальную технологию создания противоопухолевых вакцин на основе клеток иммунной системы. Эти препараты могут быть эффективны даже в терминальных случаях раковых заболеваний. Патент на последний из компонентов был получен в 2021 году. Сейчас технологию готовят к лицензированию, после чего будут применять для спасения пациентов.
40% успеха
Над созданием препаратов, которые смогут эффективно уничтожать клетки злокачественных опухолей, не повреждая при этом здоровые органы, ученые бьются давно. Разработанные в НМИЦ онкологии вакцины — как раз такое лекарство. Они изготавливаются на основе дендритных клеток (специализированные на презентации антигенов лейкоциты, необходимые для формирования Т-клеточного ответа организма инфекциям и опухоли — ред.). Для создания вакцины ученые берут кровь именно того пациента, для которого предназначается лекарство, обрабатывают ее специальным образом, обучая на девяти раковых культурах, и затем вводят больному. Если организм отзывается на препарат (это бывает в 40% случаев), то иммунная система начинает распознавать клетки опухоли и уничтожать их. Результаты поразительны.
«Онкологические пациенты нуждаются в разных методах лечения, — объясняет одна из создателей дендритной вакцины, заведующая научным отделом онкоиммунологии НМИЦ имени Н. Н. Петрова Ирина Балдуева. — Это и лучевая, и таргетная, и радио-, и химиотерапия, хирургические вмешательства и иммунотерапия. Противоопухолевая вакцина — один из видов иммунологического лечения».
Работа над ее созданием началась еще в 2010 году, но тогда получить лицензию было невозможно из-за ограничений в законодательстве. Условия изменились лишь в 2016-м, и ученые стали дорабатывать свое детище. Российский научный фонд поддержал работу сотрудников НМИЦ онкологии и дал им на продолжение перспективных исследований грант 22–25–00723*.
800 спасенных жизней
Пока вакцину использовали только для лечения пациентов в терминальных стадиях заболевания. Бывает, что организм больного не отзывается ни на один из методов лечения — рак буквально пожирает его. Или же диагноз был поставлен слишком поздно, и метастазы поразили много органов. Случается и так, что злокачественные клетки мутируют, и общеизвестные препараты перестают на них воздействовать. Во всех этих ситуациях итог один: консервативные методы лечения становятся бессильны. Прежде спасти таких пациентов было невозможно. Противоопухолевые вакцины серьезно изменили расклад.
Как рассказала Ирина Балдуева, среди тех, кому давали вакцину на основе дендритных клеток, есть человек, умиравший от меланомы и саркомы мягких тканей. 55-летний на тот момент петербуржец был признан неоперабельным, спасти его казалось невозможным. Вакцина помогла. Всего ему пришлось получить ее 41 раз, но в итоге болезнь отступила. Вот уже 15 лет мужчина живет со стойкой ремиссией, последние 4 года у него нет даже признаков болезни.
Вводили противоопухолевую вакцину и другим умирающим от онкологических заболеваний пациентам. Всего их более 800 человек. Многие из них живут уже больше пяти лет после окончания курса.
В среднем, лечение занимает три года. Сначала вакцина вводится 4 раза каждые две недели, затем пациент получает восемь доз лекарства — по одной ежемесячно. За второй год лечения вакцину вводят четыре раза, а за третий — дважды. После этого курс считается пройденным.
Еще одно действие вакцины на основе дендритных клеток — повышение иммунитета. Дело в том, что после консервативного лечения — радио-, лучевой и химиотерапии — иммунная система онкологического пациента сильно страдает. Агрессивные препараты, которые дают больному, уничтожают опухоль, но при этом повреждают и здоровые клетки. Ослабленный интоксикацией организм может даже погибнуть, не справившись после лечения с каким-то другим заболеванием — например, с гриппом. Поэтому поддержка иммунной системы онкологических пациентов крайне важна, а противоопухолевая вакцина как раз и стимулирует естественные защитные силы организма.
Защита от мутагенности
Есть среди научных открытий ученых НМИЦ онкологии имени Н. Н. Петрова и еще одно изобретение: препарат на основе лигнина (вещества, характеризующего одеревеневшие стенки растительных клеток, сложного полимерного соединения, содержащегося в клетках сосудистых растений и некоторых водорослях — ред.) Ученые считают, что он может помочь с решением проблемы отдаленного неблагоприятного воздействия противоопухолевого лечения — в том числе развития вторых первичных опухолей и фиброза легких у излечившихся пациентов, а также влияния на их детей и внуков. Эти исследования тоже поддержаны грантами Российского научного фонда (20–15–00330 и 22–25–20177*) и Санкт-Петербургского научного фонда (№ 50/2022*).
Развитие вторых первичных опухолей (возникновение рака в других органах) — осложнение, с которым сталкиваются вылечившие онкологическое заболевание люди, особенно если они болели молодыми.
«Последствиями химио- и радиотерапии может быть накопление генетических повреждений, — объясняет заведующая научной лабораторией канцерогенеза и старения НМИЦ онкологии им. Н.Н. Петрова Елена Федорос. — Это лечение — потенциально мутагенное, оно повреждает и здоровые клетки организма. Мы сталкиваемся с тем, что у вылеченных однажды людей спустя 15–20 лет появляются так называемые вторые первичные опухоли, поражающие уже другие органы. Чаще всего они наблюдаются у тех, кто пережил юношеский лейкоз (злокачественное заболевание крови)».
Специалисты уже доказали на лабораторных животных, что производные лигнина существенно снижают токсичность препаратов химиотерапевтического лечения и улучшают переносимость радиотерапии. А кроме того, это вещество предохраняет молекулы ДНК, уменьшая уровень их повреждений, что снижает риски вторых опухолей у пациентов, а также защищает их возможных детей. Патент на изобретение получили в 2017 году, но исследования еще продолжаются.
Ученые надеются, что сочетание консервативного лечения с приемом препаратов на основе лигнина снизит повреждающее воздействие агрессивных препаратов — и повторные онкологические заболевания у пациентов будут возникать реже. Исследование поддержано грантом Российского научного фонда (№ 20–15–00330*).
Возможность профилактики фиброза легких, которой рассчитывают добиться ученые, тоже связана со способностью производных лигнина защищать здоровые клетки организма от последствий агрессивного лечения. Один из часто используемых в лечении рака препаратов, эффективный при борьбе с лимфомами, онкозаболеваниями яичек и яичников и шейки матки, может привести к побочному эффекту — фиброзу легких. Уйдя в ремиссию по основной болезни, пациент рискует остаться с нездоровыми легкими — и лечить придется уже их.
Все эти исследования, по оценкам ученых, очень перспективны. Если их довести до логического и успешного завершения, Россия может стать новым мировым центром по лечению злокачественных заболеваний даже самых запущенных стадий.
Источник
«Помочь иммунитету увидеть опухоль»: как работает иммунотерапия онкозаболеваний
09.09.2022
В 2018 году иммунологи Джеймс Аллисон и Тасуку Хондзе получили Нобелевскую премию за разработку нового метода лечения онкологических заболеваний — иммунотерапии. Она не уничтожает злокачественные клетки, как, например, химиотерапия, — вместо этого помогает нашей иммунной системе «найти» опухоль и бороться с ней дальше.
Как работают иммуноонкологические препараты и в каких ситуациях они могут назначаться? Как проводится иммунотерапия и какие побочные эффекты возникают чаще всего? Нужно ли укреплять иммунитет во время лечения и что наука говорит об иммуномодуляторах?
На эти вопросы подробно отвечает онколог-химиотерапевт Владислав Евсеев — выпускник Высшей школы онкологии, эксперт онлайн-справочной «Просто спросить» для онкологических пациентов и их близких.
Рак — это всегда из-за плохого иммунитета?
Рак — заболевание, у которого сложно определить какую-то одну конкретную причину. Риски развития онкологических заболеваний зависят от огромного количества факторов — образа жизни, наследственности и различных хронических заболеваний. Иммунитет также играет роль в развитии рака и борьбе с ним.
В ряде ситуаций у человека может быть значительное снижение иммунитета — например при ВИЧ-инфекции или после трансплантации органов. При таких состояниях повышается риск развития некоторых злокачественных опухолей — в том числе плоскоклеточного рака кожи, опухолей шейки матки. В связи с этим врач может порекомендовать специальные программы наблюдения для выявления опухоли на ранних стадиях.
Но обычно люди оценивают иммунитет по тому, как часто они болеют простудой (острыми респираторными вирусными инфекциями). К сожалению, провести взаимосвязь между такими показателями работы иммунной системы и риском развития онкологических заболеваний нельзя.
Также никакие «иммунограммы» — то есть анализы, которые обещают отразить состояние иммунной системы — не помогают спрогнозировать развитие опухолей. Одним из немногих исключений может быть оценка уровня CD4 лимфоцитов и соотношения CD4 и CD8 лимфоцитов у пациентов с ВИЧ-инфекцией. Эти данные могут помочь более точно определить риск развития онкозаболевания у конкретного человека, но все равно не предскажут, будет ли вообще рак и, если да, то когда.
Что такое иммунотерапия онкологических заболеваний и как она действует?
Опухолевые клетки возникают из обычных клеток нашего организма. В норме жизнь клетки «распланирована» молекулами ДНК, но ежедневно в ДНК большого количества клеток возникают мутации. Под воздействием факторов внешней среды, например курения или ультрафиолетового излучения, риск возникновения и количество мутаций увеличиваются. Наследственность тоже может играть в этом роль.
Некоторые мутации не совместимы с жизнью клетки, и при их появлении она погибает. Другая часть мутированных клеток выявляется и уничтожается иммунной системой. К сожалению, постепенно в некоторых клетках может накопиться достаточное количество мутаций, чтобы они потеряли свою инструкцию для жизни и начали вести себя бесконтрольно, то есть, по сути, стали опухолевыми.
Чтобы выжить, злокачественные клетки находят способ скрыться и пропасть из вида иммунной системы. Такие механизмы позволяют опухоли длительное время развиваться, не будучи замеченной организмом.
Один из важнейших таких механизмов — влияние на так называемые «контрольные точки», которые представляют собой рецепторы на поверхности иммунных клеток. Опухолевые клетки воздействуют на эти рецепторы и «успокаивают» иммунную систему. В норме эта система нужна в организме человека для того, чтобы не допустить ситуации, когда наши иммунные клетки атакуют наши же органы, и это приводит к развитию аутоиммунных заболеваний, таких как ревматоидный артрит, при котором повреждаются суставы.
Иммунотерапия онкологических заболеваний оказалась настолько прорывным и важным методом лечения, что в 2018 году американец Джеймс Аллисон и японец Тасуку Хондзе получили Нобелевскую премию по медицине и физиологии за свои исследования в этой области.
Именно эти ученые и нашли «контрольные точки», которые позволили опухоли подавлять клетки иммунной системы. На основании этих фундаментальных работ появился целый класс препаратов ингибиторов контрольных точек, который помог иммунной системе увидеть злокачественные клетки и заново научить организм бороться с опухолью.
Чтобы понять, насколько сильно иммунотерапия повлияла на лечение онкологических заболеваний, можно привести в пример меланому — самый агрессивный вид рака кожи. Еще около 10-15 лет назад единственной возможностью терапии при этой опухоли с метастазами была химиотерапия, которая не помогала, и, к сожалению, большинство пациентов погибали в первый год после постановки диагноза.
Иммунотерапия в корне поменяла ситуацию: исследования показали, что даже на 4 стадии меланомы при использовании двойной иммунотерапии (ниволумаб + ипилимумаб) более 50% пациентов прожили 6 и более лет. То есть сейчас этот метод лечения дает даже таким сложным пациентам шанс на полное излечение.
Вообще идея иммунотерапии совсем не новая. На протяжении последних 100 лет исследователи пытались разными способами помочь организму самому бороться против онкологических заболеваний. Некоторые из этих методов даже вошли в клиническую практику.
Есть очень интересный пример в лечении рака мочевого пузыря: при этом заболевании введение вакцины БЦЖ (против туберкулеза) в мочевой пузырь позволяет снизить вероятность рецидива опухоли — именно за счет активизации иммунной системы. Также при меланоме и раке почки применяются препараты интерферона, которые притягивают в опухоль лимфоциты и другие клетки иммунной системы и повышают их активность.
Однако, когда сейчас говорят об иммунотерапии, в первую очередь имеют в виду именно ингибиторы контрольных точек, за которые была вручена Нобелевская премия.
В каких ситуациях назначают иммунотерапию и кому она не подходит?
Сейчас показания для иммунотерапии постоянно расширяются. Это значит, что врач может назначить такой вариант лечения в большем количестве ситуаций.
Иммуноонкологические препараты очень активно применяются при раке легкого, меланоме, опухоли почки, но и при других заболеваниях могут возникнуть ситуации, когда эти препараты будут полезны. Например, если при раке желудка выявлены метастазы в другие органы, а в клетках опухоли или ее окружения обнаружены молекулы, отвечающие за блокирование иммунной системы, то к химиотерапии может быть добавлено и иммунотерапевтическое лечение.
При этом надо понимать, что иммунотерапия подходит не всем пациентам. В ряде ситуаций, помимо типа опухоли, бывают очень важны и некоторые ее внутренние особенности, которые врач может выяснить, проведя специальные анализы. Например, при любых онкологических заболеваниях определение таких параметров, как микросателлитная нестабильность (MSI) или опухолевая мутационная нагрузка (TMB), может подсказать — будет иммунотерапия эффективна или нет.
В некоторых ситуациях иммунотерапию не назначают из-за высокого риска побочных явлений. Так, этот вид лечения может быть очень опасен для пациентов с аутоиммунными заболеваниями, при которых иммунитет атакует свои же клетки. Известный пример такой болезни — системная красная волчанка.
Иммуноонкологические препараты назначаются на разных стадиях онкологического заболевания. Изначально они использовались только в ситуации, когда опухоль уже дала метастазы в другие органы, но сейчас могут применяться после операции для снижения риска рецидива. Такой подход уже широко зарекомендовал себя при лечении меланомы.
Более того, сейчас все больше изучается вопрос назначения иммунотерапии и до операции — для того, чтобы уменьшить размеры опухоли и облегчить работу хирурга. А недавно были представлены результаты исследования, в котором у небольшой группы пациентов с раком прямой кишки применение иммунотерапии позволило и вовсе избежать операции и сохранить такой важный орган.
Какие иммуноонкологические препараты сегодня существуют?
Сейчас под иммунотерапией понимают в первую очередь ингибиторы контрольных точек, то есть препараты, которые блокируют элементы опухолевых клеток, позволяющие им скрываться от иммунной системы.
Все эти препараты уже можно разделить на несколько групп, в зависимости от того, на какую именно «контрольную точку» они действуют:
- Ингибиторы CTLA-4: ипилимумаб (Йервой)
- Ингибиторы PD-1: пембролизумаб (Китруда), ниволумаб (Опдиво)
- Ингибиторы PD-L1: атезолизумаб (Тецентрик), дурвалумаб (Имфинзи)
Это далеко не все представители иммунотерапевтических препаратов, с каждым годом их становится все больше и больше.
В 2020 году появился и российский оригинальный иммуноонкологический препарат пролголимаб (тороговое название — «Фортека»). Он относится к группе PD-1 ингибиторов и сейчас чаще всего назначается при меланоме, но со временем показания к его применению наверняка расширятся.
Как проводится иммунотерапия?
Иммунотерапия проводится посредством внутривенного введения препаратов, то есть по сути это обычные капельницы.
Как и при других вариантах лекарственного лечения, таких как химиотерапия или таргетная терапия, здесь есть определенная цикличность. То есть иммуноонкологические препараты вводятся с определенными интервалами времени. В зависимости от препарата и используемой дозы эти интервалы могут сильно отличаться — от одного раза в 2 недели, до 1 раза в 6 недель.
Важно сказать, что иммунотерапия может применяться и как отдельный вариант лечения, и в комбинации с другими препаратами.
В последнее время растет интерес к сочетанию иммуноонкологических препаратов с таргетными (то есть нацеленными против какой-то конкретной мишени в опухоли). Такие комбинации позволяют воздействовать на опухоль с разных сторон и получить эффект, превосходящий отдельное применение каждого из препаратов.
Какие побочные эффекты могут возникать?
Многие пациенты отмечают, что иммунотерапия переносится значительно лучше, чем классическая «химия», и вообще не видят никаких изменений в самочувствии. Действительно — у большинства нет таких побочных эффектов, как тошнота и рвота, слабость, падение показателей крови. Тем не менее нельзя сказать, что иммунотерапия совершенно безопасна и на ее фоне не могут возникнуть какие-то осложнения. Нет, любые медицинские вмешательства — это всегда баланс между возможными позитивными эффектами и риском осложнений.
Побочные эффекты иммунотерапии очень особенные, это связано с механизмом действия этих препаратов. В отличие от химиотерапии, они не повреждают все быстро делящиеся клетки в организме, вместо этого помогают нашей иммунной системе «найти» опухоль.
К сожалению, иногда под воздействием иммуноонкологических препаратов наша иммунная система дает сбой и начинает атаковать здоровые ткани. Например, если после проведения иммунотерапии организм начнет воспринимать клетки кишечника как чужеродные, то может возникнуть колит — воспаление толстой кишки, которое проявляется диареей, появлением крови в кале, болью в животе.
Чаще всего при иммунотерапии страдают кожа, щитовидная железа и кишечник. При этом фактически любой орган может стать мишенью иммунной системы. Например, если при проведении такого лечения иммунитет начинает воспринимать мышечные клетки сердца как чужеродные, то возникает миокардит, то есть воспаление сердечной мышцы. Это очень опасное состояние, которое без лечения может привести к гибели человека.
К счастью, тяжелые побочные явления встречаются достаточно редко, и, как правило, при непосредственном введении препаратов никаких осложнений не бывает. Только иногда могут возникать «инфузионные реакции» — аллергические реакции на препарат. Проявляются они повышением температуры тела, ознобом, иногда затруднением дыхания. В большинстве случаев с такими реакциями справиться легко, и это не противопоказание для дальнейшего лечения.
Иммунотерапия — это дорого? Можно ли получить такое лечение бесплатно?
В целом иммунотерапия — дорогой вариант лечения. Например, цена за один флакон препарата «Китруда» (международное название — «Пембролизумаб») составляет около 180000 рублей, при этом для проведения каждого цикла лечения необходимо 2 флакона, а циклы повторяются каждые 3 недели.
Но очень важно сказать, что сейчас многие иммуноонкологические препараты в России можно получать бесплатно, по полису ОМС. Год от года они становятся все доступнее в связи с увеличением количества показаний для такой терапии, а также со снижением цены. Отчасти помогает и возможность введения меньших доз некоторых препаратов, при этом эффективность лечения не уменьшается.
С каждым годом появляется все больше аналогичных препаратов от разных фармакологических компаний (речь идет не о дженериках — лекарствах, которые содержат такое же действующее вещество, как и оригинальный препарат, но выпускаются другой фирмой, а именно о новых препаратах). Многие из них могут назначаться в одинаковых клинических ситуациях. Это дополнительно повышает доступность иммунотерапевтического лечения — даже если в клинике нет одного препарата, можно назначить аналог, который зачастую никак не уступает в эффективности.
Иммуномодуляторы тоже могут быть иммунотерапией?
Очень похоже на «иммунотерапию» звучит слово «иммуномодуляторы». К этой группе препаратов относятся различные растительные средства, интерфероны, биологически активные пептиды и многие другие схожие лекарства. В теории они должны улучшать состояние иммунной системы и помогать организму бороться с опухолями. К сожалению, пока это остается только теорией.
Качественных исследований, которые бы подтвердили, что применение таких препаратов приводит к улучшению каких-либо результатов лечения (например, снижает вероятность рецидива заболевания), нет.
Хотя тут легко может возникнуть небольшая путаница. В некоторых случаях действующее вещество в иммуномодуляторах называется так же, как и в настоящих противоопухолевых препаратах. Например, интерферон: он может быть иммуномодулятором, но при этом также существует как противоопухолевый препарат для лечения меланомы и опухолей почек.
Отличие заключается в том, что разные препараты интерферона используются в совершенно разных концентрациях, имеют разный путь введения, разные побочные эффекты, и в конце концов их влияние на организм и опухоль тоже очень разное.
Кроме того, иммунотерапевтические препараты вводятся под контролем врача в онкологических клиниках, а не продаются в аптеках как иммуномодуляторы.
Нужно ли укреплять иммунитет во время лечения?
Для онкологических пациентов важно поддерживать здоровый образ жизни. Адекватные физические нагрузки (нужно стремиться примерно к 150 минутам физической активности в неделю и пытаться проходить хотя бы 8-10 тысяч шагов в день, но с поправкой на свое самочувствие), полноценное питание, здоровый сон и отказ от вредных привычек помогают лучше переносить лечение, снижают риски побочных явлений, а при их возникновении врачам становится легче с ними справиться. Но надо понимать, что это происходит не потому, что иммунитет лучше работает, а потому что это укрепляет организм в целом и дает ему ресурсы и силы.
Во время лечения онкологических заболеваний может повышаться риск инфекционных заболеваний. Например, при проведении химиотерапии нередко снижаются показатели крови, ответственные за борьбу с инфекциями (лейкоциты и нейтрофилы).
Это одно из типичных побочных явлений любой химиотерапии. Чтобы предотвратить присоединение инфекции в такой ситуации, могут быть назначены специальные лекарства, которые поддерживают уровень лейкоцитов и нейтрофилов. Но делать это необходимо не всегда, а только по рекомендации лечащего врача — в зависимости от того, есть ли высокий риск критического падения показателей крови и возникала ли инфекция на фоне низких нейтрофилов в предыдущих циклах лечения.
В интернете можно найти много способов укрепления иммунитета, например применение отвара из чистотела или смеси из чеснока с лимоном. Все подобные способы не имеют под собой хорошей научной основы, поэтому наиболее вероятно, что они никак не влияют на процесс лечения онкологических заболеваний. Поэтому не надо стараться найти любые возможности «улучшить» работу иммунной системы.
Наш иммунитет — сложная и очень тонко налаженная система, попытки вмешаться в нее зачастую не имеют предсказуемого результата, особенно во время лечения онкологических заболеваний.
Кроме того, некоторые способы повышения иммунитета предполагают употребление в том или ином виде различных растительных препаратов или настоек. Такие средства могут влиять на эффективность других лекарств, а также вызывать побочные эффекты, схожие с побочными эффектами противоопухолевых препаратов. Поэтому если возникает желание прибегнуть к такой дополнительной «естественной» терапии, то крайне важно обсудить это с врачом, чтобы он мог проверить совместимость с проводимым лечением, а также понимал дополнительные причины возможных нежелательных явлений.
Что нужно запомнить
- Острые респираторные вирусные инфекции (простуды) не влияют на риск развития рака: он повышается только при значительном снижении иммунитета. Кроме того, никакие «иммунограммы» не помогают спрогнозировать развитие онкозаболеваний, за редким исключением.
- Злокачественные клетки способны ускользать от иммунитета, и благодаря этому опухоль может длительное время развиваться, не будучи замеченной организмом. Иммуноонкологические препараты — прежде всего ингибиторы контрольных точек — помогают иммунной системе увидеть опухоль и заново начать с ней бороться.
- Иммунотерапию сейчас активно применяют при раке легкого, меланоме, опухоли почки, а также при опухолях головы и шеи, раке шейки матки. При этом такие препараты назначают на разных стадиях онкологического заболевания, а не только в ситуации, когда опухоль дала метастазы в другие органы.
- Иммунотерапия может применяться и как отдельный вариант лечения, и в комбинации с другими препаратами — например с таргетными. Это позволяет воздействовать на опухоль с разных сторон и получить лучший эффект. Метод введения иммунотерапии — внутривенный, то есть это обычные капельницы.
- Большинство пациентов переносят такое лечение легко. Однако побочные эффекты тоже есть: иногда под воздействием иммуноонкологических препаратов иммунная система начинает атаковать здоровые ткани. К счастью, это происходит редко, и врачи умеют с этим бороться.
- Иммунотерапия подходит не всем. Врач подскажет, какие анализы провести, чтобы понять, будут ли такие препараты эффективны. Некоторым пациентам иммунотерапию не назначат из-за высокого риска побочных явлений.
- В целом иммунотерапия — это дорогой вариант лечения. К счастью, сейчас многие иммуноонкологические препараты в России можно получать по полису ОМС. Кроме того, с каждым годом появляется все больше аналогов, которые зачастую никак не уступают друг другу в эффективности.
- Важно не путать иммунотерапевтические препараты с иммуномодуляторами — пока их эффективность в лечении остается только теорией. Кроме того, иммунотерапевтические препараты вводятся под контролем врача в онкологических клиниках, а не продаются в аптеках как иммуномодуляторы.
- Наш иммунитет — сложная и очень тонко налаженная система, поэтому не надо «улучшать» ее работу, особенно во время лечения. Онкологическим пациентам важно поддерживать здоровый образ жизни. А вот прием растительных препаратов или настоек нужно обсудить с врачом, чтобы не навредить себе.
Что еще почитать:
- Лекарства против рака: как получить бесплатно и что делать, если возникнут сложности.
- «Поиск наилучшего решения»: что такое второе мнение в онкологии и зачем его получать.
- Большой раздел о видах лекарственного лечения в «Онко Вики» — онлайн-справочнике с ответами на большинство вопросов про рак.
Важные контакты:
Бесплатная онлайн-справочная «Просто спросить» для онкологических пациентов и их близких. Специалисты помогут узнать больше о диагнозе, корректности назначенной схемы лечения, необходимых обследованиях и возможностях медицинской помощи в вашем регионе.
Новые методы лечения рака
По данным Минздрава РФ, только в 2018 году в мире было зарегистрировано около 18 миллионов новых случаев рака и других злокачественных новообразований. Всемирная организация здравоохранения (ВОЗ) утверждает, что с онкологическими заболеваниями сталкивается каждый пятый мужчина и каждая шестая женщина.
Новые методы лечения рака позволяют помочь пациентам, которые ранее могли рассчитывать только на паллиативную помощь.
Люди, далекие от медицины и сами врачи связывают терапию онкологических заболеваний с массивными, калечащими операциями, изнуряющей химиотерапией, которая переносится тяжелее, чем сами симптомы болезни, долгим восстановлением и постоянным страхом, что болезнь вернется.
Критерием эффективности лечения рака считают так называемую пятилетнюю выживаемость. Этот отрезок времени отмеряют от момента обнаружения онкологического процесса. Он связан с тем, что в данные сроки возникает наибольшее число рецидивов опухоли. ВОЗ отмечает, что ранняя диагностика и успешное лечение в последние годы «подарили» до 5 лет жизни почти 44 миллионам пациентов.
Как развивается рак
Клетки организма размножаются делением и начинают умирать после 50-52 циклов. Процесс естественной гибели называется апоптоз. Зараженные вирусом, мутирующие клетки выставляют на своих оболочках специальные маркеры. Их распознает и немедленно уничтожает иммунная система. Соседние клетки утилизируют продукты распада.
В организме человека ежедневно возникает угроза появления и воспроизведения «неправильных» клеток. Заболевание возникает только при нарушениях со стороны иммунитета или внутриклеточных механизмов регуляции.
Бесконтрольное размножение приводит к тому, что клетки не успевают созревать, утрачивают свои свойства. Они распространяются в окружающие ткани или мигрируют с кровью, лимфой, образуя метастазы. Канцерогенез — процесс перерождения обычных клеток в атипичные.
Как работает традиционное лечение
Стандартные современные методы лечения рака направлены на уничтожение опухоли различными способами:
- оперативное вмешательство;
- введение химиопрепаратов;
- лучевая или радиотерапия
- иммунотерапия
При хирургическом лечении врач удаляет массив атипичных клеток. К недостаткам метода относят невозможность убедиться на месте, что рак удален в полном объеме, и сложность проведения операции в труднодоступных местах.
Во время химиотерапии пациент получает лекарства, которые нарушают жизнедеятельность, тормозят размножение клеток опухоли или стимулируют их апоптоз. Препараты воздействуют и на здоровые ткани организма, что ухудшает переносимость лечения. У ряда пациентов рак может и не реагировать на стандартные средства.
Радиотерапия борьба с опухолью различными видами излучения. Она повреждает ДНК быстро делящихся клеток, приводя к их гибели. Недостаток метода заключается в невозможности прицельного воздействия только на патологический очаг.
Чтобы стандартное лечение помогло пациенту, необходимо стечение обстоятельств:
- небольшой размер и хорошая доступность первичной опухоли,
- низкая злокачественность и хороший ответ на препараты,
- хорошая переносимость курса терапии.
А как же быть тем, чья история борьбы с раком осложнена отягчающими обстоятельствами? В области онкологии новости лечения связаны с преодолением стандартных проблем терапии:
- нечувствительность рака к препаратам или облучению;
- невозможность воздействия только на клетки опухоли;
- большой объем образования и риск непереносимости терапии;
- риск оставить рак на месте после операции.
Если иммунитет «растерялся»
В крови человека есть клетки, выполняющие защитную функцию. Это T и B-лимфоциты. Они помогают расправляться как с инфекционными агентами, так и с аномальными образованиями: обнаруживают, передают информацию о «преступниках», ликвидируют угрозу и сохраняют в памяти сведения о контакте. На оболочках клеток организма находятся рецепторы, которые сигнализируют иммунитету, все ли с ними в порядке. Зараженные вирусами или атипичные образования подлежат уничтожению.
Маркировка опасных раковых клеток
Если иммунная система пропускает начало опухолевого процесса, болезнь прогрессирует. Раковые клетки действуют хитростью, маскируя свои рецепторы специальными белками.
Микробиологи изобрели так называемые моноклональные антитела. Это белковые молекулы, имеющие сродство только к определенным рецепторам. Антитела связываются с раковыми клетками, не только делая их видимыми для иммунной системы, но активируя их уничтожение.
Моноклональные антитела созданы для молекул, отвечающих за развитие разных заболеваний. Этот принцип лег в основу таргетной (прицельной) терапии. Например, препарат Ритуксимаб эффективен при лечении B-клеточных лимфом, Цетуксимаб для борьбы с раком толстой и прямой кишки, опухолями головы и шеи. Бевацизумаб применяют при опухоли молочной железы, толстого кишечника, головного мозга и немелкоклеточном раке легких.
Эти медикаменты доступны и в России. Первое время их производством занимались только иностранные компании. Пациенты с нечувствительностью к стандартной химиотерапии могли опасаться, что препарат не придет вовремя или будет стоить дороже. С 2012 года российская компания Biocad производит биоаналоги: Гертикад, Авегра, Ацеллбия.
CAR-T – найти и уничтожить
Генная терапия помогает организму бороться с опухолью посредством модифированных T-лимфоцитов. Их готовят индивидуально. Из крови пациента выделяют нужные клетки, а в структуру ДНК встраивают рецептор, состоящий из нескольких частей. Его внеклеточная часть на оболочке распознает раковые клетки. Внутриклеточная область активизирует другие звенья иммунитета. За счет этого происходит уничтожение опухоли. «Отработавшие» лимфоциты не погибают, а продолжают поиски новых клеток.
Универсальный рецептор на поверхности позволяет настраивать иммунитет против разных опухолевых антигенов. T-клетки легко проникают внутрь раковой опухоли. Так CAR-T позволяет уничтожать самые мелкие метастазы в головном и спинном мозге, снижая риск рецидива. Генную терапию считают более эффективной по сравнению с моноклональными антителами.
Достижения иммунной терапии
Среди последних новостей в онкологии – официальное разрешение американской федерации FDA на применение CAR-T в борьбе с B-клеточными лимфомами. Препарат Yescarta — лишь второе такое средство за всю историю генной терапии.
Ученые доказали, что применение моноклональных антител в комплексе с CAR-T – один из самых эффективных методов лечения рака у пациентов с плохой переносимостью и резистентностью к традиционной химиотерапии. Так у пациентки с 4 стадией карциномы молочной железы уменьшился в объеме первичный очаг и его метастазы.
В 2018 году Нобелевская премия за метод лечения рака была присуждена двум ученым Джеймсу Эллисону (США). Их исследования продолжались более 20 лет и привели к открытию белка PD-1 и рецепторов CD152 на лимфоцитах, мешающих иммунитету находить и уничтожать раковые клетки. Затем ученые синтезировали препараты, которые решают эту проблему. В перспективе средства позволят увеличить выживаемость при опухолях различной локализации, в том числе при наличии метастазов.
Эти новые методы лечения рака доступны и в России. Среди зарегистрированных зарубежных препаратов: Китруда, Ервой, Тецентрик.
Диагностика и лечение с помощью света
Отделение злокачественной опухоли от здоровой ткани представляет определенные сложности. Травмы новообразования при операции и сохранение в организме «забытых» клеток может стимулировать рост и метастазирование опухоли. Так в 2017 году хорошей новостью в лечении рака стало открытие профессора Хайинь Лю из Мичиганского технологического университета. Химик обнаружил антитела, которые при введении в организм прикрепляются только к раковым клеткам и заставляют их светиться в инфракрасном диапазоне. Очаги опухоли хорошо заметны на фоне здоровых тканей, имеющих зеленоватое или синеватое свечение. Этот метод стали применять для ревизии операционного поля и окружающих лимфоузлов во время операции.
Фотодинамическая терапия основана на использовании светочувствительных веществ (фотосенсибилизаторов) и лазерной установки. Их молекулы поглощают кванты света, уничтожая раковые клетки и разрушая сосуды, питающие опухоль. Невозможность прицельного воздействия лазера позволяла применять его только для видимых кожных опухолей.
Однако изобретение ученых в московском университете НИТУ «МИСиС» позволило преодолеть это ограничение. Они соединили молекулу фотосенсибилизатора с контрастным агентом. Так в конце 2018 года был получен инструмент, помогающий использовать фототерапию для рака другой локализации. Новое в лечении онкологии в 2019 году — это возможность отслеживать границы опухоли и концентрацию фото-лекарства в пораженном органе с помощью МРТ.
Нижегородские ученые синтезировали флуоресцентный белок, который позволяет обнаруживать клетки опухолей. В 2012 году они получили патент на воспроизведение пептида, уничтожающего рак шейки матки в поле лазера.
Прицельное воздействие на опухоль
Радиотерапия сопряжена с риском получения массивного облучения. Во время лечения повреждаются не только раковые, но и здоровые клетки. К самым сложным локализациям опухоли относят голову и шею ввиду опасности повреждения головного мозга и крупных сосудов. Поражение зрения, слуха неизбежно снижает качество жизни пациента. Кроме того, до ряда опухолей нельзя добраться хирургическим путем.
Уничтожить такой рак помогает стереотаксическая гамма-терапии (или гамма-нож). Лучевые диагносты определяют точную локализацию и размеры образования, после чего в патологический очаг направляют до 200 лучей из разных точек. Единственная процедура занимает несколько часов и дает результат, сопоставимый с 30 сеансами облучения.
Гамма-нож – неинвазивная хирургическая процедура, которая позволяет пациентам возвращаться домой в день ее проведения. В 2019 году в России действует 6 установок, позволяющих помочь 3 тысячам пациентов в год. Новости онкологии в этой области обнадеживают онкобольных перспективами открытия 20 таких центров в стране.
В 2018 году сотрудники филиала «НМИЦ радиологии» Минздрава в г. Обнинске сконструировали портативные нейтронные генераторы на базе гамма-излучателей. Нейтронное излучение в онкологии применяется более 40 лет. Однако необходимость строить для оборудования отдельные здания и возможность пролечить не более 10 человек в день существенно ограничивали применение генератора. Компактные приборы решают эту проблему.
Снизить повреждение окружающих тканей возможно благодаря замене рентгеновского излучения на протонное. Оно лучше концентрируется в очаге. В 2018 году немецкие ученые из Центра им. Гельмгольца Дрезден-Россендорф успешно соединили протонную терапию с МРТ-сканером. Ранее визуализацию опухолей выполняли с помощью компьютерной томографии, на которой хорошо отображаются только неподвижные костные образования. Среди новостей в лучевом лечении рака в 2019 году – создание прибора, позволяющего ввести протонное облучение в клиническую практику.
Экспериментальное лечение рака
Внедрение новых методик терапии возможно благодаря клиническим исследованиям. В ходе экспериментального лечения используются методы, эффективность и безопасность которых полностью не изучена. Онкологи проводят набор пациентов с определенным заболеванием. Они полностью обследуют кандидатов и отсеивают тех, кто не подходит по состоянию здоровья.
Лица, прошедшие скрининг, получают бесплатную экспериментальную терапию. К ней относят:
- генное лечение;
- локальное замораживание тканей;
- точечный нагрев тканей;
- применение бактерий-анаэробов;
- вакцины против рака;
- лечение лазером;
- нанотехнологии.
Участие в клинических исследованиях дает шанс выйти в ремиссию пациентам, которым не помогают стандартные схемы лечения.
Можно ли считать, что экспериментальная терапия позволяет победить рак? Исследователи рассказывают о протоколах с ошеломляющими результатами. Так при испытании препарата Китруда в 2013 году около 76% участников почувствовали облегчение, а полностью излечилось от рака около 20%. Так препарат был включен в схемы лечения различных агрессивных опухолей.
При обнаружении немедленных или отсроченных негативных последствий протоколы закрывают, а средства или методы не допускают до рутинной практики.
С 2018 года работает сервис, позволяющий онкологам России искать больницы, в которых проводят экспериментальную терапию, и направлять туда пациентов. Он создан непосредственно Агентством клинических исследований и Российским онкологическим обществом RUSSCO.
Ученые разных стран объединяются в интересах пациентов. Так 19 февраля 2019 года на базе филиала ФГБУ «НМИЦ радиологии» Минздрава России состоялся первый семинар по регенеративной медицине. Отрасль находится на стыке биологии, инженерии и лечебной деятельности. Регенеративная медицина помогает восстанавливать поврежденные, удаленные ткани за счет стволовых клеток пациентов, трансплантации или имплантации биоматериалов.
Специалисты в области клинической иммунологии, радиологии, регенеративных технологий из России принимали японских коллег. Трансляция семинара позволила коллегам из 38 регионов получить актуальную информацию о применении новых дендритно-клеточных вакцин от рака, культивировании стволовых клеток с помощью роботов, инженерных методиках.
Кроме того, среди новостей онкологии 2019 года в России — успешное внедрение органосохраняющих операций при раке легких и эндоскопическое удаление новообразования желудка и толстого кишечника.
К сожалению, онкологи до сих пор не располагают «волшебной таблеткой» от всех видов опухолей. Рак остается заболеванием с высокой летальностью. Однако современные изобретения в этой области помогают подарить жизнь и здоровье все большему числу пациентов.
Когда пациент впервые начинает лечить злокачественное образование, то он сталкивается с мифами, о которых прочитал в Интернете или услышал от знакомых. В результате человек не понимает, что в этой, часто противоречивой, информации является правдой, а чему верить нельзя. Разберемся, что на самом деле можно и чего нельзя пациенту во время лекарственного лечения рака.
Напомним, существуют четыре принципиально разных варианта лекарственного лечения:
- Химиотерапия. Действует на все активно делящиеся клетки.
- Таргетная терапия. Действует целенаправленно на определённые молекулы.
- Иммунотерапия. Не действует напрямую на опухоль, но заставляет наш иммунитет убивать злокачественные клетки.
- Гормональная терапия. Применяется при гормонально чувствительных опухолях. Она не уничтожает опухолевые клетки, но может надолго затормозить их рост и взять заболевание под контроль.
Миф № 1. Опухоль питается глюкозой и это заставляет ее расти все больше и больше. Поэтому при лечении рака, нельзя есть сладкое: печенье, конфеты и пирожные.
Это самый распространенный миф, связанный с питанием во время лекарственной терапии. На самом деле, все клетки нашего организма питаются глюкозой, в том числе головной мозг. Но все-таки сахаросодержащие продукты следует употреблять в ограниченном количестве, как и всем людям.
Все хорошо в меру и строгих ограничений нет, но нужно помнить, что избыточное потребление сахаросодержащих продуктов может привести к ожирению, а ожирение – это как раз фактор риска развития нескольких видов злокачественных образований. Поэтому нужно все делать с умом.
Миф № 2. Во время лекарственного лечения рака необходимо придерживаться строгой диеты.
В питании онкологических пациентов есть свои правила. В основном, все они направлены на то, чтобы избежать инфекции, потому что лекарственная терапия снижает иммунитет. Поэтому рекомендуется не употреблять в пищу сырую или слегка приготовленную рыбу, суши, мягкие сыры, созревшие с плесенью, неохлаждённые кондитерские изделия с кремовой начинкой. Разрешается пастеризованное молоко, йогурты, сыр или другие молочные продукты, яйца должны быть сварены только вкрутую.
Также рекомендуется мыть руки теплой водой с мылом в течение 20 секунд до и 20 секунд после приготовления пищи и перед едой. Использовать размороженные продукты сразу и не подвергать их повторной заморозке. Пить воду только из городских или муниципальных водопроводных сетей или бутилированную воду.
Миф № 3. Красное вино помогает лечить рак.
Доказано, что алкоголь во время лекарственной терапии может увеличить риск побочных эффектов. Употребление алкоголя может повлиять на способность печени правильно метаболизировать токсины. Многие химиопрепараты выводятся через печень, она же утилизирует алкоголь, поэтому при употреблении спиртного печень испытывает двойную нагрузку. Если у пациента имеется оральный мукозит (отек или язвочки во рту), то употребление алкоголя может значительно усугубить этот побочный эффект.
Миф № 4. Онкологическим пациентам курение не вредно, а даже в какой-то степени полезно – помогает успокоиться.
Конечно, это неправда. Курение также может усугубить побочные эффекты проводимого лечения и снизить эффективность лекарственных препаратов. Также не надо забывать, что курение повышает риск развития рака других локализаций.
Миф № 5. Травяные и витаминные добавки помогут справиться с раком.
Чаще всех травяные добавки используют пациенты пожилого возраста. Но применять их во время лечения мы не рекомендуем, так как некоторые добавки могут не только изменить эффективность терапии, но и повысить токсичность лекарств.
Такие растительные добавки как эхинацея, куркумин, зверобой, корень валерианы могут нарушить баланс токсичности и эффективности химиотерапии. Сок алоэ-вера может уменьшать всасывание химиотерапевтических препаратов или вызывать диарею (понос). Имбирь и чеснок могут мешать действию антикоагулянтов (препаратов, препятствующих свертыванию крови), увеличивая риск кровотечения.
Кроме того, многие детокс-программы, антиоксидантные добавки могут сделать лекарственную и лучевую терапию менее эффективными.
Необходимо помнить, что некоторые химиотерапевтические препараты натурального происхождения. Например, препараты винорельбин, винбластин – это производные барвинока розового. Паклитаксел, доцетаксел – производные тисового дерева.
Самое лучшее, чем можно помочь своему организму, это более-менее правильно и сбалансированно питаться, чтобы обеспечить свой организм необходимыми макро- и микронутриентами. Принимать мультивитаминные комплексы нужно только по показаниям при дефиците определенных витаминов, и только с разрешения лечащего врача.
Обязательные вопросы, которые нужно задать своему врачу перед прохождением лекарственного лечения:
— Каким образом взаимодействуют препараты, которые назначил врач-онколог, с какими-либо другими лекарствами (например, уже по сопутствующей патологии)?
— Какие продукты необходимо исключить из рациона, а какие, наоборот, стоит употреблять чаще во время лекарственного лечения рака?
— Какие витамины нужно принимать в процессе лечения?
Миф № 6. Во время лекарственного лечения рака противопоказаны физические нагрузки.
На эту тему проводилось много исследований и все они показали, что физическая активность улучшает не только общее соматическое состояние пациента, но и психическое состояние.
Силовые тренировки приводят к уменьшению мышечной слабости, увеличению мышечной массы и, следовательно, мышечной силы.
Физические упражнения могут поспособствовать снижению артериального давления.
Но необходимо помнить, что и здесь имеются противопоказания. Пациентам с лимфостазом, тем, кто перенес операцию, некоторые виды активности могут быть противопоказаны. Поэтому важно сначала проконсультироваться со своим лечащим врачом.
Миф № 7. Во время лекарственного лечения нельзя делать массаж.
Доказано, что массаж может облегчать тошноту, уменьшать боль, снижает беспокойство, усталость, стресс и улучшает качество сна. Но необходимо помнить, что массаж безопасен только для пациентов в ремиссии. В остальных случаях, особенно в период активного лекарственного лечения, нужно проконсультироваться у лечащего онколога. Как правило, допускается только поверхностный массаж. Массажист должен иметь опыт работы с онкологическими пациентами, так как, к примеру, у пациентов на химиотерапии может быть снижено количество тромбоцитов. Это чревато тем, что при активном глубоком массаже может возникнуть риск возникновения гематом (кровоизлияний в подкожную клетчатку).
Во многих больших онкологических учреждениях для пациентов созданы реабилитационные центры, куда можно обратиться за помощью. Специалисты посоветуют, как поддержать свой организм и наиболее эффективно, безопасно пройти лечение.
Отдельно необходимо сказать про стоматологические процедуры. Перед началом любой лекарственной терапии пациентам рекомендуется провести санацию полости рта. А вот проводить плановые стоматологические вмешательства во время лечения лучше не стоит по одной причине – у пациента могут быть снижены какие-то показатели крови. Это может вызвать кровотечение, присоединение инфекций. Если все-таки возникла острая ситуация, то необходимо сообщить об этом лечащему онкологу, сдать клинический анализ, и предупредить стоматолога о том, что проводится лечение онкологического заболевания.
Миф № 8. При лечении рака нельзя выходить на солнце.
Нужно помнить, что некоторые препараты делают кожу более восприимчивой, более чувствительной к солнечному излучению. Но каких-то особых рекомендаций для онкопациентов нет. Правила общие для всех. Использовать солнцезащитный крем с SPF не менее 30. Обязательно носить головной убор и закрывать одеждой участки тела, которые подвергаются солнечному воздействию.
Миф № 9. Во время лечения нельзя летать на самолетах.
Запрет на авиаперелет в основном касается пациентов, которые перенесли оперативное лечение, например, большую полостную операцию, где есть риск повышения внутрибрюшного давления. Это может неблагоприятно сказаться на пациенте.
Если человек перенес трансплантацию костного мозга или стволовых клеток за последний год, ему также стоит отказаться от авиаперелета из-за возможного риска присоединения инфекции.
У пациентов с низким уровнем тромбоцитов или эритроцитов в крови перелет может спровоцировать кровотечение.
Поэтому, если планируется перелет, лучше всего проконсультироваться с лечащим онкологом.
Миф № 10. Во время лечения нельзя красить волосы, делать маникюр и педикюр.
Противопоказаний к тому, чтобы красить волосы во время лечения, нет. Но, так как краски имеют разный химический состав, стоит проконсультироваться со своим врачом.
При маникюре и педикюре лучше избегать агрессивного воздействия аппаратного обрезания, используя щадящие методики.
Отдельная тема – косметологические процедуры. Чистки, пилинги рекомендуется отложить до конца лечения, так как они могут привести к ненужному повреждению кожных покровов, присоединению инфекций, образованию гематом. Поэтому, выбирайте проверенные клиники, грамотных специалистов с высшим медицинским образованием и перед началом косметологической процедуры посоветуйтесь со своим лечащим онкологом.
Читайте также: Особенности вакцинации онкологических пациентов: рекомендации для детей и взрослых
Новые методики лечения рака уже позволили довести выживаемость пациентов на ранних стадиях до значений, приближающихся к 100%. Но и четвертая стадия рака, когда опухоль метастазировала в другие органы, больше не является синонимом терминальной стадии заболевания. Какие подходы способны сделать лечение метастазов эффективным, и в каких случаях есть вероятность полностью вылечить метастатический рак, — в материале Онкологической клиники МИБС.
Еще два-три года назад метастатический рак любой локализации считался практически инкурабельным (неизлечимым). Системная химиотерапия с серьезными побочными эффектами и паллиативная лучевая терапия для снижения болевого синдрома — вот тот минимум, на который могли рассчитывать пациент и его родственники. Развитие медицины привело к развитию технологий и объединению усилий различных методов при лечении одного пациента. Но обновился не только арсенал доступных врачам средств и методик. Анализируя внушительные объемы результатов проводимых по всему миру исследований, ученым удалось подтвердить существование особой формы течения метастатического рака — “ограниченное системное метастазирование” (олигометастазы).
Что такое олигометастатическая болезнь?
В упрощенной форме особое течение опухолевого процесса можно описать как небольшое количество отдельных метастазов, распространившихся не по всему организму, а сконцентрированных в одном-двух органах (олигометастазы). То есть, имеет место олигометастатическое поражение или олигометастатическая болезнь. Дальнейшее изучение показало, что при адекватном лечении первичной опухоли и локальном лечении метастазов удается добиться даже полного выздоровления. Одновременно резко повышается качество жизни пациента, так как отсутствует мощное системное воздействие на организм (химиотерапия), и связанные с ним побочные эффекты.При каких видах рака чаще всего возникают олигометастазы?
Современная статистика в онкологии относит к олигометастатическому поражению случаи, в которых выявляется не более пяти метастазов, из них не менее трех — в одном органе. По этому критерию статистика США (как наиболее полная) показывает наличие около 90 тысяч новых случаев олигометастатического рака ежегодно. Ведущий “источник” олигометастазов — рак легкого (около 56%), вторую и третью позиции занимают рак молочной железы и колоректальный рак (по 16%). Более подробная работа над совершенствованием критериев определения олигометастатического процесса может изменить соотношения, но и эти цифры близки к статистике успешных случаев лечения олигометастазов, наблюдаемой в клинической практике.
Лечение олигометастазов — важна синергия
Важнейшим этапом лечения олигометастатической болезни является адекватная терапия первичной опухоли. Хирургия, радиочастотная абляция, радиохирургия позволяют избавиться от первичной опухоли, чтобы избежать появления новых метастазов, кроме тех, которые уже были диагностированы.
Наиболее эффективно лечение олигометастазов, в котором объединяются усилия высокотехнологичных методов. В первую очередь, радиохирургии, которая позволяет разрушить метастаз, независимо от его расположения, не прибегая к хирургическому вмешательству, сохраняя окружающие ткани. Онкологическая клиника МИБС имеет возможность и подтвержденный опыт лечения олигометастазов рака молочной железы в головной мозг, олигометастатического течения немелкоклеточного рака легких и других внечерепных локализаций (радиохирургия на Кибер-ноже или высокоточном линейном ускорителе TrueBeam STx). Сочетание радикальных методик с системным воздействием (химиотерапией и, особенно, таргетной терапией) позволяет добиться лучших результатов, чем применение каждого из методов по-отдельности.
Поэтому в Онкологической клинике МИБС подразделения лучевого лечения активно взаимодействуют с отделением медикаментозного лечения, и собственной морфологической лабораторией, без которой таргетная терапия не имеет смысла.
Свои особенности имеет лечение олигометастатического колоректального рака в печень: и первичная опухоль, и олигометастазы могут быть удалены в рамках одного хирургического вмешательства. Но и в этом подходе все шире применяется радиочастотная абляция, как альтернатива хирургии в удалении части опухолевых тканей. Хирургическое лечение олигометастазов также может быть проведено в хирургическом отделении клиники МИБС.
Эффективность лечения олигометастазов
Комплексный подход позволяет излечить полностью 25-30% заболевших. А при метастазах РМЖ возможно взять под контроль, по данным разных исследований, до 89-97% опухолей.
Перспективы лечения олигометастатической болезни
Как показывает практика, лечения олигометастатического рака может быть успешным не только при хорошо изученных заболеваниях (рак кишки, рак легкого, молочной железы), но и при других вариантах опухолей. Этот подход необходимо начинать активно использовать. По мере набора материалов, критерии определения клинического случая, как олигометастатического рака (количество очагов, органы поражения), будут уточняться.
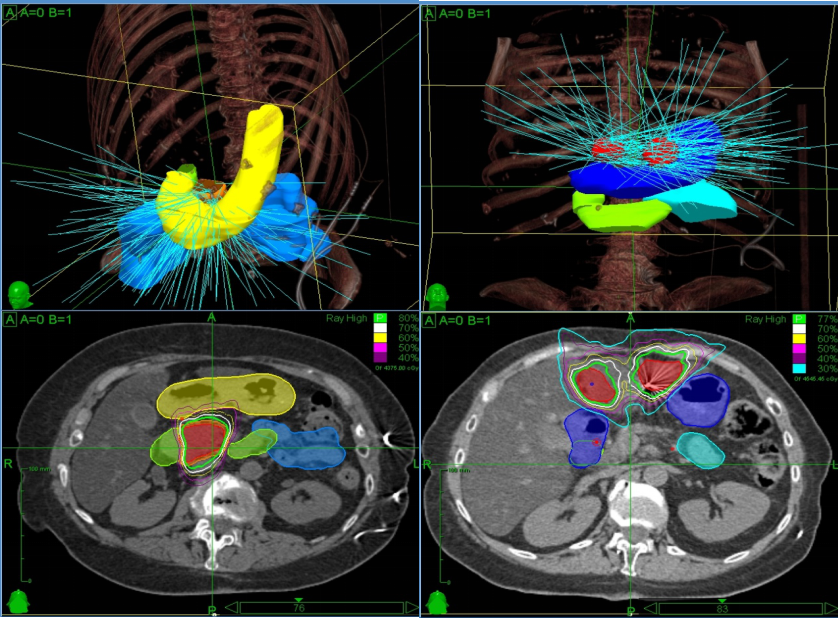
Эту гипотезу подтверждает и опыт Онкологической клиники МИБС: у нас есть случаи успешного лечения четвертой стадии рака. В том числе, такого агрессивного заболевания, как рак поджелудочной железы с олигометастатическим поражением печени (радиохирургия была применена как для первичной опухоли, так и для метастазов, пациентка наблюдается пять лет без прогрессии опухоли).
Радиохирургическое лечение олигометастазов и первичного рака поджелудочной железы на Кибер-ноже (скриншот плана лечения Онкологической клиники МИБС). Высокую дозу облучения получили зоны внутри красного контура, здоровые органы не повреждаются
Этот же пример иллюстрирует высокий потенциал расширения применения неинвазивных методов разрушающего воздействия. Например, два-три крупных олигометастаза рака груди в головной мозг можно попытаться удалить хирургическим путем. Но гораздо безопаснее, быстрее и дешевле (если считать не только стоимость операции, но и стоимость восстановления после хирургии) провести лечение олигометастазов в головной мозг Гамма-ножом. Знание врачом-маммологом (как и хирургом любого иного профиля) современных методик комплексного подхода к лечению олигометастазов открывает новые возможности для пациентов старшей возрастной группы и для тех, чье общее состояние не позволяет провести хирургическое вмешательство.
Залогом эффективной работы онкологической клиник является постоянное развитие специалистов, отслеживание, тестирование и внедрение новых методик лечения.
Отдельно следует выделить потенциал сочетания иммунотерапии с лучевыми методами. Чтобы “сработала” иммунная терапия, опухоль должна быть распознана иммунной системой. А лучевая терапия обладает способностью давать иммунной системе распознать опухоль — при облучении погибают опухолевые клетки, новые белки выходят из погибших клеток, их опознает иммунная система, начинается иммунный ответ.
Такой подход уже имеет успехи в лечении ряда заболеваний (рак легкого, рак мочевого пузыря). Ожидается, что часть из них будет зарегистрирована в качестве рекомендованных подходов к лечению в ближайшем будущем.
Но уже сейчас эффективное лечение олигометастазов доступно и в России. Онкологическая клиника МИБС предлагает все передовые возможности, используемые в мировой медицине для лечения олигометастатической болезни. У нас уже более десяти лет работает отделение радиохирургии и лучевой терапии для точечного разрушения метастазов и первичной опухоли, а также для упрощения распознавания опухоли препаратами иммунотерапии; отделение малоинвазивной лапароскопической и открытой хирургии для эффективного удаления первичных опухолей; собственная морфологическая лаборатория для определения потенциально возможного применения таргетных препаратов и иммунотерапии и т.д.
С первого дня работы Онкологическая клиника МИБС верна курсу на активное участие в мировом медицинском сообществе и реализацию ведущих международных стандартов на благо пациентов из России и других стран.
Звоните, чтобы получить больше информации о возможностях клиники МИБС для помощи в Вашем случае.
Врач-онколог, врач- радиолог
Заведующий отделением протонной лучевой терапии