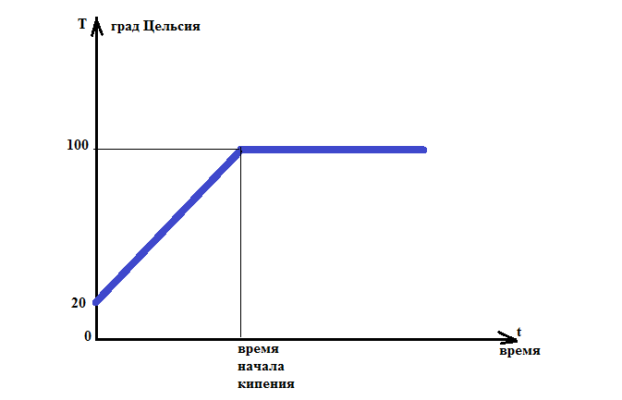
Испарение сопровождается остыванием жидкости. Чем она холоднее, тем менее интенсивно происходит образование пара. Но скорость процесса можно поддерживать, если жидкость подогревать, то есть подводить к ней тепло.
Так возникает понятие удельной теплоты парообразования. У каждого жидкости и даже твердого тела (ведь и его можно превратить в пар) эта величина своя. Рассмотрим, как найти удельную теплоту парообразования.
Содержание
- Единица измерения
- Формула для величины
- Какие данные нужны, чтобы рассчитать значение?
- Алгоритм и правила расчета
- Несколько примеров нахождения
- Таблица для ряда веществ
- Видео по теме статьи
- Заключение
Единица измерения
Удельная теплота парообразования – это величина, которая показывает, сколько теплоты необходимо сообщить веществу массой 1 кг, чтобы превратить его в пар. При этом температура вещества должна быть постоянной.
Обычно рассматриваемую величину обозначают латинскими буквами L, r или греческой λ (лямбда). Теплота в системе СИ измеряется в Джоулях (Дж), масса – в килограммах (кг). Таким образом, L измеряется в Дж/кг.
Так как теплота в джоулях принимает зачастую большие значения, может встречаться обозначения кДж (килоджоули) – Дж*1000, или МДж (мегаджоули) – Дж*1000 000.
Формула для величины

- Q – теплота,
- m – масса.
Ее часто используют для расчетов энергетических затрат на выпаривание воды из растворов: Q= L* m.
L определяют в лабораториях и заносят в таблицы, составляют справочники, которыми можно пользоваться любому желающему. При этом всегда указывают температуру и давление, при которых находилось L.
С ростом температуры L уменьшается, так как жидкость расширяется, взаимодействие между ее частицами уменьшается, и ее легче превратить в пар. Когда плотность пара и жидкости сравниваются, наступает критическое состояние.
Оно характеризуется определенным давлением и температурой. Для воды — это 374 ℃ и 218,5 атм. В таком состоянии L=0.
Какие данные нужны, чтобы рассчитать значение?
Чтобы вычислить искомую величину, применяют знания о том, что теплота испарения равна теплоте конденсации со знаком «минус». Это значит, что когда пар конденсируется (превращается в воду), он охлаждается и отдает свое тепло окружающей среде. Можно применить формулу: Q= L* m.
Для расчетов необходимы следующие данные:
- Q – теплота, отданная паром, Дж,
- m – масса образовавшейся в процессе конденсации воды, кг;
- L – удельная теплота парообразования, Дж/кг – собственно то, что нужно определить.
Применяют также закон сохранения энергии и понятие теплоемкости: Qв=С*Mв*(T2-T1), где:
- С – удельная теплоемкость воды, которая нагревается под действием сконденсированного пара, Дж/(кг*К), – считается известной и берется из таблицы,
- Mв – ее масса;
- T2-T1 – изменение температуры в Кельвинах или градусах Цельсия.
Алгоритм и правила расчета

- Анализируют, как проходит процесс, какое вещество отдает, а какое получает тепло.
- Переводят все единицы измерения в одну систему.
- Записывают необходимые формулы.
- Решают уравнение с одним неизвестным.
При проведении расчетов надо следить за размерностью величин. В системе СИ масса измеряется в кг, теплота в Дж, а температура в градусах Кельвина. Разность температур можно считать в градусах Цельсия.
Часто бывает нужно найти удельную теплоту парообразования при условиях кипения жидкости и нормальном атмосферном давлении (760 мм рт. ст.). В таких условиях получают чистую воду из растворов или выделяют из смеси веществ ее части.
Процесс используется в химической и пищевой промышленности и даже на бытовом уровне.
Несколько примеров нахождения
Задача №1. Сколько необходимо энергии для превращения в пар следующих кипящих веществ:
- 2 кг этилового спирта;
- 2 кг воды;
- 2 кг расплавленного свинца.
Необходимо воспользоваться формулой Q= L* m и взять значение L из таблицы. Получится:
- 0,84*МДж*2 кг = 1,68 МДж;
- 2,3 МДж*2 кг = 4,6 МДж;
- 8,6 МДж *2 кг = 17,2 МДж.
Как видно, превратить в пар воду сложнее, чем этанол, но легче, чем металл. На первый взгляд, это очевидно, но когда дело касается веществ, близких по температуре кипения, то разница становится менее заметна, ее невозможно угадать. Тем не менее, она имеет особое значение.
Задача №2. Как вычислить, сколько энергии необходимо, чтобы превратить 1 тонну воды при 20 ℃ в пар при 100 ℃?
Решение: 1 т = 1000 кг.

- Q1 – тепло, ушедшее на нагревание воды с 20 до 100 градусов,
- Q2 – тепло, необходимое для образования пара (процесс происходит без изменения температуры).
Q1 = С*M* (T2-T1), С воды = 4200 Дж/(кг*К), Q2 = L*M, L воды при обычном кипении = 2,3 МДж/кг, T2-T1 = 100-20 = 80.
Подставляя известные величины, находят искомую энергию: Q = 4200*1000*80+2,3 *106*1000 = 4,2*80*106+2300*106=2636 (МДж)
Задача №3. Сколько надо затратить электроэнергии, чтобы превратить 1 л воды в пар?
Решение: Q= Lводы*m. Масса 1 литра обычной водопроводной воды равна 1 кг. Q=2260 кДж/кг *1 кг=2260 кДж=2,3 МДж.
1 кВт*ч = 3,6 МДж. Из простой пропорции следует, что надо затратить 0,64 кВт*ч. Для 2-х литров величина возрастет в 2 раза, для 3-х – в три, и так далее.
Зная тарифы на электроэнергию, несложно посчитать стоимость, во сколько рублей обойдется такое кипячение. Надо также учитывать, что частично энергия уйдет в воздух и на нагрев сосуда, частей плиты, поэтому реальный расход будет выше.
Таблица для ряда веществ
Удельная теплота парообразования при нормальном атмосферном давлении (1 атм = 760 мм рт. ст.) и температуре кипения (для каждого вещества она своя).
| Вещество | L, МДж/кг | T кипения, ℃ |
| Вода | 2,3 | 100 |
| Этиловый спирт | 0,84 | 78,4 |
| Метиловый спирт | 1,1 | 64,1 |
| Ртуть | 0,28 | 357 |
| Жидкий азот | 0,2 | -195,8 |
| Аммиак | 1,4 | -33,4 |
| Фреон 12 | 0,16 | -24,9 |
| Расплавленный алюминий | 10,9 | 2450 |
Для воды при 20 ℃ L=2,45МДж/кг.
Видео по теме статьи
Об удельной теплоте парообразования расскажет видео:
Заключение
Единица измерения удельной теплоты парообразования – Дж/кг. Она показывает, сколько при заданной температуре надо подвести тепла, чтобы преобразовать 1 кг вещества в пар. Величина определяется путем проведения экспериментов.
Для воды при 100 ℃ ее значение 2260 кДж/кг. Эта величина довольно большая в сравнении с характеристиками других веществ. С ростом температуры значение удельной теплоты образования пара уменьшается.
На этой странице вы можете рассчитать количество теплоты, необходимое для превращение жидкости в пар с помощью калькулятора онлайн. Для этого необходимо ввести массу жидкости и ее удельную теплоту парообразования (см. таблицу).
Удельная теплота парообразования — физическая величина, показывающая, какое количество теплоты потребуется для превращения жидкости массой 1кг в пар без изменения температуры. Обозначается буквой L и измеряется в Дж/кг.
Содержание:
- калькулятор количества теплоты для превращения в пар
- формула количества теплоты для превращения в пар
- таблица «Удельная теплота парообразования»
- примеры задач
Формула количества теплоты для превращения в пар
{Q = L cdot m}
Q — необходимое количество теплоты для превращения жидкости, находящейся при температуре кипения в пар
L — удельная теплота парообразования (см. таблицу)
m — масса жидкости, находящейся при температуре кипения.
Удельная теплота парообразования жидкостей и расплавленных металлов при температуре кипения и нормальном атмосферном давлении
| Жидкость | Удельная теплота парообразования, кДж/кг |
|---|---|
| Азот жидкий | 201 |
| Аллюминий | 9200 |
| Аммиак | 1370 |
| Бензин | 230 — 310 |
| Висмут | 840 |
| Вода (при 0°С) | 2500 |
| Вода (при 20°С) | 2450 |
| Вода (при 100°С) | 2260 |
| Вода (при 370°С) | 440 |
| Вода (при 374,15°С) | 0 |
| Водород жидкий | 450 |
| Воздух | 197 |
| Гелий жидкий | 23 |
| Железо | 6300 |
| Золото | 1650 |
| Керосин | 209 — 230 |
| Кислород жидкий | 214 |
| Магний | 5440 |
| Медь | 4800 |
| Никель | 6480 |
| Олово | 3010 |
| Ртуть | 293 |
| Свинец | 860 |
| Спирт этиловый | 906 |
| Эфир этиловый | 356 |
| Цинк | 1755 |
Примеры задач на нахождение количества теплоты
Задача 1
Какое количество теплоты требуется для обращения в пар воды массой 0.2 кг при температуре 100°C?
Решение
Подставим значения из условия в формулу и рассчитаем результат. Удельную теплоту парообразования для воды при температуре 100°C возьмем из таблицы: L = 2260 кДж/кг.
Q = L cdot m = 2260 cdot 0.2 = 452 Дж
Ответ: 452 Дж
Проверим ответ с помощью калькулятора .
Твердые кристаллические вещества переходят в жидкое состояние посредством плавления. Чтобы расплавить вещество, необходимо сообщить ему некоторое количество теплоты. И, наоборот, при кристаллизации (переходе жидкости в твердое состояние) энергия выделяется в окружающую среду.
Проведем аналогию с переходом жидкости в пар. Этот переход может быть осуществлен двумя способами: испарением или кипением. Кипение является тем же испарением, но более интенсивным. Очевидно, что для того, чтобы происходил процесс кипения, жидкости необходимо сообщать какое-то количество теплоты. Это количество теплоты будет идти на образование пара.
На данном уроке мы познакомимся с новым определением — удельной теплотой парообразования и конденсации. Вы узнаете формулу для расчета количества теплоты, необходимого для парообразования жидкости и научитесь ею пользоваться.
Удельная теплота парообразования
Вы уже знаете, что кипение происходит при определенной для каждой жидкости температуре. Количество теплоты, которое потребуется сообщить этим жидкостям одинаковой массы для превращения их в пар тоже будет различно.
Опытным путем было выяснено следующее. Если мы возьмем воду массой $1 space кг$ при температуре $100 degree C$, то нам потребуется затратить $2.3 cdot 10^6 space Дж$ энергии для полного превращения этой воды в пар.
Температура кипения во время всего процесса остается постоянной. Следовательно, нам необходимо подводить к кипящей жидкости определенное количество теплоты. Для воды это энергия в $2.3 cdot 10^6 space Дж$.
Удельная теплота парообразования — это физическая величина, показывающая, какое количество теплоты необходимо, чтобы обратить жидкость массой $1 space кг$ в пар без изменения температуры.
- Обозначается буквой $L$
- Единица измерения удельной теплоты парообразования — $1 frac{Дж}{кг}$
- При температуре кипения внутренняя энергия вещества в парообразном состоянии больше внутренней энергии вещества такой же массы в жидком состоянии
Удельная теплота парообразования некоторых жидкостей
В таблице 1 приведены экспериментально полученные величины удельной теплоты парообразования некоторых жидкостей.
| Вещество | $L, frac{Дж}{кг}$ |
| Вода | $2.3 cdot 10^6$ |
| Аммиак (жидкий) | $1.4 cdot 10^6$ |
| Спирт | $0.9 cdot 10^6$ |
| Эфир | $0.4 cdot 10^6$ |
| Ртуть | $0.3 cdot 10^6$ |
| Воздух (жидкий) | $0.2 cdot 10^6$ |
Удельная теплота парообразования эфира равна $0.4 cdot 10^6 frac{Дж}{кг}$. Что это означает?
Возьмем $1 space кг$ эфира при его температуре кипения ($35 degree C$). Для того чтобы полностью превратить его в пар, нам потребуется $0.4 cdot 10^6 space Дж$.
Обратите внимание, что удельная теплота парообразования показывает количество теплоты, необходимое для превращения жидкости, взятой при ее температуре кипения, в пар.
Удельная теплота конденсации
Нужно ли сообщать пару энергию при его конденсации? Давайте рассмотрим простой опыт (рисунок 1).
Нальем в сосуд воду и закроем его пробкой. Через пробку проведем трубку и направим ее на кусочек охлажденного стекла. Доведем воду до кипения с помощью горелки.
Пар, поднимающийся над кипящей водой, будет конденсироваться, соприкасаясь с холодным стеклом. Если мы дотронемся до стекла, то обнаружим, что оно очень сильно нагрелось.
Так энергия пара передается стеклу. В результате этой потери энергии пар конденсируется. Если бы температура стекла была равна температуре пара, то теплопередача бы не происходила, и конденсат не образовывался бы.
Это говорит о том, что при конденсации пар отдает, выделяет энергию.
Более точные опыты также показывают, что
Конденсируясь, пар отдает то количество энергии, которое пошло на его образование.
Значит, при превращении $1 space кг$ водяного пара в воду при температуре $100 degree C$ выделяется $2.3 cdot 10^6 space Дж$ энергии.
Это довольно большая энергия, поэтому человечество стремится ее использовать. Например, на крупных тепловых электростанциях паром, который уже прошел через турбины, нагревают воду. Ее, в свою очередь, используют для отопления зданий и бытовых нужд.
Расчет количества теплоты, необходимого для парообразования
Чтобы вычислить количество теплоты $Q$, необходимое для превращения в пар жидкости любой массы, взятой при температуре кипения, нужно удельную теплоту парообразования $L$ умножить на массу $m$:
$Q = Lm$.
Из этой формулы при расчетах мы можем выражать массу ($m = frac{Q}{L}$) и удельную теплоту парообразования ($L = frac{Q}{m}$).
Для расчета количества теплоты, которое выделит пар массой $m$ при температуре кипения в ходе конденсации, используется эта же формула.
Упражнения
Упражнение №1
У вас есть вода массой $2 space кг$ с температурой $20 degree C$. Рассчитайте, какое количество энергии потребуется для ее превращения в пар.
Дано:
$m = 2 space кг$
$t_1 = 20 degree C$
$t_2 = 100 degree C$
$c = 4200 frac{Дж}{кг cdot degree C}$
$L = 2.3 cdot 10^6 frac{Дж}{кг}$
$Q — ?$
Показать решение и ответ
Скрыть
Решение:
Сначала нам потребуется нагреть воду до температуры кипения, затратив на это количество энергии $Q_1$:
$Q_1 = cm (t_2 — t_1)$.
$Q_1 = 4200 frac{Дж}{кг cdot degree C} cdot 2 space кг cdot (100 degree C — 20 degree C) = 8400 frac{Дж}{degree C} cdot 80 degree C = 672 space 000 space Дж approx 0.7 cdot 10^6 space Дж$.
Теперь рассчитаем количество энергии $Q_2$, затраченное для превращения воды в пар:
$Q_2 = Lm$.
$Q_2 = 2.3 cdot 10^6 frac{Дж}{кг} cdot 2 space кг = 4.6 cdot 10^6 space Дж$.
Рассчитаем общее количество энергии, которое нам потребуется:
$Q = Q_1 + Q_2 = 0.7 cdot 10^6 space Дж + 4.6 cdot 10^6 space Дж = 5.3 cdot 10^6 space Дж$.
Ответ: $Q = 5.3 cdot 10^6 space Дж$.
Упражнение №2
Вычислите, какое количество энергии выделится при охлаждении водяного пара массой $2 space кг$ от $100 degree C$ до $0 degree C$.
Дано:
$m = 2 space кг$
$t_1 = 100 degree C$
$t_2 = 0 degree C$
$c = 4200 frac{Дж}{кг cdot degree C}$
$L = 2.3 cdot 10^6 frac{Дж}{кг}$
$Q — ?$
Показать решение
Скрыть
Решение:
Температура $100 degree C$ — это температура парообразования воды и конденсации водяного пара. При понижении температуры пар сначала сконденсируется в жидкость, а жидкость продолжит охлаждаться.
Количество теплоты, выделенное при этом будет равно:
$Q = Q_1 + Q_2$, где
$Q_1$ — количество выделенной теплоты при конденсации пара,
$Q_2$ — количество теплоты, выделенное при охлаждении жидкости до $0 degree C$.
$Q_1 = Lm$.
$Q_1 = 2.3 cdot 10^6 frac{Дж}{кг} cdot 2 space кг = 4.6 cdot 10^6 space Дж$.
$Q_2 = cm (t_1 — t_2)$.
$Q_2 = 4200 frac{Дж}{кг cdot degree C} cdot 2 space кг cdot (100 degree C — 0 degree C) = 8400 frac{Дж}{degree C} cdot 100 degree C = 840 space 000 space Дж approx 0.8 cdot 10^6 space Дж$.
$Q = 4.6 cdot 10^6 space Дж + 0.8 cdot 10^6 space Дж= 5.4 cdot 10^6 space Дж$.
Ответ: $Q = 5.4 cdot 10^6 space Дж$.
Упражнение №3
Из чайника выкипела вода объемом $0.5 space л$. Начальная температуры этой воды составляла $10 degree C$. Какое количество энергии оказалось излишне затраченным? Плотность воды — $1000 frac{кг}{м^3}$.
Дано:
$V = 0.5 space л$
$rho = 1000 frac{кг}{м^3}$
$L = 2.3 cdot 10^6 frac{Дж}{кг}$
СИ:
$0.5 cdot 10^{-3} space м^3$
$Q — ?$
Посмотреть решение и ответ
Скрыть
Решение:
После закипания воды в чайнике огонь выключают. Если его не выключить, то процесс кипения продолжится, и вода из чайника будет испаряться. Так как превращение воды в пар не является целью кипячения воды, энергию, которая ушла на парообразование можно считать излишне затраченной. Рассчитаем ее по формуле: $Q = Lm$.
Массу мы можем выразить через плотность и объем:
$m = rho V$.
Тогда наша формула примет вид:
$Q = Lrho V$.
$Q = 2.3 cdot 10^6 frac{Дж}{кг} cdot 1000frac{кг}{м^3} cdot 0.5 cdot 10^{-3} space м^3 = 2.3 cdot 10^6 frac{Дж}{кг} cdot 0.5 space кг = 1.15 cdot 10^6 space Дж$.
Ответ: $Q = 1.15 cdot 10^6 space Дж$.
Муниципальное
бюджетное общеобразовательное учреждение Московской области
Гимназия
№3
Определение
удельной теплоты парообразования.
учитель
физики
Ольга
Алексеевна Байшева
Дубна
– 2017
Содержание
1.Введение
2.Теоретические
исследования
3.Экспериментальные
исследования
4.Заключение
Введение
Практически
ежедневно мы сталкиваемся с таким явлением, как кипение. Но обращали ли вы
внимание, что температура воды во время процессе не меняется? Вопрос – куда
девается образующаяся энергия, если мы постоянно держим емкость на огне? Мы
заинтересовались изучением данного явления после «знакомства» с ним и
определением удельной теплоты парообразования на уроках физики 8 классе. Также
мы задались вопросом, что нужно сделать, чтобы самостоятельно рассчитать
удельную теплоту парообразования жидкости?
Данная тема
показалась нам достаточно интересной, и мы решили исследовать это.
Одной из
особенностей выбранной нами работы является доступность необходимого
оборудования и исследуемых материалов.
Цель работы:
определение удельной теплоты парообразование воды, изучение такого процесса как
кипение (испарение)
Методы
исследования: наблюдения, теоретические и
экспериментальные исследования
Задачи: изучить
литературу по данной теме;
Провести
лабораторную работу и определить удельную теплоту парообразования
Актуальность
и практическая значимость:
Интерес к теоретической и
экспериментальной физике, расширение кругозора в этой области, что помогает
совершенствовать исследовательские навыки.
Этапы работы:
* Подбор литературы
* Изучение теоретического материала
* Составление примерного плана работы
*
Экспериментальная часть, оформление результатов исследование
* Подготовка к отчету
Теоретические
исследования
Давайте
познакомимся с определениями «кипение» и «удельная теплота парообразования».
Что такое кипение?
Это физический процесс, в ходе которого происходит интенсивное парообразование
как на свободной поверхности жидкости, так и внутри ее структуры. Одним из
признаков кипения является образование пузырьков, которые состоят из
насыщенного пара и воздуха.
Стоит отметить
существование такого понятия, как температура кипения. От давления также
зависит скорость образования пара. Оно должно быть постоянным. Как правило,
основной характеристикой жидких химических веществ является температура кипения
при нормальном атмосферном давлении. Тем не менее на данный процесс также могут
оказать влияние такие факторы, как интенсивность звуковых волн, ионизация
воздуха.
Кипение является
фазовым переходом первого рода. Кипение происходит гораздо более интенсивно,
чем испарение с поверхности, из-за присутствия очагов парообразования,
обусловленных как более высокой температурой достигаемой в процессе кипения,
так и наличием примесей.

начинает образовываться пар во время такой процедуры, как нагревание. Кипение
подразумевает прохождение жидкости через 4 стадии:
1. На
дне сосуда, а также на его стенках начинают образовываться небольшие пузырьки.
Это является результатом того, что в трещинках материала, из которого
изготовлена емкость, содержится воздух, который расширяется под воздействием
высокой температуры.
2. Пузырьки
начинают увеличиваться в объеме, в результате чего они вырываются на
поверхность воды. Если верхний слой жидкости еще не достиг температуры кипения,
полости опускаются ко дну, после чего снова начинают стремиться вверх. Этот
процесс приводит к образованию звуковых волн. Именно поэтому во время кипения
воды мы можем услышать шум.
3. На
поверхность выплывает наибольшее количество пузырьков, что создает впечатление
мутности воды. После этого жидкость бледнеет. Учитывая визуальный эффект,
данную стадию кипения называют «белым ключом».
4. Наблюдается
интенсивное бурление, которое сопровождается образованием больших пузырей,
которые быстро лопаются. Этот процесс сопровождается появлением брызг, а также
интенсивным образованием пара.
В
кипящей жидкости устанавливается определённое распределение температуры: у
поверхностей нагрева (стенок сосуда, труб и т. п.) жидкость заметно перегрета.
Величина перегрева зависит от ряда физико-химических свойств как самой
жидкости, так и граничных твёрдых поверхностей. Тщательно очищенные жидкости,
лишённые растворённых газов (воздуха), можно при соблюдении особых мер
предосторожности перегреть на десятки градусов без закипания. Когда такая
перегретая жидкость в конце концов вскипает, то процесс кипения протекает
весьма бурно, напоминая взрыв. Вскипание сопровождается расплёскиванием
жидкости, гидравлическими ударами, иногда даже разрушением сосудов. Теплота
перегрева расходуется на парообразование, поэтому жидкость быстро охлаждается
до температуры насыщенного пара, с которым она находится в равновесии.
Возможность значительного перегрева чистой жидкости без кипения объясняется
затрудненностью возникновения начальных маленьких пузырьков (зародышей), их
образованию мешает значительное взаимное притяжение молекул жидкости. Иначе
обстоит дело, когда жидкость содержит растворенные газы и различные мельчайшие
взвешенные частицы.
Для кипения
требуется энергия. Большая ее часть используется для разрыва химических связей
между атомами и молекулами, в результате чего образуются пузырьки пара, а
меньшая идет на расширение пара, то есть на то, чтобы образовавшиеся пузырьки
могли лопнуть и выпустить его. Так как жидкость всю энергию вкладывает в
переход в газообразное состояние, ее «силы» иссякают. Для постоянного возобновления
энергии и продления кипения нужно подводить к емкости с жидкостью все новое и
новое тепло. Обеспечить его приток может кипятильник, газовая горелка либо
любой другой нагревательный прибор. Во время кипения температура жидкости не
растет, идет процесс образования пара такой же температуры.
Разным жидкостям
требуется разное количество теплоты для перехода в пар. Какое именно –
показывает удельная теплота парообразования.
Уде́льная теплота́
парообразова́ния и конденса́ции — физическая величина, показывающая, какое
количество теплоты необходимо, чтобы обратить количество жидкости с единичной
массой в пар без изменения температуры.
Если известно,
что вещество находится при температуре кипения, то для вычисления
количества теплоты, необходимого для превращения его в газообразное
состояние используют следующую формулу:
Обозначения:
количество
теплоты парообразования, Дж;
удельная
теплота парообразования и конденсации, ;
масса
вещества, кг.
Данная величина
очень важна для производственных процессов на основе современных технологий.
Например, на нее ориентируются при производстве металлов. Оказалось, что
если железо расплавить, а потом сконденсировать, при дальнейшем затвердении
образуется более прочная кристаллическая решетка.
Экспериментальные
исследования
Один из методов
основан на том, что при конденсации пара происходит выделение тепла в
количестве, равном теплоте парообразования. Пар получаем в парообразователе и
пропускаем через трубочку в воду, налитую в калориметр. При конденсации пара и
охлаждении полученной из него воды происходит нагревание воды в калориметре.
Оборудование:
парообразователь; электрическая плитка; калориметр с крышкой; электронные весы;
термометр.
Ход
работы
1. Наливаем
воду в калориметр.
2. Определяем
массу калориметра с водой и начальную температуру.
3. Нагреваем
воду до состояния кипения и дожидаемся интенсивного парообразования в
калориметре.
4. Ждем
примерно 5 мин.
5. Измеряем
массу калориметра с водой и температуру после 5 мин.
6. По
уравнению теплового баланса вычисляем L.
7. Делаем
выводы
Удельную теплоту
парообразования L вычисляют из уравнения теплового баланса:
приравнивают количества теплоты, полученные калориметром Q1=cкmкt1 и
водой в нём Q2=cвmвt1,
количеству теплоты, отданному паром Q3 = Lmп при
конденсации и горячей водой, полученной из пара при её охлаждении до конечной
температуры Q4 = cвmпt2:
Q1 + Q2 = Q3 + Q4,
или
cкmкt1 + cвmв
t1 = Lmп + cвmп
t2
L = (cкmкt1 + cвmв
t1 —
cвmпt2)
: mп
При вычислении L
из уравнения теплового баланса мы пренебрегли потерями тепла в калориметре.
L
= ( cвmвt1 —
cвmпt2)
: mп
Массу
сконденсировавшегося пара находят по разности результатов взвешивания
калориметра до и после пропускания пара. Обратите внимание на то, что колба
парообразователя изготовлена из специального, закалённого, стекла. Изделия из
такого стекла помечают матовой меткой в форме круга, прямоугольника или
треугольника. Колбу из такого стекла можно ставить не только на электроплитку,
но и на открытый огонь.
|
№ |
T1 0С |
T2 0С |
M1 кг |
M2 кг |
L 106 |
|
1 |
20 |
46 |
0,126 |
0,132 |
2,17 |
|
2 |
18 |
51 |
0,126 |
0,133 |
2,42 |
|
3 |
20 |
48 |
0,126 |
0,132 |
2,36 |
|
4 |
20 |
50 |
0,126 |
0,133 |
2,18 |
|
5 |
18 |
50 |
0,126 |
0,133 |
2,32 |
|
Ср. |
19,2 |
49 |
0,126 |
0,1326 |
2,29 |
Ср.ар. L = (2,17 + 2,42 + 2,36 + 2,18 + 2,32) * 106 : 5 = 2,29*106
Дж/кг
Табличное значение
– 2,3*106 Дж/кг
Погрешность
измерений
∆=∆и
+∆о
∆и
– инструментальная погрешность
Определяется
классом прибора
Для
весов +-1г
Для
термометра +-10С
∆о –
погрешность отсчета
Имеет
смысл говорить об этой погрешности только, если прибор не цифровой. Термометр
– аналоговый прибор; весы – цифровые. ∆о для термометра 10С
∆Т=∆иТ
+∆оТ=20 С
∆M=∆иM
=1г= 10-3кг
Относительные
погрешности измерения температуры
Относительные
погрешности измерения массы
Абсолютная погрешность косвенных измерений определяется методами
математической статистики. Для формулы
L
= ( cвmвt1 —
cвmпt2)
: mп
ДЖ/Кг
ДЖ/Кг
Заключение
L=(2,29)*106 ДЖ/Кг
Удельная теплота парообразования

4.6
Средняя оценка: 4.6
Всего получено оценок: 198.
4.6
Средняя оценка: 4.6
Всего получено оценок: 198.
Если жидкость разогреть до температуры кипения, то начнется процесс парообразования. Молекулы жидкости, получив дополнительную энергию, отрываются от поверхности и переходят в газообразное состояние. Это явление называется парообразованием. Обратный процесс, когда молекулы пара, потеряют излишки энергии и снова перейдут в жидкое состояние, называется конденсацией.
Удельная теплота парообразования
Удельной теплотой парообразования называется физическая величина равная количеству тепла, которое необходимо потратить, чтобы превратить жидкость массой 1 кг в пар. Обозначают эту единицу латинской буквой L. Формула удельной теплоты парообразования выглядит так:
$$L={Q over m}$$
где:
Q — количество тепла израсходованное на преобразование жидкости в пар, Дж;
m — масса жидкости, кг.
Значения L для разных веществ определяют экспериментально.
Зная L, можно вычислить количество тепла Q, которое необходимо сообщить телу массой m для его полного преобразования в пар:
$$Q={L*m}$$
В каких единицах измеряется удельная теплота парообразования
Удельная теплота парообразования в СИ (Международная система ) измеряется в джоулях на килограмм, Дж/кг. Для некоторых задач применяется внесистемная единица измерения – килокалория на килограмм, ккал/кг. Напомним, что 1 ккал = 4,1868 Дж.
После достижения точки кипения (температуры кипения) температура не возрастает, хотя тепло непрерывно поступает. Это объясняется тем, что после закипания почти все тепло идет на создание пара — разрыв молекулярных связей и отрыв от поверхности жидкости.
Удельная теплота парообразования некоторых веществ
Информацию о значениях удельной теплоты парообразования для конкретного вещества можно найти в технических справочниках или в их электронных версиях на интернет-ресурсах. Обычно они приводятся в виде такой таблицы “Удельная теплота парообразования, L”
|
Вещество |
105 * Дж/кг |
ккал/кг |
Вещество |
105 * Дж/кг |
ккал/кг |
|
Аммиак |
13,6 |
327 |
Скипидар |
3 |
70 |
|
Вода |
22,6 |
5,39 |
Спирт |
8,5 |
204 |
|
Железо |
0,58 |
13,9 |
Ртуть |
3,0 |
71 |
|
Сероуглерод |
3,5 |
84 |
Эфир |
3,5 |
84 |
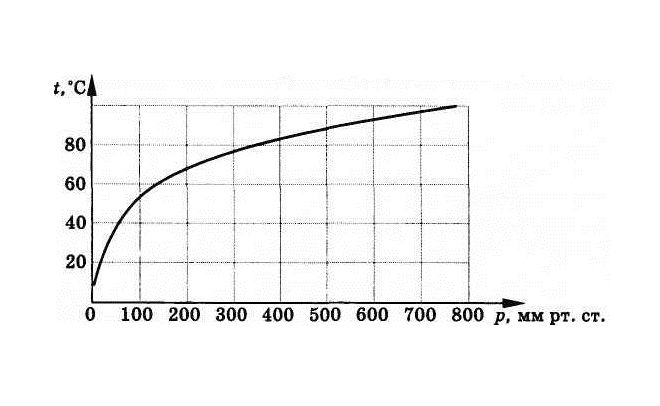
Температура кипения зависит от атмосферного давления. Чем ниже давление, тем меньше температура кипения. Например, температура кипения воды равна 1000С при нормальном атмосферном давлении, равном 760 мм.рт.ст. А если подняться в горы, на высоту порядка 4000 метров, то точка кипения у воды упадет до 800С.
Что мы узнали?
Мы узнали как определяется удельная теплота парообразования L. С помощью этой величины можно рассчитать количество тепла, требуемого для преобразования определенной массы жидкости в пар. Такие вычисления необходимо производить в промышленности, где в качестве теплоносителя используется пар, например на тепловых электростанциях.
Тест по теме
Доска почёта

Чтобы попасть сюда — пройдите тест.
Пока никого нет. Будьте первым!
Оценка доклада
4.6
Средняя оценка: 4.6
Всего получено оценок: 198.
А какая ваша оценка?